Давление пара растворов. Закон Рауля
Осмос
РАЗБАВЛЕННЫЕ РАСТВОРЫ НЕЭЛЕКТРОЛИТОВ
В начале XIX в. английский ученый Майкл Фарадей, изучая особенности водных растворов солей, кислот и оснований проводить электрический ток, пришел к заключению, что вещества можно разделить на электролиты и неэлектролиты.
Неэлектролитами называются вещества, растворы которых не проводят электрический ток. Примерами неэлектролитов являются водные растворы органических веществ (сахара, глюкозы, мочевины). Разбавленные растворы неэлектролитов проявляют ряд общих свойства, количественное выражение которых зависят только от концентрации и не зависит от природы растворенных веществ.
Односторонняя диффузия молекул растворителя через полупроницаемую перегородку называется осмосом. Сила, обусловливающая осмос, называется осмотическим давлением. Величина осмотического давления зависит от концентрации раствора и его температуры, но не зависит ни от природы растворенного вещества, ни от природы растворителя. Зависимость осмотического давления от температуры и концентрации раствора выражается уравнением Вант-Гоффа:
π = cB RT,
где π – осмотическое давление раствора, кПа; сВ – его молярная концентрация,
моль/л; R – универсальная газовая постоянная, 8,314 Дж/(моль ∙ К); T – абсолютная температура раствора.
При данной температуре давление насыщенного пара над жидкостью – величина постоянная. Опыт показывает, что при растворении в жидкости какого-либо вещества давление насыщенного пара над жидкостью понижается.
В разбавленных растворах неэлектролитов при постоянной температуре относительное понижение давления насыщенного пара растворителя над раствором равно молярной доле растворенного вещества (законРауля):
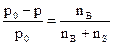 ,
,
где р0 – давление насыщенного пара над чистым растворителем; р – давление пара над раствором; nB – количество растворенного вещества; nS – количество растворителя.