Лекция № 2. АМИНОКИСЛОТЫ
Аминокислоты -производные карбоновых кислот, имеющие аминогруппу в a- положении. Классифицируются по строению, характеру заряженности и заменимости-незаменимости.
Аминокислоты являются карбоновыми кислотами, содержащими аминную и карбоксильную группы, которые находятся у одного и того же углеродного атома. В организме человека найдено около 70 аминокислот, причем 20 из них входят в состав белков. Это так называемые протеиногенные аминокислоты. Применительно к аминокислотам используют как систематическую номенклатуру, так и тривиальные названия. Последние чаще всего связаны с источником их получения. Так, тирозин был впервые выделен из сыра (от греч.tyros-сыр), аспарагиновая кислота – из спаржи (от лат.asparagus- спаржа) и т.д. Аминокислоты кроме карбонильной и аминной группировок содержат боковые радикалы, причем именно эти химические группировки определяют большинство свойств той или иной аминокислоты. В общем виде формула аминокислоты может быть представлена следующим образом:
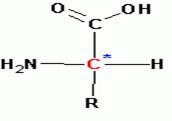
Классификация по строению.
а) моноаминомонокарбоновые;
б) диаминомонокарбоновые (лизин, аргинин, цитруллин)
в) моноаминодикарбоновые (аспарагиновая и глутаминовая кислоты);
г) диаминодикарбоновые (цистин).
Название по номенклатуре IUPAC формируется, как у карбоновых кислот вообще, с перечислением имеющихся в углеродной цепи заместителей. Например, аминокислота лизин, имеющая строение: 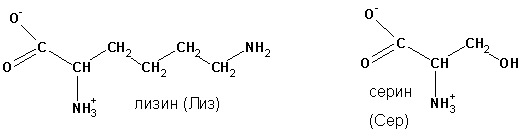
будет называться 2,6-диаминогексановая, а серин, соответственно, 2-амино-3-гидроксипропановая кислота. Однако, на практике, названия по номенклатуре IUPAC по отношению к протеиногенным аминокислотам никогда не применяют, обходясь исторически сложившимися тривиальными названиями. Исключение составляют лишь аспарагиновая и глутаминовая кислоты, для которых весьма часто используют названия аспартат и глутамат, соответственно.
Очень важным свойством аминокислот является строение так называемого бокового радикала R, поскольку остальная часть молекулы, включающая карбоксильную группу, аминогруппу, асимметрический атом углерода и водород для всех протеиногенных аминокислот совершенно одинакова:.
Наличие в боковом радикале R функциональных групп, таких, как сульфгидрильная –SH, карбаминовая H2N-C(=O)- , гидроксильная HO- , аминогруппа H2N-, карбоксильная HOOC- и некоторые другие, оказывает решающее значение не только при формировании вторичной, третичной и четвертичной структур белковой молекулы, но и на ее биологические функции. В водных средах при различных значениях рН эти группы отвечают за формирование электрических зарядов белковой молекулы, ее растворимость и ряд других физико-химических свойств. Например, замена одного-единственного аминокислотного остатка (глутаминовой кислоты в положении 6) в полипептидной цепи субъединицы гемоглобина на остаток аминокислоты валин приводит к такому изменению свойств молекулы гемоглобина, что это вызывает патологию, называемую “серповидноклеточная анемия”.
По характеру заряженности боковых радикалов аминокислоты подразделяют на:
а) неполярные гидрофобные (ГЛИ, АЛА, ВАЛ, ЛЕЙ, ИЛЕ, ПРО, ФЕН, ТИР, ТРИ, МЕТ);
б) полярные, но незаряженные (СЕР, ТРЕ, ЦИС, АСН, ГЛН);
в) полярные с отрицательным зарядом (АСП, ГЛУ);
г) полярные с положительным зарядом (ЛИЗ, АРГ, ГИС).
В зависимости от того, могут ли аминокислоты синтезироваться в организме или должны поступать в составе пищи, различают:
а) ЗАМЕНИМЫЕ,
б) НЕЗАМЕНИМЫЕ АК (лейцин, изолейцин, валин, лизин, гистидин, метионин, фенилаланин, треонин, триптофан). В детском возрасте также незаменимой является АК АРГИНИН.
Для человека АРГ, ТИР- полузаменимые, а для курицы- незаменимые.
Список 20 протеиногенных аминокислот млекопитающих:
| название | структура (R-CH(NH2)-COOH) | * | ** | |
| ГЛИЦИН | NH2-CH2-COOH | ГЛИ | G | |
| АЛАНИН | CH3-CH(NH2)-COOH | АЛА | A | |
| ВАЛИН | (CH3)2CH-CH(NH2)-COOH | ВАЛ | V | Н |
| ЛЕЙЦИН | CH3-CH(CH3)-CH2-CH(NH2)-COOH | ЛЕЙ | L | Н |
| ИЗОЛЕЙЦИН | CH3-CH2-CH(CH3)-CH(NH2)-COOH | ИЛЕ | I | Н |
| СЕРИН | HO-CH2-CH(NH2)-COOH | СЕР | S | |
| ТРЕОНИН | CH3-CH(OH)-CH(NH2)-COOH | ТРЕ | T | Н |
| ЦИСТЕИН | HS-CH2-CH(NH2)-COOH | ЦИС | C | |
| МЕТИОНИН | CH3-S-(CH2)2-CH(NH2)-COOH | МЕТ | M | Н |
| ЛИЗИН | NH2-(CH2)4-CH(NH2)-COOH | ЛИЗ | K | Н |
| АРГИНИН | NH2-C(=NH)-NH-(CH2)3-CH(NH2)-COOH | АРГ | R | ПЗ |
| АСПАРАГИНООВАЯ К-ТА | COOH-CH2-CH(NH2)-COOH | АСП | D | |
| АСПАРАГИН | NH2-C(=O)-CH2-CH(NH2)-COOH | АСН | N | |
| ГЛУТАМИНОВАЯ К-ТА | HOOC-(CH2)2-CH(NH2)-COOH | ГЛУ | E | |
| ФЕНИЛАЛАНИН | Ph-CH2-CH(NH2)-COOH | ФЕН | F | Н |
| ГЛУТАМИН | NH2-C(=O)-(CH2)2-CH(NH2)-COOH | ГЛН | Q | |
| ТИРОЗИН | HO-Ph-CH2-CH(NH2)-COOH | ТИР | Y | ПЗ |
| ТРИПТОФАН | 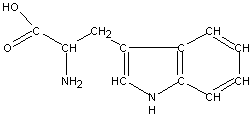
| ТРИ | W | Н |
| ГИСТИДИН | 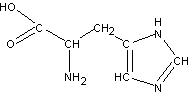
| ГИС | H | Н |
| ПРОЛИН | 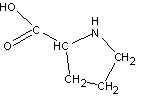
| ПРО | P |
*- однобуквенное международное обозначение
**- н- незаменимая; пз- полузаменимая; остальные- заменимые
Небелковые и редковстречающиеся аминокислоты:
ОКСИЛИЗИН (много в коллагене) NH2-CH2-CH(OH)-(CH2)2-CH(NH2)-COOH
a,g-ДИАМИНОПИМЕЛИНОВАЯ (только у бактерий) HOOC-CH(NH2)-(CH2)3-CH(NH2)-COOH
a-АМИНОАДИПИНОВАЯ (в белке зерна кукурузы) HOOC-(CH2)3-CH(NH2)-COOH
НЕПРОТЕИНОГЕННЫЕ АМИНОКИСЛОТЫ: b-АЛАНИН NH2-(CH2)2-COOH
ОРНИТИН 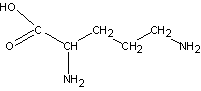
ЦИТРУЛЛИН 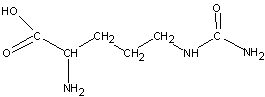
g-АМИНОМАСЛЯНАЯ КИСЛОТА NH2-(CH2)3-COOH