Очистка коллоидных растворов
Коллоидная защита
Устойчивость лиофобных золей против коагуляции возрастает в присутствии ВМС. Это проявляется в повышении порогов коагуляции у защищенного золя и неподчинении правилу Шульце-Гарди.
Способность защищать золи от коагуляции количественно выражают защитным числом, равным числу миллиграммов сухого ВМС, защищающего 10 мл золя от коагуляции при приливании к золю 1 мл 10%-го раствора NaCl.
В зависимости от природы золя защитное число называют «золотым» (золь золота), «серебряным» (золь серебра), «рубиновым» (конго красный), «железным» (оксид железа) и т.д. Чем больше величина защитного числа, тем слабее защитное действие данного ВМС. Наиболее сильное защитное действие у белков.
Механизм защитного действия можно объяснить тем, что макромолекулы ВМС адсорбируются на поверхности коллоидных частиц, создавая адсорбционно-сольватные слои, которые повышают гидрофильность коллоидных частиц. Вследствие этого усиливается взаимодействие частица-растворитель. Сольватные слои обеспечивают большое расклинивающее давление при сближении двух частиц и препятствуют их слипанию. Кроме того, адсорбционные слои стабилизатора обладают повышенными структурно-механическими свойствами. Защитное действие усиливается. Если в адсорбционном слое ВМС образуются гелеобразные структуры с высокой прочностью и упругостью. Таким образом, при введении защитных лиофильных коллоидов ведущую роль играют адсорбционно-сольватный и структурно-механические факторы устойчивости.
Защитное действие ВМС зависит от:
1. природы стабилизатора. Наибольшее защитное действие проявляется при одноименных зарядах ионогенных ВМС и частиц золя;
2. состава среды (влияние рН).
Некоторые молекулярно-кинетические свойства коллоидных систем используют для очистки золей от электролитов и молекулярных примесей, которыми полученные золи часто бывают загрязнены. Наиболее распространенными методами очистки коллоидных систем являются диализ, электродиализ и ультрафильтрация, основанные на свойстве некоторых материалов – т.н. полупроницаемых мембран (коллодия, пергамента, целлофана и т.п.) – пропускать ионы и молекулы небольших размеров и задерживать коллоидные частицы. Все полупроницаемые мембраны представляют собой пористые тела, и непроницаемость их для коллоидных частиц обусловлена тем, что коэффициент диффузии для коллоидных частиц значительно (на несколько порядков) меньше, чем для ионов и молекул, имеющих намного меньшие массу и размеры.
Прибор для очистки золей методом диализа называется диализатором; простейший диализатор представляет собой сосуд, нижнее отверстие которого затянуто полупроницаемой мембраной.
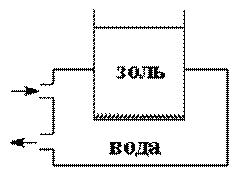
Схема диализатора
Золь наливают в сосуд и помещают последний в ёмкость с дистиллированной водой (обычно проточной); ионы и молекулы примесей диффундируют через мембрану в растворитель.
Диализ является очень медленным процессом; для более быстрой и полной очистки золей применяют электродиализ.

Схема электродиализатора
Электродиализатор состоит из трех частей; в среднюю часть, отделенную от двух других полупроницаемыми мембранами, за которыми помещены электроды, наливается золь. При подключении к электродам разности потенциалов катионы содержащихся в золе электролитов диффундируют через мембрану к катоду, анионы – к аноду. Преимущество электродиализа заключается в возможности удаления даже следов электролитов (необходимо помнить, что степень очистки ограничивается устойчивостью коллоидных частиц; удаление из золя ионов-стабилизаторов приведет к коагуляции).
Еще одним методом очистки золей является ультрафильтрация – отделение дисперсной фазы от дисперсионной среды путем фильтрования под давлением через полупроницаемые мембраны. При ультрафильтрации коллоидные частицы остаются на фильтре (мембране). Этот метод позволяет скорее отделить от коллоидного раствора электролиты и другие примеси, чем это происходит при диализе. На конечной стадии путем отсасывания дисперсионной среды можно сконцентрировать коллоидный раствор. При ультрафильтрации достигают высокой степени очистки дисперсной системы, периодически разбавляя ее водой.
СВОЙСТВА ДИСПЕРСНЫХ СИСТЕМ