Понятие об адсорбции
КЛАССИФИКАЦИЯ ДИСПЕРСНЫХ СИСТЕМ
Зміст
Література
1. А.М. Горячковский. Справочное пособие по клинической биохимии. Одесса. ОКФА. – 1994.
2. Марри Р., Греннер Д., Мейес П., Родуелл В. «Биохимия человека»: в 2-х томах. Пер. с англ.: - Москва, Мир, 1993.-384с.
3. Ф.Ф.Боєчко. Біологічна хімія: Навч. посібник. – К. : Вища шк., 1995. – 536с.
4. Біохімія : Практикум // М.Є. Кучеренко, Ю.Д. Бабенюк, В.М.Войницький, В.І. Гаврилей. – К.: Либідь, 1995. – 152с.
5. А.Т.Пилипенко, И.В.Пятницкий. Аналитическая химия: В 2-х книгах. – М. : Химия, 1990.
6. В.П.Васильєв. Аналитическая химия. В 2-х частях. Ч.2. Физико-химические методы анализа. – М. : Высш. шк., 1989. – 384с.
7. А.И. Кононский. Биохимия животных. – К.: Вища шк. – 1984. – 415 с.
8. А.Я. Николаев. Биологическая химия. – М.: Медицинское информационное агенство, 2001. – 496 с.
9. А. Ленинджер. Биохимия. //Пер. с англ. под ред. А.А. Баева и Я.М. Варшавского. – М.: Мир, 1974. – 957 с.
10. Справочник по клиническим лабораторным методам исследования. // Под ред. Е.А. Кост. – М.: Медицина. – 1975. – 383 с.
11. Филиппович Ю.Б. и др. Практикум по общей биохимии: Учеб. пособие для студ. хим. спец. пед. ин-тов. – М.: Просвещение, 1982. – 311 с.
12. Комаров Ф.И., Коровкин Б.Ф., Меньшиков В.В. Биохимические исследования в клинике. Л.: Медицина. –1976. – 384с
13. Каррер П., Курс органической химии, пер. с нем., 2 изд., Л., 1962; Фердман Д. Л., Биохимия, 3 изд., М., 1966.
14. А.Я Циганенко, В.И. Жуков, В.В. Масоедов, И.В. Завгородний. «Клиническая биохимія» (Учебное пособие для студентов медицинских вузов). – Москва. «Триада-Х». – 2002г. 504с.
15. Кольман Я., Рем К. Г. «Наглядная биохимия» Пер. с нем. — М.: Мир, 2000. - 469 с.,
16. Березов Т.Т., Коровкин Б.Ф. «Биологическая химия», - Москва, «Медицина» - 1998г. 704с.
17. Кноре Д.Г., Мизина С.Д. «Биологическая химия», - Москва, «Висшая Школа», 2000. – 479 с.
18. Клінічна біохімія: Практикум. Навч. посібник. // В.М.Безпальченко. – Херсон. ХДТУ. 2003. – 124 с.
| С. | |
| Лекція № 1. Вступ 1. Предмет вивчення клінічної біохімії. Розділи дисципліни. 2. Організація роботи клініко-діагностичної лабораторії. Етапи формування діагнозу. 3. Поняття "норма". Фактори біологічної варіації. 4. Клінічна аналітика. Контроль якості біохімічних досліджень: внутрішньолабораторний і міжлабораторний. Метод Юдена. 5. Уніфікація клінічних досліджень. | |
| Лекція 2. Фізико-хімічні методи аналізу, які застосовують в медицині 1. Класифікація методів. 2. Оптичні методи: фотометрія, рефрактометрія, поляриметрія. 3. Електрохімічні методи. рН-метрія. | |
| Лекція № 3. Обмін речовин. Обмін білків 1. Обмін речовин. 2. Обмін білків. Загальна характеристика білків: хімічна будова, властивості, функції, травлення. 3. Небілкові азотисті компоненти крові. Залишковий азот. 4. Загальна характеристика та патологія обміну сечовини, креатину, креатиніну, сечової кислоти, індикану, амінокислот. | |
| Лекція 4. Білки плазми крові. Методи дослідження білків 1. Функції і властивості білків плазми крові. 2. Патологія білків плазми крові: дис-, пара-, дефектпроїнемія. 3. Методи дослідження білків: електрофоретичні, імунохімічні, хроматографічні та хімічні. | |
| Лекція 5. Ферменти. Обмін вуглеводів 1. Загальна характеристика ферментів, як біологічних каталізаторів: властивості, класифікація, номенклатура, механізм дії, активність. Вплив на активність різних чинників. 2. Клінічна ферментологія. 3. Обмін вуглеводів: загальна характеристика, хімічна будова, біологічні функції, травлення. | |
| Лекція 6. Обмін вуглеводів та ліпідів 1. Патологія обміну вуглеводів. Тести толерантності до глюкози. 2. Цукровий діабет. 3. Ліпіди: загальна характеристика, будова, функції, травлення. 4. Ліпіди плазми крові. | |
| Лекція 7. Водно-солевий обмін 1. Обмін води й мінеральних речовин у нормі й патології. Регуляція водно-сольового обміну. Значення води. 2. Мінеральний обмін | |
| Лекція 8. Вітаміни. Біологічне окиснення. Сеча 1. Загальна характеристика вітамінів, класифікація, вплив на організм. Авітамінози. 2. Біологічне окиснення. 3. Загальна характеристика сечі. | |
| Лекція 9. Рідини внутрішнього середовища організму. Гормони. Обмін речовин у нервовій тканині 1. Кров, її фізико-хімічні властивості. 2. Загальна характеристика лімфи. 3. Загальна характеристика гормонів. 4. Обмін речовин у нервовій тканині. | |
| Література |
Дисперсные системы в коллоидной химии состоят по меньшей мере из двух фаз: сплошной дисперсионной среды и раздробленной дисперсной фазы. По агрегатному состоянию выделяют 9 типов дисперсных систем (табл. 1.1).
Примеры по каждой из систем можно найти в пособии для практических занятий по коллоидной химии.
Согласно классификации, по взаимодействию между частицами все дисперсные системы можно разделить по кинетическим свойствам дисперсной фазы на свободнодисперсные и связнодисперсные системы с подвижной и неподвижной фазами соответственно.
Таблица 1.1
Классификация дисперсных систем по агрегатному состоянию фаз
| Дисперсионная среда | Дисперсная фаза | Обозначение |
| Твердая Жидкая Газообразная | Твердая Жидкая Газообразная Твердая Жидкая Газообразная Твердая Жидкая Газообразная | Т/Т Ж/Т Г/Т Т/Ж Ж/Ж Г/Ж Т/Г Ж/Г Г/Г |
Свободнодисперсные системы делят на ультрамикрогетерогенные (10-7 –10-5 см), микрогетерогенные ( 10-5 – 10-3 см ) и грубодисперсные ( > 10-3 см ).
Ультрамикрогетерогенные системы называют коллоидными, или золями. Различают твердые золи – системы Т/Т, аэрозоли – золи с газообразной дисперсионной средой, лиозоли – золи с жидкой дисперсионной средой. Лиозоли, в свою очередь, в зависимости от природы среды делятся на гидрозоли (вода), алкозоли (спирты), этерозоли (эфиры) и т. д.
Микрогетерогенные системы включают суспензии (Т/Ж), эмульсии (Ж/Ж), пены (Г/Ж), порошки (Т/Г). Из грубодисперсных систем чаще встречаются Т/Г (песок, щебень).
Коллоидная химия изучает объекты, которые широко распространены в повседневной жизни. Гетерогенное состояние в какой-то мере универсально и является одной из ступеней строения материалов, следующей после атомов и молекул.
Представления коллоидной химии используются в материаловедении, астрономии, метеорологии, биологии, почвоведении и т. д. Методы этой науки применяются в коксохимии, производстве пластмасс, стройматериалов, нефтедобыче и других отраслях промышленности.
2. АДСОРБЦИЯ НА ГРАНИЦЕ РАЗДЕЛА ТВЕРДОЕ ТЕЛО – ГАЗ
Пусть поверхность твердого тела граничит с газом. Частицы внутри твердого тела образуют кристаллическую решетку, их взаимодействие уравновешено. В то же время взаимодействия частиц на поверхности твердого тела не уравновешены, поэтому молекулы газовой фазы будут притягиваться поверхностью, что приведет к повышению концентрации на поверхности по сравнению с объемом газа. Это явление называется адсорбцией и представляет собой концентрирование вещества на границе раздела фаз. Вещество, поглощаемое из объемной фазы, называется адсорбатом или адсорбтивом, а вещество, на поверхности которого идет адсорбция, называется адсорбентом. Явление адсорбции открыто в 18 веке Шееле, Фонтана, Ловитцем.
Различают физическую адсорбцию и хемосорбцию. Физическая адсорбция протекает самопроизвольно с установлением динамического равновесия между скоростью адсорбции и десорбции. Хемосорбция необратима, так как идет с образованием новых соединений.
Существует ряд способов количественного выражения адсорбции.
1. Величина Г, или гиббсовская адсорбция – избыток числа молей адсорбата в объеме поверхностного слоя площадью 1 см2 по сравнению с числом молей в том же объеме, если бы у межфазной границы не происходило изменение концентрации адсорбата.
2. a – количество адсорбата в объеме адсорбционного слоя, отвечающего единице массы адсорбента, моль/г.
3. 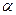 – количество адсорбированного вещества на единицу поверхности адсорбента, моль/м2, ммоль/см2.
– количество адсорбированного вещества на единицу поверхности адсорбента, моль/м2, ммоль/см2.
Адсорбцию можно характеризовать изотермой, которая представляет собой зависимость количества адсорбированного вещества от концентрации (давления) в объеме фазы при постоянной температуре. На рис 2.1 схематически представлен вид изотерм при разных температурах. Изотерму можно разбить на 3 участка: начальный – почти линейный, когда адсорбция прямо пропорциональна концентрации, а поверхность почти свободна, конечный, отвечающий полному заполнению поверхности, и промежуточный участок, соответствующий средним степеням заполнения.
.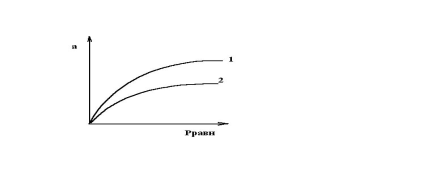
Рис. 2.1. Вид изотермы адсорбции при разных температурах:
1 – для Т1 2. Для Т2. Т1 < T2
Изотерма адсорбции описывается эмпирическим уравнением Фрейндлиха:
a = x/m.Kp1/n , (2.1)
где x – количество адсорбированного вещества, m – масса адсорбента, p – равновесное давление газа, К и 1/n – константы
Для адсорбции из раствора a = 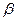 C1/n , (2.2)
C1/n , (2.2)
где С – равновесная концентрация. Если С = 1, то а = b . С ростом температуры К и b уменьшаются, а 1/n увеличивается. Константы уравнения можно определить графически. Для этого нужно прологарифмировать уравнение (2.2 ).
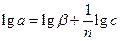 . (2.3)
. (2.3)
Это уравнение в координатах lga – lgC будет прямой линией. Обычно а выражают в ммоль/г, а С в ммоль/л. Уравнение Фрейндлиха пригодно только для интервала средних концентраций.