Биосинтез Хс.
На синтез одной молекулы Хс (С27 необходимо 18 молекул АТФ и 18 молекул ацетилКоА.
2 стадия: мевалоновая кислота превращается в сквален.

3стадия

сквален
холестерин
Синтезируемый в печени Хс упаковывается в ЛОНП вместе с жирами, которые
поступают в кровь, из них образуются ЛНП, которые снабжают Хс органы и ткани. Как
предотвратить накопление Хс в органах и тканях?
Этому способствуют другие транспортные частицы: ЛВПЗ, которые синтезируются в
печени и содержат небольшое количество Хс. Они поступают в кровь, взаимодействуют
с ЛНП либо с клетками тканей —> кровь, забирают избыток Хс из них.
Функционирование ЛНП и ЛВП поддерживает гомеостаз Хс в клетках.
Каким образом ЛВП забирают избыток Хс из других липопротеинов, органов и тканей?
Это связано с присутствием на поверхности ЛВПЗ фермента, который называется
лицетинХсацилтрансфераза (ЛХАТ). Здесь же на поверхности присутствует его
кофактор - А1. Этот фермент отщепляет ЖК от фосфолипидов на поверхности ЛВПЗ и
переносит ее на гидроксильную группу Хс.
В результате образуются ЭХс.
ЭХс - гидрофобные, погружаются внутрь ЛВПЗ.
Концентрация Хс на поверхности снижается и освобождается место для Хс и других
частиц.

|

|
Таким образом ЛВПЗ извлекают Хс из мембран клеток. В результате образуется ЛВП2 с
большим содержанием Хс —> печень, там распадается.
Хс используется для синтеза желчных кислот. В конечном итоге избыток Хс выводится с
желчью, либо в виде свободного Хс, либо в виде желчных кислот. Около 1г Хс
выводится из организма с фекалиями. 50% в составе желчи, в виде желчных кислот и
50% в виде капростенола, который образуется из Хс в нижних отделах кишечника под
действием микрофлоры.
Нарушение баланса между ЛНП и ЛВП может привести к липопротеинемиям. Например, гиперхиломикронемия (дефект ЛП-липазы), гиперхолестеринемия (нарушение поглощения ЛНП клетками), увел. концентрации Хс - основной патогенетический фактор развития атеросклероза.
Главное проявление: отложение Хс в стенках в основном, крупных сосудов.
Предрасположенность к нему считается по коэффициенту атерогенности.
ЛНП еще называют атерогенными.
Для возникновения атеросклероза имеют значение первичные повреждения кровеносных сосудов: при гипертонии, воспалительных процессах, сахарном диабете, нарушении свертываемости, действии токсических веществ (например, курении). В результате нарушается барьер проницаемости сосудов (повышаются промежутки между эндотелиальными клетками, в эти области проникают ЛНП, которые поглощаются макрофагами, все компоненты ЛНП разрушаются лизосомальными ферментами, кроме Хс) —>Хс накапливается, инкапсулируется соединительной тканью, образуется атеросклеротическая бляшка, в которую могут откладываться соли Са.
В результате стенки сосудов деформируются, сужается их просвет. При атеросклерозе поток ЛНП в клетке преобладает.
Профилактика атеросклероза.
Диета и потребление ненасыщенных жирных кислот, которых много в растительном масле. N Хс = 3,6 - 6,4 ммоль/л, человек должен стремиться к значению 5,5 ммоль/л.
Обмен нуклеотидов.План:
1. переваривание нуклеиновых кислот (НК)
2. синтез пуриновых нуклеотидов
3. синтез пиримидиновых нуклеотидов
4. катаболизм пуриновых нуклеотидов
5. катаболизм пиримидиновых нуклеотидов
6. синтез дезоксирибонуклеотидов
1. Ни нуклеотиды, ни пуриновые основания исходные, поступившие с пищей, не включаются в НК тканей человека, а также не в пуриновые и пиримидиновые коферменты (НАД, ФАД, КоА).
В организме человека нуклеотиды, необходимые для синтеза НК, синтезируются заново или деново.
Нуклеотидыпоступают в организм, в составе НК, а НК в составе нуклеопротеинов (икра, печень, молока, почки, рыба, шоколад, кофе, какао, чай, красное вино, мясо, яйца, молоко, сыр - практически нет).
Под действием фермента поджелудочной железы рибонуклеазы и дезоксирибонуклеазы расщепляют 3,5-фосфодиэфирные связи и НК расщепляются до нуклеотидов. Нуклеотидазы и фосфатазы гидролизуют нуклеотиды до нуклеозидов. Нуклеозиды либо всасываются, поступают в печень, где подвергаются катаболизму, либо небольшое количество расщепляется до пуриновых и пиримидиновых оснований в слизистой кишечника под действием фосфатазы, здесь же могут окисляться, т.е. расщепляться до конечных продуктов, которые всасываются и затем выводятся с мочой.
2. Синтезируются пуриновые и пиримидиновые нуклеотиды из СО^ , аспарагиновой
кислоты, глутамата, глицина и рибозы.
Путь синтеза пуринов завершается образованием икозин-5-монофосфата, который затем превращается в АМФ и ГМФ. Конечный продукт синтеза пиримидинов-УМФ, который является предшественником других пиримидинов. В обоих синтезах участвует ТГФ (Н4-фолат), как переносчик одноуглеродных фрагментов. Азотистые основания синтезируются из простых соединений, донорами С и N служат:
глицин
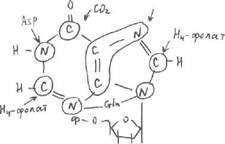 Для пуриновых нуклеотидов существует 2 пути:
Для пуриновых нуклеотидов существует 2 пути:
1. сборка из мелких фрагментов
2. из азотистых оснований, полученных при катаболизме (20% от общего синтеза,
называется «путь спасения»)
Синтез включает много реакций:
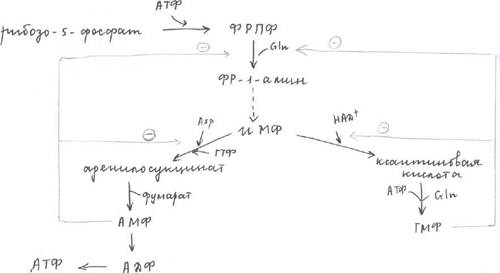
|
ПФП поставляет нам рибозо-5-фосфат, который под действием АТФ и 1 фермента превращается в фосфорибозилпирофосфат, который под действием второго фермента и амидной группы глутамина превращается в фосфорибозил-1-амин. ИМФ - инозинмонофосфат ТМФ - гуанозинмонофосфат