Поведение гидроксикислот при нагревании
Поведение дикарбоновых кислот при нагревании
Результат нагревания дикарбоновых кислот зависит от взаимного расположения карбоксильных групп:
1. Декарбоксилирование (в случае близкого расположения карбоксильных групп ):
НОСО – СООН ® СО2 + НСООН
НООС – СН2 – СООН ® СО2 + СН3СООН
НООС-СНR-СООН ® СО2 + R-СН2СООН
алкилуксусная кислота
Одно- и двузамещенные гомологи малоновой кислоты используются для получения алкилуксусных кислот.
2. Дегидратация с образованием циклических ангидридов (для янтарной и глутаровой кислот):
СН2СООН СН2СО
¾® Н2О + О
СН2СООН СН2СО
янтарный ангидрид
3. Декарбоксилирование и дегидратация с образованием циклических кетонов ( для адипиновой и других кислот с большим числом атомов углерода):
a-гидроксикислоты при нагревании отщепляют воду и образуют циклические сложные эфиры – лактиды, состоящие из остатков двух молекул:
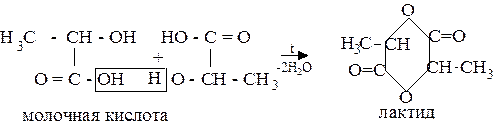 |
b-гидроксикислоты при нагревании образуют непредельные кислоты:
t
СН2 – СН – СООН ¾¾¾® СН2 =СН –СООН
ОН Н -Н2О