АКТИВНАЯ РЕАКЦИЯ ВОДНЫХ РАСТВОРОВ
Биохимия животных
Электронный дидактический комплекс (ЭДК)
Настоящий электронный дидактический комплекс (ЭДК) объединяет в себе несколько функций учебных материалов:
- Информационная текстовая часть учебного курса «биохимия животных с основами физколлоидной химии».
- Наглядные материалы (рисунки, схемы, таблицы).
- Материалы для самоконтроля знаний обучающихся.
В текстовой части кратко изложены основные термины и понятия с выделением ключевых слов. В дополнительный блок ЭДК помещены краткие учебные пособия, методические разработки по биохимии животных.
Составители: заведующий кафедрой органической и биологической химии Казанской государственной академии ветеринарной медицины доктор ветеринарных наук профессор Хазипов Нариман Залилович, доцент кафедры биохимии Казанского государственного университета Аскарова Альфия Наримановна, доценты кафедры органической и биологической химии Казанской государственной академии ветеринарной медицины доктор биологических наук Логинов Георгий Павлович, Тюрикова Раиса Павловна, Закирова Лилия Азатовна, ассистент кафедры Казанской государственной академии ветеринарной медицины Шилова Светлана Вячеславовна.
Техническое исполнение осуществлено кандидатом ветеринарных наук ассистентом КГАВМ Усольцевым Константином Валерьевичем.
При разработке ЭДК были использованы учебники «Биохимия животных» (Н.З.Хазипов, А.Н.Аскарова, 2003 г.), «Биохимия» (В.П.Козлов, В.Н.Шведова, 2004 г.), «Физическая и коллоидная химия» (М.М.Равич-Щербо, В.В.Новиков, 1975), «Методическое пособие по физической и коллоидной химии» (Р.П.Тюрикова, 2001 г.).
ФИЗИЧЕСКАЯ ХИМИЯ
ВОДА
Как известно, жизнь зародилась в воде и по-прежнему остается тесно связанной с водой. Вода является источником кислорода в атмосфере Земли. Это происходит при фотосинтезе в растениях, при этом энергия света преобразуется в энергию химических связей молекул. Животный мир может использовать только энергию, освободившуюся из этих химических связей в форме АТФ и других трифосфатов.
Вода составляет от 50 до 98% от общей массы организма. Каждая клетка и каждая ткань содержит определенное количество воды, так кожа содержит 72%, сердце – 79%, спинной и головной мозг – 70%, кровь – 79%, лимфа – 96%. С помощью воды осуществляется перенос питательных веществ и продуктов обмена веществ; вода играет важную роль в осмотических явлениях, в сохранении коллоидного состояния протоплазмы и т.д.
Вода обеспечивает растворение веществ, процессы всасывания, передвижения, набухания, осмоса и многих других. Высокая теплоемкость, теплопроводность, теплота испарения воды способствует поддержанию температуры тела у теплокровных животных. Она участвует в реакциях гидролиза, вызывает диссоциацию молекул (электролитов). Вода – конечный продукт обмена веществ в организме
Уникальные свойства воды Н2О становятся очевидными при сравнении с метаном (СН4). Обе молекулы одинаковы по массе и размерам. Тем не менее температура кипения воды на 250°С выше по сравнению с температурой кипения метана. В результате вода на поверхности Земли находится в жидком, а метан – в газообразном состоянии. Высокая точка кипения воды является следствием высокой теплоемкости испарения, что в свою очередь обусловлено неравномерным распределением электронной плотности в молекуле воды. Молекула воды имеет форму тетраэдра, в центре которого расположен атом кислорода. Две вершины тетраэдра заняты свободными электронными парами атома кислорода, а остальные две – атомами водорода. Поэтому связи Н—О—Н расположены под углом друг к другу. Кроме того, из-за высокой электроотрицательности атома кислорода связь О—Н полярна. т. е. молекула воды представляет собой электрический диполь.
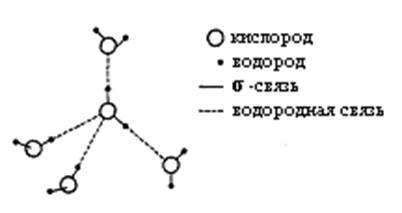
Каждая молекула тетраэдрически координирована с четырьмя другими молекулами воды, благодаря водородным связям энергия диссоциации водородной связи составляет 25 кДж/моль.
Биполярное строение молекул воды благоприятствует образованию водородных связей. Поэтому у воды в жидком состоянии многие молекулы связаны между собой водородными «мостиками». Часто образуются тетраэдрические структуры, так называемые "кластеры" воды. Поскольку в твердом состоянии расстояние между молекулами в среднем больше, чем в жидкости, плотность льда меньше по сравнению с плотностью воды. Это свойство воды очень важно в экологическом отношении, т.к. зимой на поверхности водоемов образуется слой льда, и они редко промерзают до дна.
Вода имеет высокую константу диэлектрической проницаемости, т.е. в воде электростатическое притяжение двух противоположно заряженных ионов снижается примерно в 80 раз.
В этом полярном растворителе (воде) хорошо растворяются полярные молекулы. Они окружаются молекулами воды, происходит гидратация молекул.
Электростатические силы притяжения удерживают молекулы воды, тем самым разрушая межионные или внутримолекулярные связи самой гидратированной молекулы.

Рис.1.1. Электростатические силы притяжения
АКТИВНАЯ РЕАКЦИЯ ВОДНЫХ РАСТВОРОВ
Под активной реакцией среды понимают концентрацию водородных ионов. В числе различных физико-химических защитных констант организма таких, как изотермия, изотония и другие постоянство концентрации водородных ионов – изогидрия – имеет особо важное значение для биологических процессов организма. Физико-химическое состояние белков, каталитическая функция ферментов, активность солевых ионов зависят от концентрации ионов водорода.