Ионное произведение воды. Водородный показатель рН
Равновесие электролитической диссоциации воды:
Н2О⇆Н+ + ОН−
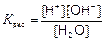
K[H2O] = Kw;
Kw = [H+]∙[OH−] = 10−14
Kw = 10−14,
[H+]∙[OH−] = 10−7
Величина Kw – называется ионным произведением воды. Расчет концентраций ионов водорода и гидроксид-ионов в водных растворах ведется по величине Kw:


где [H+] и [OH−] – равновесные молярные концентрации ионов.
В нейтральном водном растворе [H+] = [OH−] = 10−7 моль/л.
В кислом растворе [H+] > [OH−], [H+] > 10−7 моль/л.
В щелочном растворе [OH−] > [H+], [H+] < 10−7 моль/л.
В технике для характеристики кислотности растворов используют величину водородного показателя рН:
рН = -lg[H+].
Гидроксидный показатель pOH = -lg[OH−].
Наглядно шкалу рН можно выразить схемой:
 |
0 7 14
кислая нейтральная щелочная
рН < 7, pOH > 7 pH = 7 pH > 7, pOH < 7