Эквиваленты.
Химическим эквивалентом элемента называется такое его количество, которое соединяется с 1 молем атомов водорода или замещает то же количество атомов водорода в химических реакциях. Химический эквивалент не является постоянной величиной, он зависит от валентности элемента
5) Закон эквивалентов: (В. Рихтер, 1793 г.) – вещества взаимодействуют между собой в количествах, пропорциональных их химическим эквивалентам.
Значение эквивалентной массы элемента определяется по уравнению:
Э=А/В, (1) где
Э - эквивалентная масса элемента;
А - атомная масса элемента;
В - валентность элемента в данном соединении.
Например, ЭAl в Аl2О3 равен 27/3=9 г/моль; ЭCa в СаSO4 равен 40,08/2=20,04 г /моль.
Эквивалентом сложного вещества называется такое его количество, которое взаимодействует без остатка с одним эквивалентом водорода или с одним эквивалентом любого другого вещества.
Эквивалентную массу вещества вычисляют из его молярной массы:
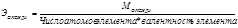
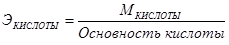
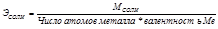
, где
М - молярная масса.
Основность кислоты определяется числом атомов водорода, которое отдаёт молекула кислоты, реагируя с основанием.
Кислотность основания определяется числом протонов, присоединённых молекулой основания при взаимодействии его с кислотой.
Подобно эквивалентной массе элемента, эквивалентная масса сложного вещества может иметь несколько значений в зависимости от реакции, в которой участвуют вещества.
Например, в реакции:
H3PO4 + NaOH à NaH2PO4 + H2O.
Эквивалентная масса кислоты равна её мольной массе:
Э(H3PO4) = М / 1 = 98 г / моль.
В реакции
H3PO4 + 2NaОН à Na2HPO4 + 2H2O
Э(H3PO4) = М / 2 = 49 г / моль.
В реакции
H3PO4 + 3NaОН à Nа3РO4 + ЗН2О
Э(H3PO4) = M / 3 = 32.7 г / моль.
Эквивалентный объем водорода при н.у. равен 11,2 л(кислорода – 5.6)
3.