Метод трилонометрии
Методом трилонометрии можно определить содержание не только ионов Са2+, но и ионов Mg2+, которые также имеются в составе слюны от 0,1 до 0,5 ммоль/л.
В основе метода лежит реакция образования прочного комплекса иона Са2+ или Mg2+ с трилоном Б (двунатриевая соль этилендиаминтетрауксусной кислоты) при рН = 8-10, создаваемом с помощью аммиачного буферного раствора.
Для фиксации наступления состояния эквивалентности используют металл-индикатор хромоген черный, который может образовывать непрочный комплекс с ионом определяемого металла. Индикатор представляет собой слабый электролит, ионизирующий по-разному в зависимости от рН раствора:
H3V ↔ H2V- + H+ (винно-красный) ↔ HV2- + 2H+ (синий) ↔ V3- + 3H+ (оранжевый)
рН< 6 pH=6 pH=7-11 pH=11,5
При рН = 9,5-10 комплекс Са2+ с индикатором имеет винно-красную окраску:
Са2+ (синий) + HV2- → СаV- (винно-красный) + H+
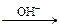 При титровании трилоном Б в точке эквивалентности наблюдается полный переход металла из непрочного комплекса с индикатором в более прочный комплекс с трилоном Б (бесцветным), и винно-красная окраска меняется на синюю:
При титровании трилоном Б в точке эквивалентности наблюдается полный переход металла из непрочного комплекса с индикатором в более прочный комплекс с трилоном Б (бесцветным), и винно-красная окраска меняется на синюю:
СаV- + Na2H2Y Na2СаY + HV2- + H+
винно-красн. б/цветн. б/цветн. синяя
 или:
или:
Ход определения:
Предварительно проведите определение ионов Са2+ и Mg2+ в контрольном растворе (получить у преподавателя) по указанной методике.
Для определения суммарного содержания ионов Са2+ и Mg2+ в коническую колбу с помощью пипетки отмерьте 10,0 мл исследуемой слюны. Добавьте 5 мл буферного раствора мерной пробиркой и несколько кристалликов индикатора. Исследуемый раствор приобретает винно-красную окраску. Титруйте из бюретки трилоном Б до перехода винно–красной окраски в синюю. Показания бюретки отметьте с точностью до 0,1 мл. Титрование повторите до получения двух результатов, отличающихся не более чем на 0,1 ± 0,2 мл. По 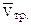 рассчитайте содержание ионов Са2+ и Mg2+ в слюне, ммоль/л. СЭтрилона = 0,01 моль экв/л. Результаты титрования занесите в табл. 2.1.
рассчитайте содержание ионов Са2+ и Mg2+ в слюне, ммоль/л. СЭтрилона = 0,01 моль экв/л. Результаты титрования занесите в табл. 2.1.
Для определения содержания только ионов Са2+ также в коническую колбу отмерьте пипеткой 10,0 мл исследуемой слюны, добавьте 1 мл раствора NaOH (CЭ = 1 моль экв/л), выдержите не менее 5 мин. Затем добавьте 5 мл буферного раствора и несколько кристалликов индикатора мурексида. Исследуемый раствор приобретает ярко розовую окраску. Титруйте из бюретки трилоном Б до перехода окраски в фиолетовую. Показания бюретки занесите в таблицу 2.1. Опыт повторите дважды. По среднему объему трилона Б, пошедшего на титрование, рассчитайте содержание ионов Са2+ в слюне.
По разности в объемах трилона Б рассчитайте содержание ионов Mg2+ в слюне. Все полученные данные также занесите в таблицу 2.1.
Таблица 2.1
Результаты трилонометрического определения содержания ионов кальция и магния в слюне
| № опыта | Vслюны, мл | Vтрилона, мл |  ,
мл ,
мл
| 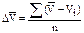 ,
мл ,
мл
| Относит. ошибка
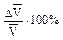
| Содержание, ммоль/л | ||||
| Mg2+ и Са2+ | Са2+ | Mg2+ | ||||||||
| Mg2+ и Са2+ | Са2+ | |||||||||
| 10,0 | ||||||||||
| 10,0 |