Постулат Клаузиуса

Рудольф Юлиус Эммануэль Клаузиус
Второй закон термодинамики, как и первый, также выведен опытным путём. Автором первой формулировки второго закона термодинамики считается немецкий физик, механик и математик Рудольф Клаузиус.
«Теплота сама собой не может переходить от тела холодного к телу горячему». Это утверждение, которое Клазиус назвал «тепловой аксиомой», было сформулировано в 1850 г. в работе «О движущей силе теплоты и о законах, которые можно отсюда получить для теории теплоты». «Само собой теплота передаётся лишь от тела с более высокой температурой к телу с меньшей температурой. В обратном направлении самопроизвольная передача теплоты невозможна». Таков смысл постулата Клаузиуса, определяющего суть второго закона термодинамики.
Обратимые и необратимые процессы
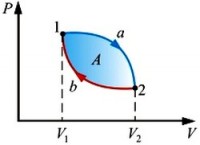
Первый закон термодинамики показывает количественную связь между теплотой, полученной системой, изменением её внутренней энергии и работой, произведённой системой над внешними телами. Но он не рассматривает направление передачи теплоты. И можно предположить, что теплота может передаваться как от горячего тела к холодному, так и наоборот. Между тем, в действительности это не так. Если два тела находятся в контакте, то теплота всегда передаётся от более нагретого тела к менее нагретому. Причём этот процесс происходит сам по себе. При этом во внешних телах, окружающих контактирующие тела, никаких изменений не возникает. Такой процесс, который происходит без совершения работы извне (без вмешательства внешних сил), называется самопроизвольным. Он может быть обратимым инеобратимым.
Самопроизвольно остывая, горячее тело передаёт свою теплоту окружающим его более холодным телам. И никогда само собой холодное тело не станет горячим. Термодинамическая система в этом случае не может возвратиться в первоначальное состояние. Такой процесс называется необратимым. Необратимые процессы протекают только в одном направлении. Практически все самопроизвольные процессы в природе необратимы, как необратимо время.
Обратимымназывается термодинамический процесс, при котором система переходит из одного состояния в другое, но может вернуться в исходное состояние, пройдя в обратной последовательности через промежуточные равновесные состояния. При этом все параметры системы восстанавливаются до первоначального состояния. Обратимые процессы дают наибольшую работу. Однако в реальности их нельзя осуществить, к ним можно только приблизиться, так как протекают они бесконечно медленно. На практике такой процесс состоит из непрерывных последовательных состояний равновесия и называетсяквазистатическим. Все квазистатические процессы являются обратимыми.
10) Все термодинамические процессы, протекающие в замкнутой системе, подразделяющиеся на обратимые и необратимые.
Термодинамический процесс называется обратимым, если, протекая в обратном направлении, он возвращает систему в исходное состояние без затрат энергии.
(упругая деформация тел, незатухающие колебания).
Все изопроцессы идеального газа являются обратимыми. В противном случае процесс называется необратимым.
Все реальные процессы необратимы, т.к. их нельзя провести в обратном направлении без затраты дополнительной энергии (расширение газа в пустоту, затухающие колебания, взрыв).
Если прямой необратимый процесс АВС дополнить обратным процессом СДА, то получим замкнутый процесс, называемый круговым или циклом (рис. 5).
 Круговым процессом или циклом называется такой процесс, при котором система после ряда изменений возвращается в исходное состояние.
Круговым процессом или циклом называется такой процесс, при котором система после ряда изменений возвращается в исходное состояние.
Цикл изображается замкнутой кривой.
Циклы могут состоять как из обратимых, так и необратимых процессов. Цикл, состоящий из обратимых процессов, называется обратимым.
Тепловой двигатель - это система, совершающая многократно круговой процесс (цикл), при котором за счёт подведённого извне тепла совершается механическая работа. Для этого необходимо рабочему веществу в начале цикла сообщать некоторое количество теплоты Q1, а в конце цикла отнимать количество теплоты Q2.
Принцип действия теплового действия представлен на рис. 6.
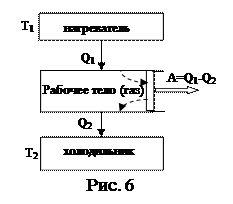 Рабочее тело приводится в контакт с нагревателем и получает от него количество теплоты Q1. При этом температура газа повышается, он расширяется и перемещает поршень, совершая работу А1. Затем рабочее тело приводится в контакт с холодильником, отдает ему Q2, газ охлаждается и сжимается, перемещая поршень в обратном направлении, что равносильно совершению газом отрицательной работы А2. После установления теплового равновесия с холодильником рабочее тело вновь приводится в контакт с нагревателем; цикл завершен.
Рабочее тело приводится в контакт с нагревателем и получает от него количество теплоты Q1. При этом температура газа повышается, он расширяется и перемещает поршень, совершая работу А1. Затем рабочее тело приводится в контакт с холодильником, отдает ему Q2, газ охлаждается и сжимается, перемещая поршень в обратном направлении, что равносильно совершению газом отрицательной работы А2. После установления теплового равновесия с холодильником рабочее тело вновь приводится в контакт с нагревателем; цикл завершен.
Количество получаемого за цикл тепла равно Q1, а отданного Q2. Их разность перешла в полезную работу:
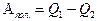 .
.
Разные тепловые машины, получив одинаковое количество теплоты, могут совершать разную полезную работу. Способность разных тепловых двигателей превращать тепловую энергию в работу характеризуется их коэффициентом полезного действия (КПД).
КПД теплового двигателя называется величина, равная отношению совершаемой за цикл полезной работы ко всему количеству теплоты, полученному от нагревателя:
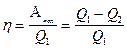 .
.
При рассмотрении работы тепловой машины не было оговорено, из каких процессов состоит её цикл: обратимых или необратимых.
В случае необратимых процессов только часть разности Q1-Q2 перейдет в полезную работу, остальная часть энергии рассеется в окружающем пространстве.
Следовательно, КПД тепловой машины, работающей на обратимых циклах, всегда больше КПД такой же машины, работающей на реальных (необратимых) циклах.
Для практических целей очень важно найти метод расчёта КПД идеальной тепловой машины, работающей на обратимом цикле. Тогда, основываясь на том, что hр<hид, можно будет оценить возможность реальной тепловой машины.
Как было сказано, все изопроцессы являются обратимыми и из них можно построить идеальный цикл. Поскольку каждый изопроцесс характеризуется соответствующей работой, которую с его помощью можно совершить, КПД различных идеальных циклов различны. В термодинамике показывается, что максимальным КПД обладает цикл, составленный из двух изотерм и двух адиабат. Этот цикл называется циклом Карно.
 Указный выше оптимальный цикл был рассмотрен французским инженером Сади Карно в 1824г. Выбор именно этих изопроцессов обусловлен тем, что при изотермическом процессе вся подведённая системе теплота идёт на совершение работы, а адиабатическое изменение температуры происходит без теплообмена с окружающей средой, т.е. без потерь.
Указный выше оптимальный цикл был рассмотрен французским инженером Сади Карно в 1824г. Выбор именно этих изопроцессов обусловлен тем, что при изотермическом процессе вся подведённая системе теплота идёт на совершение работы, а адиабатическое изменение температуры происходит без теплообмена с окружающей средой, т.е. без потерь.
Круговой процесс (цикл), состоящий из 2-х изотерм и 2-х адиабат, называется циклом Карно (рис.7).
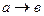 - изотермическое расширение.
- изотермическое расширение.
За счет получения газом количества теплоты Q1 газ изотермически расширяется, переходя из состояния " 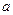 "в состояние "в". При этом всё
"в состояние "в". При этом всё  переходит в работу А1, поскольку DU= .
переходит в работу А1, поскольку DU= .
Q1=A1, 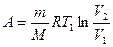 - работа, совершенная газом при изотермическом расширении.
- работа, совершенная газом при изотермическом расширении.
в®с - адиабатное расширение.
В состоянии "в "нагреватель убирают и газ, адиабатно расширяясь, переходит в состояние "с". При этом работа совершается газом за счет убыли его внутренней энергии, и температура газа понижается до Т2, T2<T1.
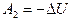 ,
, 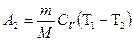 - работа, совершаемая газом при адиабатном расширении.
- работа, совершаемая газом при адиабатном расширении.
c®d - изотермическое сжатие.
В точке "с" газ вводят в контакт с холодильником. Газ, изотермически сжимаясь, переходит в состояние "d" и отдаёт холодильнику количество теплоты Q2.
Q2=A3, 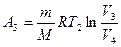 - работа над газом при изотермическом сжатии за счёт отдачи Q2 холодильнику.
- работа над газом при изотермическом сжатии за счёт отдачи Q2 холодильнику.
 - адиабатное сжатие.
- адиабатное сжатие.
В точке "d" холодильник убирают, и газ под действием внешних сил адиабатно сжимается, повышая при этом свою температуру до T1. Система возвращается в исходное состояние " 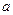 ", цикл завершён.
", цикл завершён.
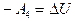 ,
, 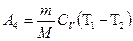 - работа над газом при адиабатном сжатии за счёт внешних сил.
- работа над газом при адиабатном сжатии за счёт внешних сил.
Т.к. для адиабатных процессов справедливы соотношения:

следовательно,
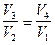 или
или 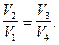
КПД тепловой машины, работающей с идеальным газом по циклу Карно, равен
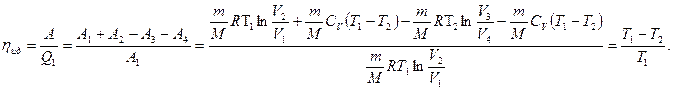 Таким образом,
Таким образом, 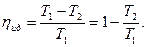
Анализ полученного выражения показывает, что чем больше разница между температурами нагревателя и холодильника, тем выше КПД. Это один из путей повышения КПД реальных тепловых двигателей.
11) 1)Существуют способы изменения внутренней энергии тела: совершение работы и теплопередача.
При совершении работы она меняется в двух случаях: при трении и при неупругой деформации. При совершении работы силой трения внутренняя энергия увеличивается за счёт уменьшения механической энергии, трущиеся тела нагреваются. В случае неупругого сжатия тела его внутренняя энергия увеличивается за счёт уменьшения механической энергии.
Теплопередача – процесс изменения внутренней энергии без совершения работы, при этом внутренняя энергия одного тела увеличивается за счёт уменьшения внутренней энергии другого тела. Переход энергии идет от тел с более высокой температурой к телам с более низкой температурой. Существует ее варианты: теплопроводность, конвекция и излучение.
~~~~~~~~~
Внутренняя энергия не постоянная величина. Она может изменяться. Если повысить температуру тела, то его внутренняя энергия увеличится (увеличится средняя скорость движения молекул). При понижении температуры, внутренняя энергия тела уменьшается.
Рассмотрим опыт.
Закрепим на подставке латунную трубку с тонкими стенками. Наполним трубку эфиром и закроем его пробкой. Обвяжем его веревкой и начнем интенсивно двигать веревкой в стороны. Через время эфир закипит, и сила пара вытолкнет пробку. Внутренняя энергия вещества (эфира) возросла: он изменил свою температуру, закипев. Увеличение внутренней энергии произошло за счет совершения работы.
Нагревание тел может происходить и при ударах, сгибании или разгибании, при деформации. Внутренняя энергия тела возрастает.
Внутреннюю энергию тела можно увеличить, совершая над телом работу. Если же работу выполняет само тело, его внутренняя энергия уменьшается.
Рассмотрим опыт.
В стеклянный сосуд, у которого толстые стенки и он закрыт пробкой, накачаем воздух через специально проделанное отверстие в ней.
Спустя некоторое время пробка вылетит из сосуда. В момент, когда пробка вылетает из сосуда, мы можем видеть образование тумана. Его образование обозначает, что воздух в сосуде стал холодным. Сжатый воздух, который находится в сосуде, при выталкивании пробки наружу совершает определенную работу. Данную работу он выполняет за счет своей внутренней энергии, которая при этом сокращается. Делать выводы об уменьшении внутренней энергии можно исходя из охлаждения воздуха в сосуде. Таким образом, внутреннюю энергию тела можно изменять путем совершения определенной работы.
Однако, внутреннюю энергию возможно изменить и иным способом, без совершения работы.
Рассмотрим пример.
Вода в чайнике, который стоит на плите закипает. Воздух, а также другие предметы в помещении нагреваются от радиатора центрального направления. В подобных случаях, внутренняя энергия увеличивается, т.к. увеличивается температура тел. Но работа при этом не совершается. Значит изменение внутренней энергии может произойти не из-за совершения определенной работы.
Рассмотрим пример.
В стакан с водой опустим металлическую спицу. Кинетическая энергия молекул горячей воды, больше кинетической энергии частиц холодного металла. Молекулы горячей воды будут передавать часть своей кинетической энергии частицам холодного металла. Таким образом, энергия молекул воды будет определенным образом уменьшаться, тем временем как энергия частиц металла будет повышаться. Температуры воды понизится, а температуры спицы не спеша, будет увеличиваться. В дальнейшем, разница между температурой спицы и воды исчезнет. За счет этого опыта мы увидели изменение внутренней энергии различных тел. Делаем вывод: внутренняя энергия различных тел изменяется за счет теплопередачи.
Процесс преобразования внутренней энергии без совершения определенной работы над телом или самим телом называется теплопередачей.
2) Количество теплоты — энергия, которую получает или теряет тело при теплопередаче. Количество теплоты является одной из основных термодинамических величин. Количество теплоты является функцией процесса, а не функцией состояния, то есть количество теплоты, полученное системой, зависит от способа, которым она была приведена в текущее состояние.
Внутренняя энергия тела может изменяться за счет работы внешних сил. Для характеристики изменения внутренней энергии при теплообмене вводится величина, называемаяколичеством теплоты и обозначаемая Q.
В международной системе единицей количества теплоты, также как работы и энергии, является джоуль: [Q] = [A] = [E] = 1 Дж.
На практике еще иногда применяется внесистемная единица количества теплоты – калория. 1 кал. = 4,2 Дж.
Количество теплоты, передаваемое от одного тела к другому, может идти на нагревание тела, плавление, парообразование, либо выделяться при противоположных процессах – остывании тела, кристаллизации, конденсации. Теплота выделяется при сгорании топлива.
Между массой вещества и количеством теплоты, необходимым для его нагревания, существует прямая пропорциональная зависимость.
o Количество теплоты, необходимое для нагревания тела или выделяющееся при его охлаждении, прямо пропорционально массе тела и изменению его температуры:
Q = cmΔT,
где с - удельная теплоемкость [Дж/кг·К], m - масса тела [кг], ΔT - изменение температуры [К]
o Количество теплоты, необходимое для превращения жидкости в пар или выделяющееся при его конденсации, прямо пропорционально массе жидкости:
Q = Lm,
где L - удельная теплота парообразования [Дж/кг], m - масса тела [кг]
o Количество теплоты, необходимое для плавления тела или выделяющееся при его кристаллизации, прямо пропорционально массе этого тела:
Q = λm,
где λ (лямбда) - удельная теплота плавления [Дж/кг], m - масса тела [кг]
o Количество теплоты, выделяющееся при сгорании топлива, прямо пропорционально его массе:
Q = qm,
где q - удельная теплота сгорания [Дж/кг], m - масса тела [кг]
Удельная теплоемкость вещества показывает, чему равно количество теплоты, необходимое для нагревания или выделяющееся при охлаждении 1 кг вещества на 1 К.
Удельные теплоты парообразования, плавления, сгорания показывают, какое количество теплоты требуется для парообразования, плавления или выделяется при конденсации, кристаллизации, сгорании 1 кг вещества.
определить количество теплоты формулой:
Q=cm(t_2-t_1 ) ,
где Q – количество теплоты,
m – масса тела,
(t_2-t_1 ) – разность между начальной и конечной температурами тела,
c – удельная теплоемкость вещества, находится из соответствующих таблиц.
По этой формуле можно произвести расчет количества теплоты, которое необходимо, чтобы нагреть любое тело или которое это тело выделит при остывании.
3) Уде́льная теплоёмкость — отношение теплоёмкости к массе, теплоёмкость единичной массы вещества (разная для различных веществ); физическая величина, численно равная количеству теплоты, которое необходимо передать единичной массе данного вещества для того, чтобы его температура изменилась на единицу.[1]
В Международной системе единиц (СИ) удельная теплоёмкость измеряется в джоулях на килограмм на кельвин, Дж/(кг·К)[2]. Иногда используются и внесистемные единицы: калория/(кг·К) и т.д.
Удельная теплоёмкость обычно обозначается буквами c или С, часто с индексами.
На значение удельной теплоёмкости влияет температура вещества и другие термодинамические параметры. К примеру, измерение удельной теплоёмкости воды даст разные результаты при 20 °C и 60 °C. Кроме того, удельная теплоёмкость зависит от того, каким образом позволено изменяться термодинамическим параметрам вещества (давлению, объёму и т. д.); например, удельная теплоёмкость при постоянном давлении (CP) и при постоянном объёме (CV), вообще говоря, различны.
Формула расчёта удельной теплоёмкости: 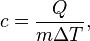 где c — удельная теплоёмкость, Q — количество теплоты, полученное веществом при нагреве (или выделившееся при охлаждении), m — масса нагреваемого (охлаждающегося) вещества, ΔT — разность конечной и начальной температур вещества. Удельная теплоёмкость может зависеть (и в принципе, строго говоря, всегда - более или менее сильно - зависит) от температуры, поэтому более корректной является следующая формула с малыми (формально бесконечно малыми)
где c — удельная теплоёмкость, Q — количество теплоты, полученное веществом при нагреве (или выделившееся при охлаждении), m — масса нагреваемого (охлаждающегося) вещества, ΔT — разность конечной и начальной температур вещества. Удельная теплоёмкость может зависеть (и в принципе, строго говоря, всегда - более или менее сильно - зависит) от температуры, поэтому более корректной является следующая формула с малыми (формально бесконечно малыми) 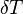 и
и 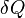 :
:

4) Уравнение теплового баланса
Q=m*c*(t1-t2)
m - масса
c - теплоемкость
t - температура
Q –тепло
12) Количество теплоты. Удельная теплоемкость вещества. Уравнение теплового баланса при теплообмене.
Если тела различной температуры привести в соприкосновение, горячее начнет остывать, а холодное — нагреваться, т.е. будет идти теплообмен. Он закончится, когда температура обоих тел сравняется. Наступит, как говорят физики, тепловое равновесие.
Второе начало термодинамики: тепло всегда переходит от горячего тела к холодному (если на тела не оказывается специального внешнего воздействия).
При этом оба тела обмениваются не температурой, а количеством теплоты(энергией). Температура же характеризует внутреннее состояние каждого тела и направление теплообмена. В процессе теплообена металла и воды равной массы температура металлического тела меняется в несколько раз больше, чем температура воды.
Вся термодинамика строится на предпосылке, что количество теплоты, отданное одним телом, равно количеству теплоты, полученному другим (при условии, что два тела изолированы от прочих). Значит, металл и вода, обладая одинаковой массой, имеют совершенно различную теплоемкость, т.е. при нагревании (остывании) на 1° получают различное количество теплоты. Таким образом, теплоемкость характеризует способность тела получать или же отдавать определенное количество теплоты в процессе нагревания или же остывания на 1°.
Количество теплоты — это отдаваемая или же получаемая телом энергия при теплообмене с другими телами. При передаче тепла уменьшаетсявнутренняя энергия тела-нагревателя, а внутренняя энергия нагреваемого тела растет. Согласно закону сохранения энергии, при теплообмене уменьшение внутренней энергии одного тела равно отданному им количеству теплоты, которое в свою очередь равно увеличению внутренней энергии другого тела (или всех окружающих тел, если система не изолирована).
Уравнение теплового баланса: тепло отданное = теплу полученному.
Количество теплоты обозначается буквой Q и измеряется в калориях (кал). 1 калория — это количество тепла, необходимое для того, чтобы нагреть воду массой 1 грамм на 1 градус.
Удельной теплоемкостью вещества называется количество тепла, необходимое для нагревания 1 грамма вещества на 1 градус.
Количество тепла=удельная теплоемкость·масса·изменение температуры
Q = cm(t-t0)
Количество теплоты, выделяемое при полном сгорании единицы топлива, называется его теплотворностью, или теплотой сгорания и измеряется в кДж/кг или кДж/м3. Теплота сгорания – основной параметр органического топлива, характеризующий его энергетическую ценность, и для расчетов определяется по табл.
Удельная теплота сгорания твердого и жидкого топлива определяется сжиганием 1 г топлива в калориметрической бомбе, заполненной кислородом, которая помещается в сосуд (калориметр) с водой, а приращение температуры воды измеряется метастатическим термометром. Удельная теплота сгорания газообразного топлива определяется в калориметре путем сжигания исследуемого газа в воздушной среде. Расход газа измеряется счетчиком, а выделившаяся при этом теплота передается потоку проточной воды, расход которой определяется взвешиванием, а приращение температуры – термометрами.
13)
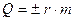 ,(8.7)
,(8.7)
где r – удельная теплота парообразования; m – масса вещества. Знак плюс в формуле при парообразовании (жидкость получает теплоту парообразования), знак минус – при конденсации (пар отдает теплоту конденсации).
Удельная теплота парообразования – величина, численно равная количеству теплоты, необходимому для превращения при постоянной температуре жидкости массой 1 кг в пар. называют удельной теплотой парообразования. Размерность величины – джоуль на килограмм (Дж/кг).
Очень велика удельная теплота парообразования воды: r = 2,26×106 Дж/кг при температуре 100°С. У других жидкостей, например у спирта, эфира, ртути, керосина, удельная теплота парообразования меньше в 3—10 раз, чем у воды.
Для превращения жидкости в пар в процессе кипения необходима передача ей определенного количества теплоты. Температура жидкости при кипении не меняется. Превращение жидкости в пар при постоянной температуре не ведет к увеличению кинетической энергии молекул, но сопровождается увеличением потенциальной энергии их взаимодействия. Ведь среднее расстояние между молекулами газа много больше, чем между молекулами жидкости.
14)  Переход кристаллического тела в жидкое состояние происходит при определенной для каждого вещества температуре и требует затраты некоторого количества тепла, называемого теплотой плавления.
Переход кристаллического тела в жидкое состояние происходит при определенной для каждого вещества температуре и требует затраты некоторого количества тепла, называемого теплотой плавления.
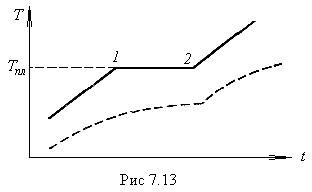
Если веществу, первоначально находившемуся в кристаллическом состоянии, сообщать каждую секунду одно и то же количество тепла, то температура тела со временем будут меняться (рис.7.13). Температура растет до значения Тпл температуры плавления (точка 1 на рис. 7.13), при дальнейшем подводе тепла температура перестает изменяться. Одновременно начинается процесс плавления твердого тела, в ходе которого все новые и новые порции вещества превращаются в жидкость. После того как процесс плавления будет закончен и все вещество полностью перейдет в жидкое состояние (точка 2 на рис. 7.13), температура снова начнет повышаться.
Кривая нагревания аморфного тела выглядит иначе (пунктирная кривая на рис. 7.13). При равномерном подводе тепла температура аморфного тела непрерывно растет, для аморфных тел нет определенной температуры перехода в жидкое состояние. Этот переход совершается непрерывно, а не скачком. Можно лишь указать интервал температур, в пределах которого происходит размягчение тела. Это объясняется тем, что жидкости и аморфные тела отличаются лишь степенью подвижности молекул, — аморфные тела, как уже отмечалось, представляют собой сильно переохлажденные жидкости.
Температура плавления зависит от давления. Таким образом, переход из кристаллического в жидкое состояние происходит при вполне определенных условиях, характеризуемых значениями давления и температуры. Совокупности этих значений соответствует кривая на диаграмме (р, Т), которую принято называть кривой плавления. Кривая плавления идет очень круто. Для того, например, чтобы изменить на 1 К температуру таяния льда, необходимо изменить давление на 132 атм. Точки кривой плавления определяют условия, при которых кристаллическая и жидкая фазы могут находиться в равновесии друг с другом. Такое равновесие возможно при любом соотношении между массами жидкости и 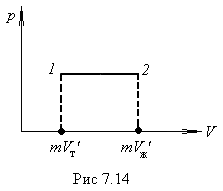 кристаллов, т. е. при значениях объема системы, заключенных в пределах от
кристаллов, т. е. при значениях объема системы, заключенных в пределах от 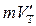 , до
, до 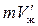 , где т — масса системы, a
, где т — масса системы, a 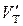 и
и 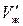 — удельные объемы твердой и жидкой фаз. Поэтому каждой точке кривой плавления соответствует на диаграмме (р, V) отрезок горизонтальной прямой (рис.7.14). Поскольку вещество в состояниях, изображаемых точками этого отрезка, имеет одну и ту же температуру, прямая 1—2на рис.7.14 представляет собой участок изотермы, соответствующий двухфазным состояниям вещества.
— удельные объемы твердой и жидкой фаз. Поэтому каждой точке кривой плавления соответствует на диаграмме (р, V) отрезок горизонтальной прямой (рис.7.14). Поскольку вещество в состояниях, изображаемых точками этого отрезка, имеет одну и ту же температуру, прямая 1—2на рис.7.14 представляет собой участок изотермы, соответствующий двухфазным состояниям вещества.
Обратный плавлению процесс кристаллизации протекает следующим образом. При охлаждении жидкости до температуры, при которой твердая и жидкая фазы могут находиться в равновесии при данном давлении (т. е. до той же температуры, при которой происходило плавление), начинается одновременный рост кристалликов вокруг так называемых зародышей или центров кристаллизации. Разрастаясь все более, отдельные кристаллики в конце концов смыкаются друг с другом, образуя поликристаллическое твердое тело.

|
Центрами кристаллизации могут служить взвешенные в жидкости твердые частицы. Тщательно очищенную от таких частиц жидкость можно охладить ниже температуры кристаллизации без того, чтобы началось образование кристалликов. Состояние такой переохлажденной жидкости является метастабильным. Обычно достаточно попасть в такую жидкость пылинке, для того чтобы она распалась на жидкость и кристаллы, находящиеся при равновесной температуре. Однако в некоторых случаях при больших переохлаждениях подвижность молекул жидкости оказывается столь незначительной, что метастабильное состояние может сохраняться очень долго. Жидкость в таких случаях обладает весьма малой текучестью и представляет собой аморфное твердое тело.
Процесс кристаллизации сопровождается выделением такого же количества тепла, которое поглощается при плавлении.