Хімічні властивості
Будучи полігідроксикарбонільними сполуками, моносахариди виявляють хімічні властивості карбонільних сполук, багатоатомних спиртів, а також циклічних напівацеталів.
Хімічні перетворення в ряду моносахаридів можна умовно розділити на дві групи: реакції за участю відкритих форм моносахаридів і реакції за участю циклічних форм.
А. Реакції за участю відкритих форм
Відновлення.При відновленні моносахаридів воднем у присутності каталізатора (нікель, паладій), боргідридом натрію або амальгамою натрію в розбавленій сірчаній кислоті утворюються багатоатомні спирти. З D-глюкози при цьому утворюється спирт – D-сорбіт, з D-манози — D-маніт, з D-ксилози – D-ксиліт і т. д.
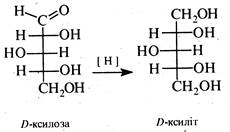
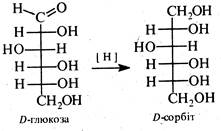
D-Ксиліт і D-сорбіт кристалічні речовини, солодкі на смак, застосовуються при цукровому діабеті як замінники цукру. D-Сорбіт є проміжним продуктом у промисловому синтезі аскорбінової кислоти з D-глюкози. При відновленні D-фруктози утворюється еквімолекулярна суміш D-сорбіту та D-маніту, що пов'язано з перетворенням карбонільної групи при С2 в асиметричний центр.
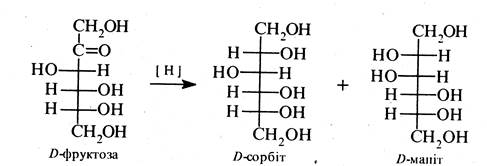
Окиснення.Моносахариди легко окиснюються, але, в залежності від природи окисника та умов окиснення, утворюються різні продукти. У кислому та нейтральному середовищі окиснення проходить без руйнування вуглецевого ланцюга молекули, в лужному середовищі, як правило, воно супроводжується розщепленням вуглецевого скелета.
Окиснення в кислому і нейтральному середовищі.При використанні слабких окисників, наприклад, бромної води або розбавленої азотної кислоти, альдози окиснюються з утворенням одноосновних поліоксикислот, які дістали загальну назву альдонові кислоти. D-Глюкоза за цих умов дає D-глюконову кислоту, D-галактоза D-галактонову кислоту і т.д. У кислих розчинах альдонові кислоти, що утворилися, відщеплюють воду і перетворюються на відповідні γ-лактони.

 Кальцієва сіль D-глюконової кислоти – глюконат кальцію – застосовується у медицині при алергічних захворюваннях, шлункових, кишкових, легеневих, маткових і носових кровотечах, різних захворюваннях шкіри, токсичних ураженнях печінки та ін.
Кальцієва сіль D-глюконової кислоти – глюконат кальцію – застосовується у медицині при алергічних захворюваннях, шлункових, кишкових, легеневих, маткових і носових кровотечах, різних захворюваннях шкіри, токсичних ураженнях печінки та ін.
Кетози бромною водою не окиснюються. Сильні окисники, наприклад, концентрована HNО3, окиснюють у молекулі альдоз альдегідну і первинну спиртову групи з утворенням дикарбонових оксикислот, Які дістали загальну назву альдарові, або цукрові, кислоти. Так, D-глюкоза окиснюється в D-глюкарову кислоту, D-маноза у D-манарову, D-галактоза в D-галактарову (слизову) кислоту, наприклад:
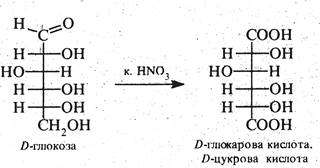
При окисненні кетоз за аналогічних умов відбувається розрив вуглецевого ланцюга за місцем карбонільної групи з утворенням дикарбонової кислоти.

При селективному окисненні у молекулі альдози первинної спиртової групи без участі вельми схильної до окиснення альдегідної групи утворюються уронові кислоти. Окисненню в таких випадках піддають моносахариди з захищеною альдегідною групою, наприклад, глікозиди (див. нижче):
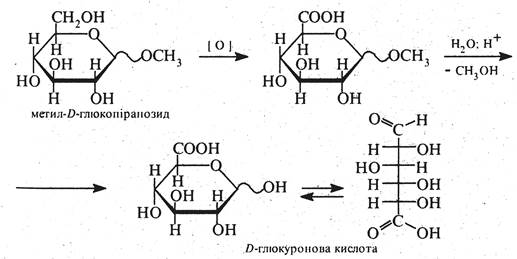
Уронові кислоти широко розповсюджені в природі. Вони входять до складу багатьох полісахаридів. Поряд з D-глюкуроновою кислотою широко представлені D-галактуронова, D-мануронова і L-ідуронова кислоти.
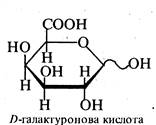
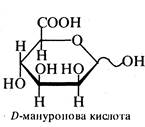

D-Галактуронова кислота є компонентом пектину фруктів, D-мануронова кислота міститься в різних морських водоростях, D-глюкуронова та L-ідуронова кислоти входять до складу гепарину та інших полісахаридів. Уронові кислоти беруть участь у процесі виведення з організму токсичних речовин.
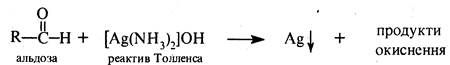
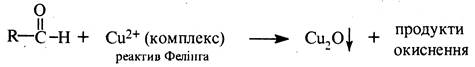
Окиснення у лужному середовищі Подібно до альдегідів, моносахариди окиснюються аміачним розчином оксиду срібла (реактив Толленса) і гідроксидом міді (II) у лужному розчині, або ж реактивом Фелінга (див. кн. 2, с, 431). В ці реакції вступають як альдози, так і кетози, тому що у лужному середовищі кетози ізомеризуються в альдози (див. нижче). З реактивом Толленса здійснюється реакція «срібного дзеркала». З реактивом Фелінга та гідроксидом міді (II) у лужному розчині утворюється оксид міді (II) червоно-оранжевого кольору. Моносахариди при окисненні у лужному середовищі розщеплюються до суміші продуктів окиснення. Ці реакції є якісними на альдози і кетози.
Перетворення моносахаридів під дією лугів (епімеризація).В розбавлених розчинах лугів при кімнатній температурі моносахариди піддаються ізомеризації з утворенням рівноважної суміші моноз, які розрізняються конфігурацією вуглецевих атомів С1 і С2. Так, D-глюкоза, витримана у розчині гідроксиду натрію (8•10-3) при 35 °С протягом 4 діб, перетворюється на суміш, яка складається з D-фруктози (~28%), D-манози (~3%) і D-глюкози (~69%). Аналогічна ізомеризація спостерігається у кетоз, наприклад, фруктози. Ізомерні перетворення моносахаридів під дією лугів називають епімеризацією,оскільки вони приводять до утворення епімерів, наприклад, глюкози і манози.
Взаємоперетворення у слаболужному середовищі проходить через ендіольну форму,котра утворюється в результаті міграції до карбонільної групи рухливого водню при α-атомі вуглецю.
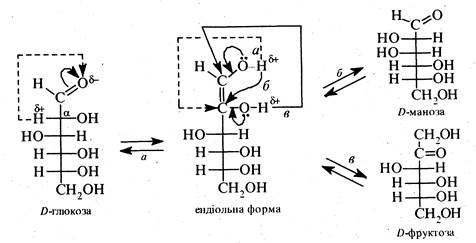
При зворотному перетворенні ендіольної форми на карбонільну утворюється суміш трьох моносахаридів.
Утворення озазонів. Принагріванні моносахаридів з фенілгідразином у молярному співвідношенні 1:3 утворюються біс-фенілгідразони, що дістали назву озазони.
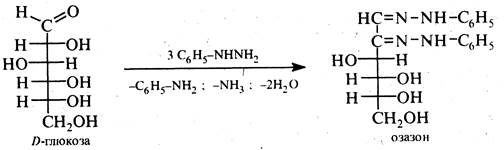
Механізм реакції. Утворення озазонів іде за декілька стадій. Спочатку молекула моносахариду реагує з однією молекулою фенілгідразину, утворюючи фенілгідразон, котрий в результаті внутрішньо-молекулярної окисно-відновної реакції піддається перегрупуванню в моноімін 1,2-дикарбонільної сполуки. Потім моноімін при взаємодії з двома молекулами фенілгідразину перетворюється на озазон.
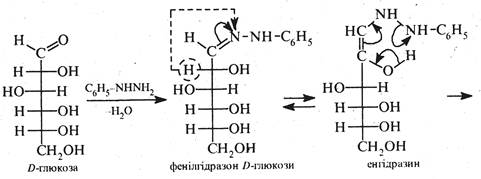
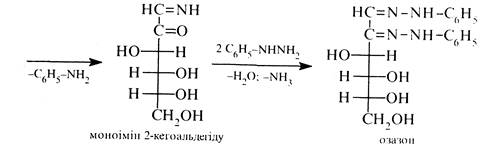
Озазони являють собою кристалічні речовини жовтого кольору, не розчинні у воді. D-Глюкоза, D-маноза і D-фруктоза дають один і той самий озазон. Під дією хлороводневої кислоти або при нагріванні з бензальдегідом озазони легко відщеплюють дві молекули фенілгідразину, утворюючи відповідні озони (кетоноальдепди). При відновленні озонів амальгамою натрію у слабокислих розчинах утворюються кетози.

Таким чином, реакція моносахаридів з фенілгідразином дозволяє здійснити перехід від альдоз через озазони і озони до кетоз.
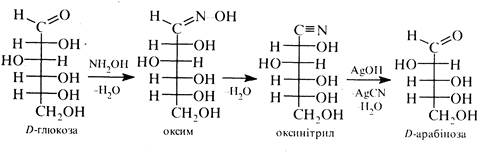
Взаємодія з гідроксилхтіном.Альдози легко вступають в реакцію з гідроксиламіном, утворюючи оксими. У присутності водовіднімаючих засобів оксими можуть бути перетворені на відповідні оксинітрили, котрі під дією іонів срібла відщеплюють HCN і утворюють оксіальдегіди, що містять на один атом вуглецю менше, ніж у вихідної альдози. За допомогою цих реакцій можна здійснити перехід від вищих альдоз до нижчих.
Виутрішньомолекулярна дегідратація. При нагріванні з мінеральними кислотами (НСl, H2SО4) пентози піддаються внутрішньомолекулярній дегідратації з утворенням фурфуролу, а гексози 5-гідрокси-метилфурфуролу:

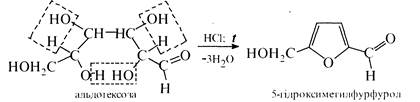
Ця реакція дозволяє відрізнити гексози від пентоз. Фурфурол дає червоне забарвлення з аніліном у присутності хлороводневої кислоти (якісна реакція на пентози).
5-Пдроксиметилфурфурол утворює червоне забарвлення з резорцином (реакція Селіванова на фруктозу).
Б. Реакції за участю циклічних форм
Утворення глікозидів. Моносахариди, будучи циклічними напівацеталями, реагують у присутності кислотного каталізатора зі спиртами та фенолами. Реакція проходить за участю напівацетальної гідроксильної групи і приводить до утворення циклічних ацеталів, які дістали назву глікозиди. Незалежно від вихідної форми моносахариду у процесі реакції утворюється суміш α- та β-глікозидів.
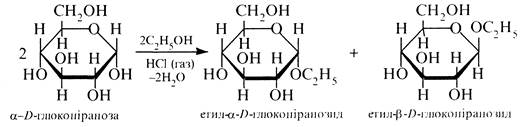
Назви глікозидів утворюють з назв моносіхаридів, замінюючи суфікс -оза на -озид. Наприклад: фруктозид, галактозид, рибозид, глюкозид тощо. В залежності від розміру циклу (піранозній, фуранозний) глікозиди поділяють на піранозиди і фуранозиди. α- та β-Аномерам моносахаридів відповідають α- та β-глікозиди. Невуглеводну частину молекули глікозиду називають агліконом. Хімічний зв'язок між аномерним атомом вуглецю моносахариду і агліконом у глікозиді називається глікозидним.
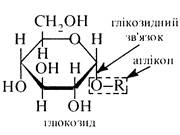 В зв'язку з тим. що у молекулах глікозидів відсутній вільний напівацетальний гідроксил, вони, на відміну від моносахаридів, не здатні до таутомерії у водних розчинах, не мутаротують і не виявляють відновних властивостей.
В зв'язку з тим. що у молекулах глікозидів відсутній вільний напівацетальний гідроксил, вони, на відміну від моносахаридів, не здатні до таутомерії у водних розчинах, не мутаротують і не виявляють відновних властивостей.
Глікозиди як ацеталі легко гідролізуються у кислому середовищі, але виявляють стійкість до гідролізу у слаболужному середовищі. У процесі гідролізу утворюється суміш α-та β-аномерів відповідного моносахариду.

Глікозиди вельми широко розповсюджені в природі. У переважній більшості вони є β-глікозидами. В якості агліконів у природних глікозидах часто виступають гідроксилвмісні сполуки феноли, стероїди (див. розд. 3.7.3 і 8.3.2, В) і самі моносахариди. Зв'язок аглікону з аномерним атомом вуглецю в цих сполуках здійснюється через атом кисню, тому такі глікозиди називають О-глікозидами.Прикладом О-глікозидів є глікозид арбутин, який міститься у листі мучниці звичайної (Arctostaphylos u va-ursi).



Крім О-глікозидів, відомі N-глікозидиі S-глікозиди.
ВN-глікозидах агліконами є залишки аліфатичних, ароматичних, гетероциклічних амінів та інші NH-вмісні органічні сполуки. Зв'язок аглікону з моносахаридом у N-глікозидах здійснюється через атом азоту. До N-глікозидів належать продукти розщеплення нуклеїнових кислот і нуклеопротеїдів (нуклеотиди, нуклеозиди), АТФ, які відіграють важливу роль в обміні речовин, а також деякі антибіотики та ін.
Прикладом S-глікозидів є глікозид синігрин, який міститься у насінні сарептської гірчиці.
В S-глікозидах агліконами є тіоли, а зв'язок аглікону з моносахаридом здійснюється через атом сірки.
Алкілування. При взаємодії моносахаридів з галогеналканами або диметилсульфатом (СН3)2SО4 в реакцію вступають усі гідроксильні групи, включаючи напівацетальний гідроксил. В результаті реакції утворюються глікозиди, алкіловані по всіх гідроксильних групах. Такі сполуки у кислому середовищі гідролізуються тільки за глікозидним зв'язком. Прості ефіри, що утворилися по решті гідроксильних груп, гідролізу не піддаються.
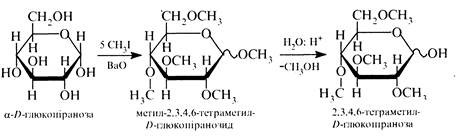
Ацилювання. При взаємодії моносахаридів з ангідридами карбонових кислот легко утворюються складні ефіри по всіх гідроксильних групах. Так, при дії на глюкозу оцтовим ангідридом утворюється пентаацетилглюкоза.

В кислому та лужному середовищі складні ефіри моносахаридів гідролізуються.
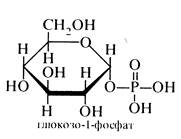
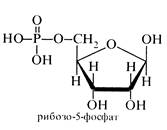
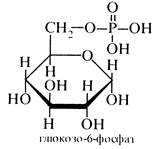
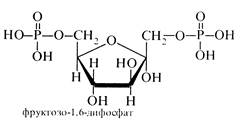
Серед складних ефірів моносахаридів важливе значення мають ефіри фосфорної кислоти. Вони містяться в усіх рослинних і тваринних організмах і відіграють велику роль в обміні речовин. Фосфати рибози і дезоксирибози входять до складу нуклеїнових кислот (див. розд. 7.1), фосфати D-глюкози і D-фруктози беруть участь в обміні вуглеводів, пірофосфорні ефіри моносахаридів беруть участь у синтезі пуринових і піримідинових нуклеотидів. Фотосинтез, бродіння та інші біологічні процеси також здійснюються за участю фосфатів моносахаридів.
Нижче наведено деякі фосфати моносахаридів, які виконують важливу роль в обміні речовин.