Задача 1.


Задача 2.
 |
m(р-ра) = 200 г
W = 10%
M(СаС12) = 111 г/моль
M(СаС12 · 6Н2О) = 219 г/моль

m(СаС12 · 6Н2О) - ?
m(Н2О) - ?
Решение:
m(СаС12) = 200 г · 0,10 = 20 г
в 219 г (СаС12 · 6Н2О) – 111 г СаС12
в Х г ----------------------- 20 г СаС12
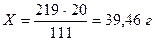
Ответ: для приготовления 10% раствора СаС12 необходимо 39, 5 г (СаС12 · 6Н2О); m(Н2О) = 200 г – 39,5 г = 160,5 г или 160, 5 мл.
Задача 3.
m(КОН) = 200 г · 0,10 = 20 г.
m(Н2О) = 200 – 20 г = 180 г или

Задача 4.
m(р-ра) = V · ρ = 3000 мл · 1,115 г/мл = 3345 г
m(КОН) = 3345 г · 0,10 = 334,5 г
m(Н2О) = 3345 – 334,5 = 3010,5 г или
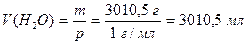
Задача 5.
1) m(р-ра) = V · ρ = 1000 мл · 1,074 г/мл = 1074 г
2) m(НС1) в этом растворе: 1074 ∙ 0,10 = 107,4 г
3) m(р-ра 38% НС1) = 100 г р-ра – 38 г кислоты
m(р-раНС1) – 107,4 г кислоты
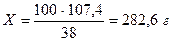
4) 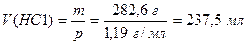
5) V(Н2О) = 1000 мл – 237,5 мл = 762,5 мл
Задача 6.
1) 1 + 7 = 8 частей; 1000 мл : 8 = 125 мл. Для приготовления раствора Н2SО4 необходимо взять 125 мл кислоты и 875 мл Н2О. Кислоту осторожно вливать в колбу с водой по стенке.