ПРОЦЕССЫ ИДЕАЛЬНОГО ГАЗА.
4.1 ИЗОХОРНЫЙ ПРОЦЕСС: V=const.

Из уравнения Клайперона для двух произвольных состояний изохорного процесса:
 ;
; 
 (4.1)
(4.1)
При постоянном объеме V=const давления одинаковых масс одного и того же газа относятся как абсолютные температуры (закон Шарля).
Δ 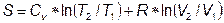 т.к.
т.к.  следовательно:
следовательно:
Δ  ; Δ
; Δ  (4.2)
(4.2)
Iый закон термодинамики для изохорного процесса:
dq=du, так как P*dV=0
q=  ; du=
; du=  (4.3)
(4.3)
величина внутренней энергии газа зависит только от ΔT.
ИЗОБАРНЫЙ ПРОЦЕСС: Р=const.
Из уравнения Клайперона для двух произвольных состояний изобарного процесса:
 ;
; 
 (4.5)
(4.5)
При постоянном давлении Р=const объемы одинаковых масс одного и того же газа относятся как абсолютные температуры (закон Гей-Люссака).

Для энтропии:





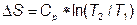 ;
;  (4.6)
(4.6)


 ;
; 

 (4.7)
(4.7)
Iый закон термодинамики для изобарного процесса:
 =
= 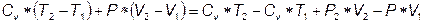

так как 
 (4.8)
(4.8) 
4.2. ИЗОТЕРМИЧЕСКИЙ ПРОЦЕСС: T=const.
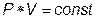 - изотерма в координатах P, V представляет собой гиперболу (закон Бойля- Мариотта).
- изотерма в координатах P, V представляет собой гиперболу (закон Бойля- Мариотта).
Из уравнения Клайперона для двух произвольных состояний изотермического процесса:
 ;
; 
 ;
;  (4.9)
(4.9)

Так как внутренняя энергия идеального газа зависит только от температуры, то в изотермическом процессе внутренняя энергия не изменяется.
 ; du=0 и следовательно
; du=0 и следовательно
dq=dL; q=L (4.10)
Теплоту и работу изотермического процесса, совершенного идеальным газом, рассчитывают по формуле, полученной методами высшей математики:

 (4.11)
(4.11)
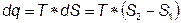 (4.12)
(4.12)
4.3.АДИАБАТНЫЙ ПРОЦЕСС: 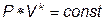 ; q=0.
; q=0.

 ;
;  ; S=const
; S=const
| |

Процесс без подвода и отвода теплоты к рабочему телу q=0; P=varia; V=varia; T=varia .
 уравнение адиабаты (Пуассона).
уравнение адиабаты (Пуассона).
Аналитическое выражение Iго закона термодинамики для адиабатного процесса:
 ;
;  ;
; 

Отсюда видно, что работа выполняется в результате изменения внутренней энергии.
 ;
;  (**)
(**)
Используя уравнение  и поделив на Т (**) запишем:
и поделив на Т (**) запишем:
 (***)
(***)
Зная, что  получим, поделив его и уравнение (***) на Сv:
получим, поделив его и уравнение (***) на Сv:


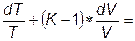 0
0
Проинтегрируем это уравнение, считая K=const:
 , зависимость между T и V; (4.13)
, зависимость между T и V; (4.13)
 , зависимость между Р и V; (4.14)
, зависимость между Р и V; (4.14)
 , зависимость между Р и
, зависимость между Р и  ; (4.15)
; (4.15)
 , зависимость между Р и Т (4.16)
, зависимость между Р и Т (4.16)
Работа 1 кг газа определяется по следующим формулам:
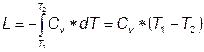 (4.17)
(4.17)
либо
 ;
; 
 ;
;

 (4.18)
(4.18)
 (4.19)
(4.19)
 ;
;  (4.20)
(4.20)
 ;
; 
Так как в адиабатном процессе dq=0, то С=  .
.