Уравнение Клаузиуса–Клапейрона для процесса испарения
Давление пара легколетучей жидкости
План коллоквиума
Фазовые равновесия в однокомпонентной системе. Уравнение Клаузиуса – Клапейрона. Процессы плавления, испарения и возгонки. Интегрирование уравнения Клаузиуса – Клапейрона. Определение теплоты испарения. Диаграмма состояния вещества.
Цель работы
Ознакомиться с одним из методов определения давления насыщенного пара (упругости пара) в зависимости от температуры в равновесной системе «жидкость – пар». Определить теплоту испарения этилового спирта.
Общие положения
Насыщенным называется пар, находящийся в равновесии с жидкостью. Давление насыщенного пара зависит от природы веществ и температуры. Равновесная однокомпонентная система, состоящая из 2-х фаз, обладает одной степенью свободы, значит, давление насыщенного пара жидкости зависит только от температуры. Применяя второй закон термодинамики, можно получить уравнение, связывающее давление Р и температуру Т. Связь между давлением насыщенного пара и температурой устанавливает уравнение Клаузиуса – Клапейрона.
Уравнение Клаузиуса–Клапейрона для процесса испарения
Если жидкость А находится в равновесии с паром и 1 моль вещества переходит в условиях равновесия из жидкой фазы в парообразную:
Аж ↔ Апар,
уравнение Клаузиуса – Клапейрона принимает вид:
 (1)
(1)
где DНисп – молярная теплота испарения вещества А,
Vж – объем 1 моля жидкого вещества,
Vпар – объем 1 моля насыщенного пара,
Р – давление насыщенного пара над жидким веществом,
Т – температура, при которой находится система.
Уравнение (1) дает в дифференциальной форме зависимость давления насыщенного пара над жидким веществом А от температуры.
Для получения зависимости давления насыщенного пара от температуры в явной форме необходимо уравнение (1) проинтегрировать.
В области невысоких давлений пара (не выше 1 – 2 атм) и в небольшом температурном интервале (~1000) можно считать, что теплота испарения (ΔНисп) не зависит от температуры, а насыщенный пар ведет себя как идеальный газ. Эти допущения позволяют легко получить интегральное уравнение Клаузиуса – Клапейрона (2):
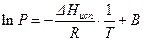 (2)
(2)
где В – константа интегрирования.
Из уравнения (2) следует, что зависимость lnР=f(1/T) является линейной функцией (у = А∙х + В), угловой коэффициент которой (А) определяется теплотой испарения жидкости:
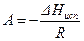 (3)
(3)
Уравнение (2) можно рассматривать и как зависимость температуры кипения жидкости от внешнего давления, поскольку условием кипения является равенство упругости пара жидкости внешнему давлению. На этом основана экспериментальная методика работы.