Задания для самостоятельного решения
1. Определите молярную и нормальную концентрации 20%-ного раствора хлорида кальция (  =1,178 г/мл).
=1,178 г/мл).
2. Определите молярную и нормальную концентрации 25%-ого раствора NH4CI (  =1,02 г/мл).
=1,02 г/мл).
3. Определите нормальную, молярную и моляльную концентрации раствора 15%-ного раствора H2SО4 (  = 1,105 г/мл).
= 1,105 г/мл).
4. Определите нормальную и моляльную концентрации 20,8%-ного раствора НNО3 (  = 1,12 г/мл). Сколько граммов кислоты содержится в 3 л этого раствора?
= 1,12 г/мл). Сколько граммов кислоты содержится в 3 л этого раствора?
5. Определите молярную, нормальную и моляльную концентрации 16%-ного раствора хлорида алюминия (  = 1,149 г/мл).
= 1,149 г/мл).
6. В 1 кг воды растворено 666 г КОН (  = 1,395 г/мл). Определите процентную, молярную и моляльную концентрации раствора КОН.
= 1,395 г/мл). Определите процентную, молярную и моляльную концентрации раствора КОН.
7. Определите массовую долю гидроксида натрия в 9,28 н растворе NaOH (  = 1,310 г/мл).
= 1,310 г/мл).
8. Вычислите нормальную и моляльную концентрации 20%-ого раствора HNO3 (  = 1,12г/мл). Сколько граммов кислоты содержится в 5 л этого раствора?
= 1,12г/мл). Сколько граммов кислоты содержится в 5 л этого раствора?
9. Определите нормальную и молярную концентрации 20%-ого раствора СаСI2 ( 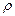 = 1,178г/мл).
= 1,178г/мл).
10. Определите нормальную и моляльную концентрации 40%-ного раствора NaOH (  = 1,43г/мл).
= 1,43г/мл).
11. Определите молярную концентрацию 36,5%-ного раствора НСl (  = 1,18 г/мл).
= 1,18 г/мл).
12. Определите нормальную и молярную концентрации 40%-ного раствора HNО3 (  = 1,25 г/мл).
= 1,25 г/мл).
13. Определите процентную концентрацию азотной кислоты в растворе, в 1 л которого содержится 224 г HNО3 (  = 1,12 г/мл).
= 1,12 г/мл).
14. Определите нормальность концентрированной соляной кислоты, содержащей 36,5% НСl (  = 1,18 г/мл)
= 1,18 г/мл)
15. Определите массу азотнокислого натрия NaNО3, необходимую для приготовления 300 мл 0,25 М раствора.
16. Какую массу азотнокислого натрия NаNО3 нужно растворить в 400 г воды, чтобы приготовить 15%-ный раствор?
17. Сколько граммов карбоната натрия Na2CО3 содержится в 500 мл 0,35 и. раствора?
18. Какой объём 20,01 %-ного раствора НСl (  = 1,100 г/мл) требуется для приготовления 1 л 10,17%-ного раствора (
= 1,100 г/мл) требуется для приготовления 1 л 10,17%-ного раствора (  = 1,050 г/мл) ?
= 1,050 г/мл) ?
19. Какой объем 50%-ного раствора КОН (  = 1,538 г/мл) требуется для приготовления 3 л 6%-ного раствора (
= 1,538 г/мл) требуется для приготовления 3 л 6%-ного раствора (  = 1,048 г/мл) ?
= 1,048 г/мл) ?
20. Какой объем 10%-ного раствора карбоната натрия (  =1,105 г/мл) требуется для приготовления 5 л 2%-ного раствора (
=1,105 г/мл) требуется для приготовления 5 л 2%-ного раствора (  =1,02 г/см3) ?
=1,02 г/см3) ?
21. Чему равна нормальная концентрации 30%-ного раствора NaОН (  = 1,328 г/мл)? К 1 л этого раствора прибавили 4 л воды. Вычислите процентную концентрацию полученного раствора.
= 1,328 г/мл)? К 1 л этого раствора прибавили 4 л воды. Вычислите процентную концентрацию полученного раствора.
22. Какой объем 40%-ного раствора Н3РО4 (  = 1,25г/мл) требуется для приготовления 200 мл 1 М раствора Н3РО4?
= 1,25г/мл) требуется для приготовления 200 мл 1 М раствора Н3РО4?
23. К 100 мл 96%-ной (по массе) H2SО4 (  = 1,84 г/мл) прибавили 400мл воды. Определите процентную и нормальную концентрации полученного раствора (
= 1,84 г/мл) прибавили 400мл воды. Определите процентную и нормальную концентрации полученного раствора (  =1,220 г/мл).
=1,220 г/мл).
24. К 3 л 10%-ного раствора НNО3 (  = 1,054 г/мл) прибавили 5 л 2%-ного раствора той же кислоты (
= 1,054 г/мл) прибавили 5 л 2%-ного раствора той же кислоты (  = 1,009 г/мл). Определите процентную и молярную концентрации полученного раствора.
= 1,009 г/мл). Определите процентную и молярную концентрации полученного раствора.
25. К 1 л 10%-ного раствора КОН (р = 1,092г/см3) прибавили 0,5 л 5%-ного раствора КОН (р = 1,045г/см3). Определите молярную и процентную концентрации полученного раствора.
26. Смешали 10 мл 10%-ного раствора НNO3 (  =1,056 г/мл) и 100 мл 30%-ного раствора НNО3 (
=1,056 г/мл) и 100 мл 30%-ного раствора НNО3 (  = 1,184 г/мл). Определите процентную концентрацию полученного раствора.
= 1,184 г/мл). Определите процентную концентрацию полученного раствора.
27. Смешали 300 г 20%-ного раствора и 500 г 40%-ного раствора NaСl. Чему равна процентная концентрация полученного раствора?
28. Смешали 200 г 10%-ного раствора и 400 г 30%-ного раствора NaОН. Чему равна процентная концентрация полученного раствора?
29. Сколько граммов 20%-ного раствора NaCl нужно добавить к 200г воды, чтобы получить 5 %- ный раствор соли?
30. Смешали 200 г 15 %-ного раствора и 400 г 20 %-ного раствора NaСl. Чему равна процентная концентрация полученного раствора?
31. Смешали 230 г 60 %-ного и 140 г 15 %-ного раствора серной кислоты. Чему равна процентная концентрация полученного раствора?
32. Определить массовую долю вещества в растворе, полученном смешением 300 г 25%-ного и 400 г 40 %-ного растворов этого вещества.
33. Сколько граммов 30 %-ного раствора NaCl нужно добавить к 300г воды, чтобы получить 10%- ный раствор соли?
34. Какой объем воды надо прибавить к 100 мл 20%-ного раствора H2S04 (р = 1,14 г/мл), чтобы получить 5%-ный раствор?
35. К 500 мл 32%-ной HNО3 (  = 1,20 г/мл) прибавили 1 л воды. Чему равна процентная концентрация полученного растворе?
= 1,20 г/мл) прибавили 1 л воды. Чему равна процентная концентрация полученного растворе?
36. До какого объема надо разбавить 500 мл 20%-ного (по массе) раствора NaCl (  = 1,152 г/мл), чтобы получить 4,5%-ный раствор (
= 1,152 г/мл), чтобы получить 4,5%-ный раствор (  = 1,029 г/мл)?
= 1,029 г/мл)?
37. Какой объем 2 М раствора Na2CО3 надо взять для приготовления 1 л 0,25 н раствора?
38. Сколько миллилитров 96%-ного раствора H2SО4 (р = 1,84 г/мл) нужно взять для приготовления 1 л 0,25 н. раствора?
39. Сколько миллилитров 0,5 М раствора H2SO4 можно приготовить из 15 мл 2,5 М раствора?
40. Какой объем 0,1 М раствора Н3РО4 можно приготовить из 75 мл 0,75 н. раствора?
41. Какую массу 20%-ного (по массе) раствора КОН надо добавить к 1 кг 50%-ного раствора, чтобы получить 25%-ный раствор?
42. Какой объем 2 н. раствора H2SO4 потребуется для приготовления 500 мл 0,5 н. раствора?
43. Какой объем концентрированной соляной кислоты (р=1,19 г/мл), содержащей 38% (масс.) НСl, нужно взять для приготовления 1 л 2 н. раствора?
44. Какой объем 6,0 М раствора НСl нужно взять для приготовления 25 мл 2,5 М раствора HCl?
45. На нейтрализацию 31 мл 0,16 н. раствора щелочи требуется 217мл раствора Н2SО4. Чему равны нормальность и титр раствора Н2SО4?
46. Какой объем 0,3 н. раствора кислоты требуется для нейтрализации раствора, содержащего 0,32 г NaОН в 40 мл?
47. На нейтрализацию 1л раствора, содержащего 1,4г КОН, требуется 50 мл раствора кислоты. Вычислите нормальность раствора кислоты.
48. Какая масса НNОэ содержалась в растворе, если на нейтрализацию его потребовалось 35 мл 0,4 н. раствора NаОН? Каков титр раствора NaОН?
49. Для нейтрализации 30 мл 0,1 н. раствора щелочи потребовалось 12 мл раствора кислоты. Определить нормальность кислоты.
50. Сколько и какого вещества останется в избытке, если к 75мл 0,3н. раствора Н2SО4 прибавить 125 мл 0,2 н. раствора КОН ?
51. Для осаждения в виде АgСl всего серебра, содержащегося в 100мл раствора АgNОэ, потребовалось 50 см3 0,2 н. раствора НСl. Какова нормальность раствора АgNОз? Какая масса АgСl выпала в осадок?
52. Сколько граммов 2%-ного раствора АgNОз дадут при взаимодействии с избытком NaCl 1,35 г осадка AgCl?
53. Сколько граммов СаСО3 выпадает в осадок, если к400 мл 0,5 н. раствора СаСl2 прибавить избыток раствора соды?
54. Для нейтрализации 20 мл 0,1 н. раствора кислот потребовалось 8 мл раствора NaOH. Сколько граммов NaOH содержит 1 л этого раствора?
55. На нейтрализацию 40 мл раствора щелочи израсходовано 24 мл 0,5 н. раствора H2SO4. Какова нормальность раствора щелочи? Какой объем 0,5н. раствора НСl потребовался бы для той же цели?
56. Для нейтрализации раствора, содержащего 2,95 г кислоты, потребовалось 25 мл 2 н. раствора щелочи. Определить эквивалентную массу кислоты.
57. На нейтрализацию 20 мл раствора, содержащегося в 1 л 12 г щелочи, израсходовано 24 мл 0,25 н. раствора кислоты. Рассчитать20. Для осаждения всего серебра, содержащегося в 100 мл раствора AgNО3, потребовалось 50 мл 0,2 Н раствора HCI. Чему равна нормальная концентрация раствора AgNО3?
58. Какой объем 10%-ной (по массе) серной кислоты (р *- 1,07 г/мл) потребуется для нейтрализации раствора, содержащего 16,0 г NaOH?
59. Какой объем 0,2 н. раствора щелочи потребуется дляосаждения в виде Fe(OH)3 всего железа, содержащегося в 100 мл 0,5 н. раствора FeCl3?
60. Какой объем 0,3 Н раствора кислоты требуется для нейтрализации раствора, содержащего 0,32 г NaOH в 40 мл?
Литература
1. Коровин Н.В. Общая химия – М.: Высшая школа, 1998. – 539 с.
2. Глинка Н. Л. Общая химия / под ред. Б. И. Ермакова. – М.: Интеграл-Пресс, 2003. – 728 с.
3. Романцева Л.М. и др. Сборник задач и упражнений по химии: учеб. пособие для нехим. спец. вузов. – М.: Высшая школа, 1991. – 288 с.
4. Глинка Н. Л. Задания и упражнения по общей химии. – М.: Интеграл-Пресс, 2001. – 240 с.
5. Лидин Р. А. Общая и неорганическая химия в вопросах. – М.: Дрофа, 2004. – 304 с.
6. Метельский А. В. Химия в вопросах и ответах. Справочник. – Мн.: Бел.Эн., 2003. – 544 с.
7. Коренев Ю. М. Задачи вопросы по общей химии. – М.: Мир, 2004. – 368 с.
8. Зоммер К. Химия. Справочник. – М.: Дрофа, 2003. – 384 с.