ОСНОВНЫЕ ПОНЯТИЯ
РАСТВОРЫ
Методические указания
к выполнению самостоятельной работы по курсу «Химия»
для студентов специальностей
120100, 170900, 290300, 060800, 100400, 250600,170500
очной и очно-заочной форм обучения
Одобрено
редакционно-издательским советом
Балаковского института техники,
технологии и управления
 Балаково 2008
Балаково 2008
ОСНОВНЫЕ ПОНЯТИЯ
Раствор – сложная гомогенная система, состоящая из двух или более компонентов. Раствор состоит из растворенных веществ и растворителя, в котором равномерно распределены вещества. Растворитель в чистом виде существует в таком же агрегатном состоянии, что и раствор. Если оба компонента до растворения находились в одинаковом агрегатном состоянии (вода-спирт), то растворителем считается компонент, находящийся в боль-шем количестве. Различают растворы коллоидные и истинные. Коллоидные растворы – дисперсные системы, обладающие микрогетерогенностью. В истинных растворах вещества раздроблены до молекулярного или ионного состояния, и молекулы и ионы одних компонентов равномерно распределены среди молекул растворителя.
Количественные соотношения между компонентами, образовавшими раствор, могут изменяться в широких пределах. Важнейшей характеристикой раствора является концентрация – содержание растворенного вещества в определенной массе или определенном объеме. Наиболее часто используются следующие способы выражения концентрации:
1. Процентная концентрация С% (массовая доля  ) – отношение массы растворенного вещества к общей массе раствора, выраженное в про-центах.
) – отношение массы растворенного вещества к общей массе раствора, выраженное в про-центах.
Процентная концентрация может рассматриваться как безразмерная, если от процентов перейти к массовым долям. Массовая доля показывает, сколько граммов растворенного вещества содержится в 100г раствора:
 , (
, (  ) , (1)
) , (1)
 , (2)
, (2)
 , (3)
, (3)
где C% – процентная концентрация, %;
mр.в. – масса растворенного вещества, г;
mр-ра – масса раствора, г;
mр-ля – масса растворителя, г;
Vр-ра – объем раствора, мл;
 - плотность раствора, г/мл.
- плотность раствора, г/мл.
2. Молярная концентрация См (молярность) – количество молей растворенного вещества в 1 литре раствора:
 , (4)
, (4)
где Cм – молярная концентрация, моль/л, М;
nр.в. – число молей растворенного вещества;
Vр-ра – объем раствора, л;
mр.в. – масса растворенного вещества, г;
Мр.в. – мольная масса растворенного вещества, г/моль.
3. Моляльная концентрация Сm (моляльность) – количество молей растворенного вещества в 1 кг растворителя:
 , (5)
, (5)
где Cm – молярная концентрация, моль/кг;
nр.в. – число молей растворенного вещества;
mр-ля – масса растворителя, кг;
mр.в. – масса растворенного вещества, г;
Мр.в. – мольная масса растворенного вещества, г/моль.
4. Нормальная концентрация Сн (нормальность) – количество эквивалентных масс растворенного вещества в 1 л раствора:
 , (6)
, (6)
где Cн – молярная концентрация, моль/л, Н;
nэк – число эквивалентов растворенного вещества;
Vр-ра – объем раствора, л;
mр.в. – масса растворенного вещества, г;
mэк – эквивалентная масса растворенного вещества, г/моль.
5. Титр раствора Т – количество граммов вещества в 1 мл раствора:
 , (7)
, (7)
где Т – титр раствора, г/мл ;
mр.в. – масса растворенного вещества, г;
Vр-ра – объем раствора, л.
Зная нормальность раствора и эквивалентную массу растворенного вещества, титр можно найти по формуле:
 , (8)
, (8)
где Т – титр раствора,
Cн – молярная концентрация, моль/л, Н;
mэк – эквивалентная масса растворенного вещества, г/моль;
1000 – объем раствора, мл.
Вещества взаимодействуют в эквивалентных количествах. Растворы равной нормальности взаимодействуют между собой в равных объемах, так как содержат равные доли эквивалентов. Если взаимодействуют два растворенных вещества разной нормальности, то их объемы можно вычислить по уравнению:
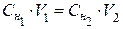 , (9)
, (9)
где Сn1, Сn2 – нормальная концентрация реагирующих веществ, моль/л, Н;
V1, V2 – объемы реагирующих растворов, л.