Дебая – Хюккеля – Онзагера
В растворах сильных электролитов изменение молярной электрической проводимости с ростом концентрации обусловлено влиянием электростатического взаимодействия на скорость их движения, а следовательно, на их и подвижность. При этом коэффициент электрической проводимости электролита fλ уменьшается, и уменьшается молярная электропроводность электролита λС:
λС = f λ·λ0.
Максимальное значение молярной электрической проводимости λ0 электролит имеет при бесконечном разведении.
На основе электростатической теории сильных электролитов Дебай. Хюккель и Онзагер получили выражение для молярной электрической проводимости бесконечно разбавленных растворов сильных электролитов. Изменение молярной электрической проводимости растворов сильных электролитов с изменение концентрации Дебай и Хюккель объясняли торможением движения ионов в электрическом поле из-за их электростатического взаимодействия. С увеличением концентрации раствора ионы сближаются, и электростатическое взаимодействие между ними возрастает. При этом усиливаются два эффекта, вызывающие электростатическое взаимное торможение ионов: электрофоретический и релаксационный.
Все ионы окружены ионными атмосферами, в которых преобладают ионы противоположного знака заряда. Электрофоретический эффект заключатся в том, что под действием внешнего электрического поля ионы и их ионные атмосферы движутся в противоположных направлениях. Таким образом, движение ионов какого-либо знака будет происходить в среде, перемещающейся в противоположном направлении. Сила трения пропорциональна скорости движения. Уменьшение электрической проводимости должно быть пропорционально электрофоретической силе трения.
Было установлено, что образование и разрушение ионной атмосферы в процессе движения ионов происходит с большой, но конечной скоростью. Характеристикой этой скорости служит время релаксации, которое рассматривают как величину обратную скорости создания или разрушения ионной атмосферы. Время релаксации зависит от ионной силы раствора, его вязкости и диэлектрической проницаемости.
При перемещении центрального иона проходит время, пока старая ионная атмосфера не разрушится и не сформируется новая. Поэтому позади иона будет всегда находиться некоторый избыток заряда противоположного знака, и возникающие электрические силы притяжения будут тормозить его движение. Этот эффект торможения называется релаксационным.
Уменьшение электропроводности с ростом концентрации раствора электролита описывается уравнением:
λС =λ0 – ΔλЭФ. – ΔλРЕЛ,
где ΔλЭФ – изменение молярной электропроводности связанное с электрофоретическим эффектом торможения;
ΔλРЕЛ – изменение молярной электропроводности связанное с релаксационным эффектом торможения.
Для водных растворов 1-1-валентных электролитов при Т =298К Онзагером было получено уравнение, описывающее зависимость молярной электропроводности от концентрации раствора:
λС =λ0 – (А + В·λ0)· 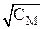 ,
,
где А и В – константы, зависящие от температуры, диэлектрической проницаемости и вязкости растворителя.
Это уравнение является теоретическим обоснованием эмпирического уравнения Кольрауша для разбавленных растворов, называемого «законом квадратного корня»:
λС =λ0 – а 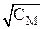 ,
,
где а – эмпирический коэффициент.
Опираясь на это уравнение, можно графическим методом определить молярную электропроводность раствора сильного электролита при бесконечном разведении.