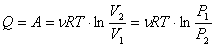Изопроцессы — равновесные процессы, в которых один из основных параметров сохраняется.
ИЗОБАРНЫЙ ПРОЦЕСС (P=const)
Для изобарного процесса в идеальном газе справедлив закон Гей-Люссака:
при постоянном давлении объем данной массы газа прямо пропорционален его термодинамической температуре: V/T=const ; V1/T1=V2/T2
Работа газа при изобарном расширении:

Изменение внутренней энергии:

Количество полученного тепла в соответствии с первым началом термодинамики:
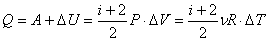 .
.
Молярная теплоемкость при изобарном процессе:
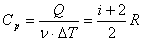 .
.
ИЗОХОРНЫЙ ПРОЦЕСС (V=const)
Изохорный процесс в идеальном газе описывается законом Шарля:
при постоянном объеме давление данной массы газа прямо пропорционально его термодинамической температуре: P/ Т=const ; P1/T1=P2/T2
Работа газа при изохорном процессе равна нулю:A=0.
Все полученное тепло идет на изменение внутренней энергии в соответствии с первым началом термодинамики:
 .
.
Молярная теплоемкость при изохорном процессе:
 .
.
ИЗОТЕРМИЧЕСКИЙ ПРОЦЕСС (T=const)
Изотермический процесс в идеальном газе подчиняется закону Бойля - Мариотта:
для данной массы газа при неизменной температуре произведение значений давления и объема есть величина постоянная: PV=const ; P1V1=P2V2
Работа газа при изотермическом расширении:
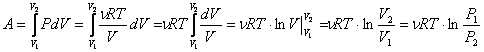 .
.
Изменение внутренней энергии при изотермическом процессе равно нулю:
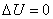 .
.
Все полученное тепло идет на совершение работы в соответствии с первым началом термодинамики: