Вычисление работы деформации газа
При изучении процессов изменения состояния газа широко используют графический метод, основанный на применении так называемой PV-диаграммы, где давление является функцией от объема (p=f(V)). Параметр p откладывается по оси ординат, а V – по оси абсцисс. Такое изображение применяют обычно при исследованиях процессов поршневых двигателей, где путь, проходимый поршнем, пропорционален приращению объема рабочего тела, заключенного в цилиндре.
Рассмотрим процесс расширения газа в двигателе внутреннего сгорания (DBC). Пусть в цилиндре DBC находится 1 кг идеального газа. Поскольку поршень неподвижен, система находится в равновесии. Это равновесное состояние на диаграмме PV обозначено точкой 1. Выведем систему из равновесия, подведя к ней некоторое количество тепла, при этом поршень начнет перемещаться вправо и через некоторое время наступит новое равновесное состояние газа, которое на диаграмме определено точкой 2.
Соединив точки 1 и 2, получим линию термодинамического процесса. Разобьем этот процесс на бесконечно большое количество элементарных процессов и рассмотрим один из них: 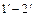 .
.
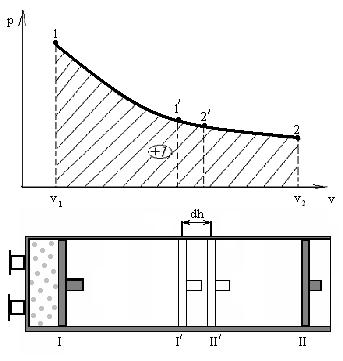
Рис 1.1 - Вычисление работы деформации газа с помощью PV-диаграммы
По общим правилам механики работа определяется произведением приложенных к телу сил на вызванное ими перемещение:
dl=P∙dh (1.10)
Сила P в данном случае это сила давления молекул газа на стенки сосуда. Тогда элементарная работа запишется:
dl=p∙f∙dh=p∙dV (т.к. f∙dh=dV) (1.11)
Полная работа при конечном изменении объема от V1 до V2 определяется по формуле:
 (1.12)
(1.12)
В координатах р,V это количество работы характеризуется площадью V1-1-2-V2 под линией процесса (рис. 1.1). Под этой работой будем в дальнейшем понимать работу изменения объема газа. Для решения интеграла (1.12) необходимо знать функциональную зависимость p=f(V), т.е. термодинамический процесс, например 12. Следовательно, работа зависит от вида процесса.
Фундаментальными процессами, изучаемыми классической равновесной термодинамикой, являются:
изотермический (Т= const), когда система находится в контакте с источником теплоты постоянной температуры;
изобарный – процесс, протекающий при постоянном давлении (p=const);
изохорный – процесс, характеризующийся тем, что переход газа из одного состояние в другое происходит при постоянном удельном объеме (V=const).
Для каждого процесса работа деформации газа определяется следующими соотношениями:
изобарный процесс (p=const):
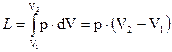 (1.13)
(1.13)
изохорный процесс (V=const):
 , т.к. dV=0 (1.14)
, т.к. dV=0 (1.14)
изотермический процесса (T=const):
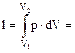
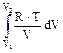
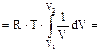
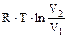 (1.15)
(1.15)