Вопрос 1(10)ф.химия
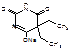 Барбитал-натрий (МНН)Barbitalum-natrium 5,5-диэтилбарбитурат натрия. Фармакологическая группа - снотворные средства. Применяется в медицинской практике как снотворное и успокаивающее средство. Благодаря легкой растворимости в воде, действует быстрее, чем барбитал. Также быстрее выводится из организма, менее токсичен. Назначают перед сном.
Барбитал-натрий (МНН)Barbitalum-natrium 5,5-диэтилбарбитурат натрия. Фармакологическая группа - снотворные средства. Применяется в медицинской практике как снотворное и успокаивающее средство. Благодаря легкой растворимости в воде, действует быстрее, чем барбитал. Также быстрее выводится из организма, менее токсичен. Назначают перед сном.
2. Относится к производным барбитуровой кислоты, или производным пиримидина.
3. Это белый кристаллический порошок, без запаха. Гигроскопичен. Легко растворим в воде, мало растворим в этаноле, практически нерастворим в эфире. Водный раствор барбитала-натрия имеет щелочную реакцию.
Подлинность барбитала-натрия можно установить по ИК-спектру. Для идентификации барбитала-натрия используют химические реакции, основанные на соле- и комплексообразовании с солями тяжелых металлов, сплавлении со щелочами, окислении, нейтрализации натриевых солей, обнаружении ионов натрия и функциональных групп.
Барбитал-натрия образует нерастворимые соли с ионами серебра, ртути (II), меди (П). Эти реакции выполняют в смеси растворов гидрокарбоната и карбоната натрия. Барбитал-натрия образует с ионом кобальта комплексное соединение, окрашенное в сине-фиолетовый цвет. С ионами серебра происходит образование однозамещенных (растворимых в воде) и двузамещенных (нерастворимых в воде) солей серебра:
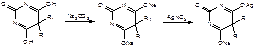 При добавлении избытка нитрата серебра однозамещенная соль превращается в двузамещенную серебряную соль:
При добавлении избытка нитрата серебра однозамещенная соль превращается в двузамещенную серебряную соль:
 При последующем подкислении хлороводородной кислотой ощущается запах жирной кислоты и выделяется диоксид углерода:
При последующем подкислении хлороводородной кислотой ощущается запах жирной кислоты и выделяется диоксид углерода:
Na2CO3 + 2HCl ¾® 2NaCl + CO2 + H2O

Отличают солевые формы барбитуров от кислотных по растворимости. Натриевые соли гигроскопичны, растворимы или очень легко растворимы в воде. Барбитал-натрия при подкислении разведенной соляной кислотой образует осадок:
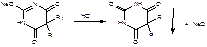
Выпавший осадок барбитала отфильтровывают, промывают и сушат. Определяют температуру плавления.Ион натрия обнаруживают по окраске пламени (желтый цвет). Для количественного определения барбитала-натрия используют физико-химические методы анализа: УФ-спектроскопию, фотоколориметрию, хроматографию. Солевые формы барбитуратов определяют количественно методом нейтрализации в присутствии спирта или в среде неводных растворителей.Барбитал-натрия титруют в водной среде 0,1 М раствором хлористоводородной кислоты по индикатору метиловому оранжевому до розовой окраски:
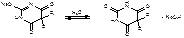
NaOH +HCl ¾® NaCl + H2O
| ЗАДАЧА 14 |
Для кислотных форм используют алкалиметрическое титрование в спиртовой среде.
При испытании чистоты барбитал-натрия устанавливают предельное содержание примеси свободной щелочи, метилового спирта и др., которые могут появиться в процессе синтеза. Свободную щелочь определяют методом ацидиметрии.Наличие примесей устанавливают методом тонкослойной хроматографии. На хроматограмме допускается не более одного постороннего пятна.