Газовые смеси
Смесь идеальных газов, химически не взаимодействующих между собой, называется идеальной газовой смесью.
Состав газовой смеси определяется количеством каждого из газов, входящих в смесь, и может быть задан массовыми или объемными долями. Массовая доля – отношением массы отдельного газа, входящего в смесь, к массе всей смеси:
 ,
,  ,
,  , …,
, …,  , ( 1.13)
, ( 1.13)
где М1, М2, М3, …, Мn – массы отдельных газов и М – масса всей смеси.
Объемной долей газа называют отношение объема каждого компонента, входящего в смесь, к объему всей газовой смеси при условии, что объем каждого компонента отнесен к давлению и температуре смеси (приведенный объем или парциальный объем, т.е. тот объем, который занимал бы компонент, если бы он, имея температуру смеси, находился под давлением смеси):
 ,
,  ,
,  , ...,
, ...,  , (1.14)
, (1.14)
где V1, V2, V3, …, Vn – парциальные (приведенные) объемы компонентов газов, входящих в смесь; V – общий объем газовой смеси. Очевидно, что:

 ,
,
а также
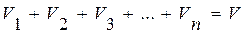
 .
.
В соответствии с законом Дальтона давление смеси р равно сумме парциальных давлений отдельных компонентов смеси (давление, которое имел бы данный компонент, если он занимал бы весь объем при температуре смеси):
 .
.
Парциальные давления определяются проще всего, если известны объемные доли отдельных компонентов, входящих в смесь:
 ,
, 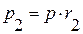 и т.д.
и т.д.
или вообще
 ,
,
где рi – парциальное давление любого газа, входящего в смесь.
Если известны массовые доли, то парциальное давление любого газа, входящего в смесь,
 . (1.15)
. (1.15)
Газовую постоянную смеси газов ( ) можно выразить или через газовые постоянные отдельных компонентов, входящих в смесь, или через кажущуюся молекулярную массу смеси (µсм)
) можно выразить или через газовые постоянные отдельных компонентов, входящих в смесь, или через кажущуюся молекулярную массу смеси (µсм)
 , Дж/(кг∙К) (1.16)
, Дж/(кг∙К) (1.16)
или
 , Дж/(кг∙К) (1.17)
, Дж/(кг∙К) (1.17)
Уравнение состояния для i – го компонента смеси имеет вид
 ,
,
а для смеси газов
 . (1.18)
. (1.18)
 . (1.19)
. (1.19)