В механизме синтеза треонина и лизина есть общие реакции
Треонин и лизин - незаменимые у млекопитающих аминокислоты. Они отличаются от остальных аминокислот тем, что при своем распаде они не подвергаются дезаминированию и следовательно не образуют соответствующих кетокислот, из которых их можно было бы получить. У микроорганизмов синтез треонина и лизина начинается преобразованием оксалоацетата в аспарагиновый полуальдегид. Этот путь использует одну молекулу АТФ и две молекулы НАДФH + Н+
Биосинтез треонина завершается в три этапа. Вначале реакция восстановления при участии НАДФH + Н + дает гомосерин, который после фосфорилирования в гомосеринфосфат с затратой АТФ превращается в треонин
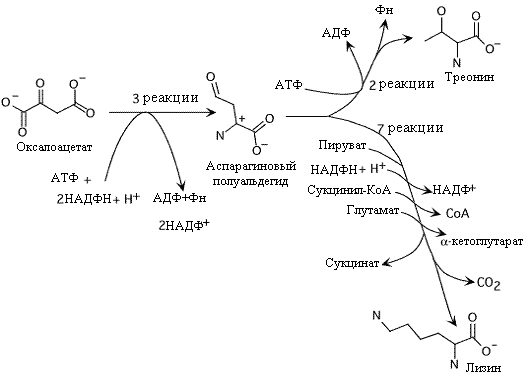
. Синтез треонина и лизина. Обратите внимание на количество энергии, которая израсходована в этих биосинтезах.
На рис приводится обобщенный путь синтеза лизина, хотя он различается у разных бактерий. Синтез лизина включает присоединение пирувата к аспарагиновому полуальдегиду, использование КоА производных (или ацетил-КоА или сукцинил-КoA) и присединение аминогруппы глутамата. Ацил-КоА (сукцинил, или ацетил) играют роль блокирующей группы, защищающей аминогруппу от атаки во время переаминирования глутаматом. NAДФH +Н+ используется для восстановления на втором этапе пути.