Химические свойства
Старое название фенола – карболовая кислота, указывает на выраженные кислотные свойства. Фенолы более сильные кислоты, чем спирты (pKa фен = 10, pKa МеОН = 16). Причина таких свойств – повышенная, по сравнению с алкоксид-, стабильность фенолят аниона за счет сопряжения.

Образование фенолятов возможно в реакциях с водными щелочами. Обратная реакция протекает под действием любой минеральной кислоты.
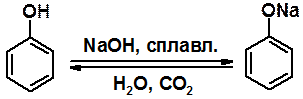
Заместители в бензольном цикле заметно влияют на кислотность. Наличие в положениях 2 или/и 4 или/и 6 электроноакцепторных групп увеличивает кислотность. Причем, чем больше акцепторов в указанных положения, тем легче проходит замещение галогена.
Если в положениях 2 или/и 4 или/и 6 расположены электронодонорные группы, кислотность уменьшается. Причем, чем больше доноров в указанных положения, тем труднее происходит замещение галогена.
Если акцепторные или донорные группы расположены в положениях 3 или/и 5 их активирующее или дезактивирующее действие выражено очень слабо.
Для объяснения изменений кислотности фенолов надо рассмотривать стабильность образующегося аниона. Логика анализа феноксид-аниона по устойчивости граничных структур аналогична рассмотрению стабильности s-комплекса, в реакциях нуклеофильного замещения галогена в ароматическом ряду (см. лекцию 25).