Получение коллоидного раствора AgI
(метод химической конденсации)
AgNO3 + KI = AgI + KNO3
Дисперсионная среда – вода, в ней частицы AgI. Если взять строго эквивалентное количество реагентов (без избытка и недостатка), то выпадает осадок AgI (так как AgI в воде нерастворим).
Как образуется осадок?
После смешения двух растворов во всем объеме образуются молекулы AgI. Далее ближайшие молекулы при столкновении слипаются и образуются более крупные.
Эти частицы грубодисперсные и они выпадают в осадок. Чтобы получился коллоидный раствор вещество должно быть в избытке.
А) если в избытке AgNO3 , то после реакции во всем объеме образуются молекулы AgI , а в растворе остаются ионы К+; NO3-; Ag+. Когда в растворе образуются коллоидные частицы, на них сразу начинается адсорбция ионов Ag – специфическая адсорбция: на поверхности твердого адсорбируются те ионы, которые уже находятся в решетке. В растворе быстро наступает равновесие, так как положительно заряженные ионы Ag, прикрепившиеся к коллоидной частице AgI, не дают возможности молекулам AgI распадаться, а также не позволяют другим ионам Ag присоединяться. Затем эта комплексная частица с положительным зарядом начинает присоединять ионы NO3-. Но адсорбция NO3- идет не до полной нейтрализации заряда, так как этих ионов недостаточно для полной нейтрализации положительного заряда частицы (на 100 Ag+ 92 NO3-). Ионы NO3- притягиваются частицей и удерживаются около нее в диффузионном слое. Не любая сила способна притянуть и удержать ион, так как он движется.
Таким образом, в растворе все коллоидные частицы одноименно заряжены, при столкновении они отталкиваются. В данном случае избыток AgNO3 выступает в качестве стабилизатора.
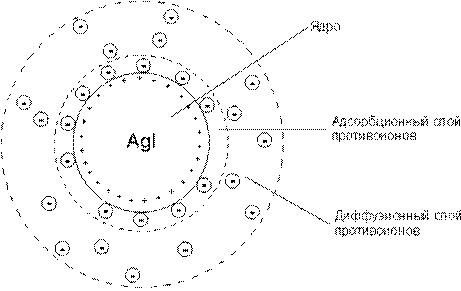
Строение коллоидной частицы
{[m•AgI]n•Ag+ (n-x) NO3-}x+ x•NO3-
[m•AgI] – из какого вещества состоит коллоидная частица.
m – число частиц, составляющих коллоидную частицу.
n – число ионов, адсорбирующихся первыми на поверхности заряженных частиц (обычно n=100). Это потенциалопределяющие ионы или адсорбционный слой противоионов.
x – число ионов противоположного знака, находящихся в диффузионном слое частицы (обычно x=8) – диффузный слой противоионов.
(n-x) – число частиц на поверхности.
[ ] – ядро, сама частица.
{ } – ядро с адсорбированными на поверхности ионами; гранула.
Все вместе – коллоидная мицелла.
Б) если избыток KI, то формула коллоидной частицы
{[m•AgI]n•I- (n-x) K+}x- x•K+
На поверхности коллоидной частицы адсорбируются I- , в диффузионном слое ионы К+. Образуется коллоидный раствор с отрицательно заряженными частицами. Чтобы получился коллоидный раствор, исходные концентрации веществ должны быть умеренные (0,001 н.). Если растворы концентрированные, то выпадает осадок.
AgNO3 + KI = AgI ↓+ KNO3
При больших концентрациях образуется много молекул AgI, то есть много коллоидных частиц, расстояние между ними маленькое, ионы Ag+ не успевают адсорбироваться и частицы слипаются. Если же концентрация слишком мала, то частиц AgI мало и их не хватит для роста до размеров коллоидной частицы. Необходимая концентрация определяется опытным путем. Чтобы убедиться в коллоидности раствора пользуются различными методами.
1. фильтрование – грубодисперсные растворы проходят через фильтр не полностью
2. опалесценция – изменение окраски раствора при падении света под разными углами зрения. Это явление характерно только для коллоидных растворов.