Правила расстановки степеней окисления
1. у простых веществ степень окисления всегда равна нулю;
2. в сложных веществах у фтора степень окисления всегда –1;
3. в сложных веществах у металлов всегда положительные степени окисления, обычно совпадающие с валентностью;
4. степень окисления кислорода в большинстве соединений –2;
Исключения
5. степень окисления водорода в большинстве соединений +1;
Исключения
6. суммарная степень окисления молекулы (ФЕ) равна 0, аниона – заряду аниона (n –), катиона – заряду катиона (n +).
Учитывая вышеизложенное: ОВР протекает в прямом направлении, если ее ЭДС положительна, т.е. Е>О; в противном случае (Е<О) ОВР будет протекать в обратном направлении. ЭДС, вычисленная для стандартных условий, называется стандартной и обозначается Е
Уравнение Нернста — уравнение, связывающее окислительно-восстановительный потенциал системы с активностями веществ, входящих в электрохимическое уравнение, и стандартными электродными потенциалами окислительно-восстановительных пар.
Нернст изучал поведение электролитов при пропускании электрического тока и открыл закон. Закон устанавливает зависимость между электродвижущей силой ( разностью потенциалов ) и ионной концентрацией. Уравнение Нернста позволяет предсказать максимальный рабочий потенциал, который может быть получен в результате электрохимического взаимодействия, когда известны давление и температура. Таким образом, этот закон связывает термодинамику с электрохимической теорией в области решения проблем, касающихся сильно разбавленных растворов.  ,
,
где
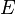 — электродный потенциал,
— электродный потенциал,  — стандартный электродный потенциал, измеряется в вольтах;
— стандартный электродный потенциал, измеряется в вольтах;
 — универсальная газовая постоянная, равная 8.31 Дж/(моль·K);
— универсальная газовая постоянная, равная 8.31 Дж/(моль·K);
 — абсолютная температура;
— абсолютная температура;
 — постоянная Фарадея, равная 96485,35 Кл·моль−1;
— постоянная Фарадея, равная 96485,35 Кл·моль−1;
 — число электронов, участвующих в процессе;
— число электронов, участвующих в процессе;
 и
и  — активности соответственно окисленной и восстановленной форм вещества, участвующего в полуреакции.
— активности соответственно окисленной и восстановленной форм вещества, участвующего в полуреакции.
Если в формулу Нернста подставить числовые значения констант  и
и  и перейти от натуральных логарифмов к десятичным, то при
и перейти от натуральных логарифмов к десятичным, то при  получим
получим
