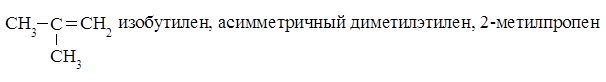Изомерия. Номенклатура
Как и в ряду предельных углеводородов структурная изомерия алкенов начинается с четвертого члена ряда. Однако число изомеров значительно больше. Изомерия олефинов обусловлена строением углеродной цепи, во-вторых – положением двойной связи в цепи и в-третьих – пространственным расположением атомов или групп при углеродах с двойной связью. Последний вид изомерии носит название геометрической или цис-транс-изомерии. Если вращение вокруг простой s-связи требует небольшого количества энергии
(8…20 кДж·моль-1), которая сообщается молекуле при комнатной температуре и даже ниже, при вращении вокруг двойной связи должна разрываться π-связь, а это примерно 250 кДж·моль-1. Поэтому поворот вокруг двойной связи возможен лишь при высоких температурах, облучении или присутствии катализаторов, когда π-связь разрывается. По этим причинам в алкенах не существует изомеров вращения вокруг двойной связи, а олефины из-за невозможности вращения вокруг двойной связи при обычных условиях присутствуют в виде стабильных геометрических изомеров. Алкены, имеющие у каждого из двух атомов углерода при двойной связи различные заместители, могут существовать в виде двух пространственных изомеров, отличающихся расположением этих заместителей относительно плоскости π-связи. Так, в молекуле бутена-2 группы СН3 могут находиться либо по одну сторону от двойной связи в цис-изомере, либо по разные стороны в транс-изомере:

При гидрировании оба бутена-2 дают один и тот же бутан.
Называют алкены по различным номенклатурам. В тривиальной номенклатуре к названию соответствующего радикала предельного углеводорода добавляют суффикс –ен: этилен, пропилен, бутилен, изобутилен, амилен и т.д. По рациональной номенклатуре олефины называются как производные этилена. При составлении названия по номенклатуре ИЮПАК в качестве основной цепи соединения выбирается самая длинная углеродная цепочка, включающая двойную связь. За основу названия берется название алкана с заменой окончания -ан на
-ен. Цифрой обозначают номер атома углерода, за которым следует двойная связь. Нумеровать углеродные атомы основной цепи следует с того конца, к которому ближе двойная связь.
Например:
СН2=СН2 этилен; этен