Первое начало термодинамики. Адиабатический процесс.
Универсальный закон природы — закон сохранения энергии применим и к тепловым явлениям. Закон сохранения энергии гласит:
количество тепла, сообщенное системе, идёт на изменение её внутренней энергии и совершение системой механической работы.
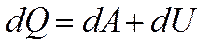 (15)
(15)
где  в свою очередь можно представить как
в свою очередь можно представить как 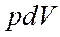 . Это соотношение называют первым началом термодинамики. Принято считать
. Это соотношение называют первым началом термодинамики. Принято считать 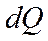 величиной положительной в (15), если тепло подводится к системе, и отрицательной, если система отдаёт тепло. Работа считается положительной, если она совершается системой над внешними телами.
величиной положительной в (15), если тепло подводится к системе, и отрицательной, если система отдаёт тепло. Работа считается положительной, если она совершается системой над внешними телами.
На основании первого начала термодинамики и уравнения состояния идеального газа можно вывести уравнение процесса, протекающего без теплообмена с окружающей средой, т.е. адиабатического процесса. Это - уравнение Пуассона:
 (16)
(16)
где 
II. ОПИСАНИЯ УСТАНОВКИ.
На рисунке 1 представлена экспериментальная установка для определенния  . Она состоит из стеклянного сосуда, в который ручным насосом закачивается воздух, и микроманометра для определения давления в сосуде.
. Она состоит из стеклянного сосуда, в который ручным насосом закачивается воздух, и микроманометра для определения давления в сосуде.
С помощью ручного насоса накачаем в сосуд небольшое количество воздуха и перекроем кран. Давление в сосуде повысится, но окончательно становится лишь через некоторое время. Процесс нагнетания происходит довольно быстро и его можно считать адиабатическим, при этом температура в сосуде сравняется с температурой окружающего воздуха  , микроманометр будет показывать давление
, микроманометр будет показывать давление  (в ммводяного столба). При этом давление воздуха в сосуде, очевидно, равно
(в ммводяного столба). При этом давление воздуха в сосуде, очевидно, равно
 (17)
(17)
где  — атмосферное давление (причём
— атмосферное давление (причём 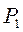 ,
,  и
и 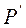 должны быть выражены в одних и тех же единицах).
должны быть выражены в одних и тех же единицах).
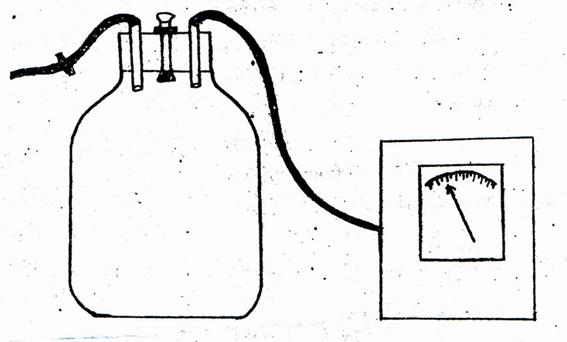
Рис.1.
Итак, исходное состояние воздуха характеризуется параметрами 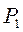 и
и  . Если теперь быстро соединить сосуд с атмосферой, то воздух будет расширяться адиабатически и давление в сосуде станет равным атмосферному
. Если теперь быстро соединить сосуд с атмосферой, то воздух будет расширяться адиабатически и давление в сосуде станет равным атмосферному  . При этом воздух в сосуде охладится до, температуры
. При этом воздух в сосуде охладится до, температуры  . Второе, промежуточное состояние характеризуется параметрами
. Второе, промежуточное состояние характеризуется параметрами  ,
,  .
.
После установления атмосферного давления в сосуде, клапан снова закрывается. Давление в сосуде растёт, т.к. воздух, охладившийся пои быстром расширении, нагревается, и температура в сосуде становится равной температуре окружающего воздуха  .
.
Давление установится при этом
 (18)
(18)
где  - новое показание микроманометра.
- новое показание микроманометра.
К процессу расширения воздуха, т.е. к. переходу из первого
состояния во второе, может быть применен закон Пуассона:
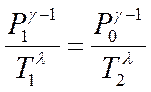 (19)
(19)
В действительности реальный процесс не будет строго описываться
эти уравнением, т.к., во-первых, процесс расширения происходит, во-вторых, масса воздуха в сосуде уменьшается, а рассмотренные выше законы идеального газа сформулированы при условии постоянства массы газа.
Переход из второго состояния к третьему, конечному состоянию происходит при постоянном объёме, следовательно, к нему можно применить уравнение (5)
 (20)
(20)
Преобразуем соотношение (19)

или 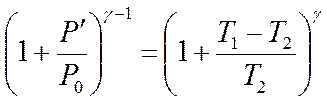
В последнем выражении 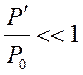 и
и 
Разложим.левую и правую части по формуле Маклорена и ограничимсятолько членами первого порядка малости
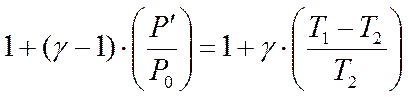
Откуда

Из выражений (18) и (20) имеем
 (21)
(21)
Подставим (21) в предыдущее выражение и разрешив относительно получим:
 (22)
(22)
III.ИЗМЕРЕНИЯ И ОБРАБОТКА РЕЗУЛЬТАТОВ.
1. Осторожно, но достаточно быстро, накачать ручным насосом воздух в сосуд так, чтобы микроманометр показывал избыточное над атмосферным давление в сосуде 25-30 мм водяного столба.
2. После того, как давление установится, произвести отсчёт показаний микроманометра 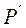 .
.
3. Соединить на короткое время сосуд с атмосферой так, чтобы давление в сосуде стало равным атмосферному, и снова закрыть клапан.
4. После установления давления в сосуде произвести второй отсчет показании микроманометра  .
.
5. По формуле (22) рассчитать  .
.
6. Повторить опыт 10-15 раз, записывая результаты измерений в таблицу:
| № | 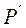
| 
| 
| 
|
| 1. | ||||
| 2. | ||||
| 3. | ||||
| 4. | ||||
| 5. | ||||
| 6. | ||||
| 7. | ||||
| 8. | ||||
| 9. | ||||
| 10. |
7. Рассчитать среднеквадратичную ошибку измерений.
8. Используя соотношение (14), определить число степеней свободы i.
IV. КОНТРОЛЬНЫЕ ВОПРОСЫ.
1. Изобразить графики изотермического, изохорического, изобарического и адиабатического процессов в координатах 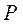 и
и  ,
,  и
и 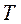 ,
, 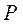 и
и 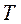 .
.
2. Вывести уравнение Пуассона.
3. Сформулировать-закон равнораспределения энергии по степеням свободы.
4. Дать определение работы в термодинамике. Сформулировать первое начало термодинамики.
-
V.Литература.
1. Кикоин А. Е., Кикоин И. К. Молекулярная физика. Изд.
"Наука", 1976. §§ 5, 20, 23-27,30.
2. Савельев И. В. Курс общей физики. Т. 1. Изд. "Наука", 1970.§§
94,95,96, 101, 102, 103.