Обнаружение ионов железа (II) и (III).
Для установления подлинности соединений железа в ГФ описаны два метода (А и Б) идентификации ионов закисного железа (Fe2+) и три (А, Б и В) ионов окисного железа (Fe3+). Открытие закисного железа (метод А) основано на обработке исследуемого вещества разведенной хлористоводородной кислотой с целью перевода железа в ионизированное состояние и последующей обработке полученного раствора раствором феррицианида калия (красная кровяная соль). При этом образуется синий осадок. В основе этого метода открытия закисного железа лежат следующие реакции:

Феррицианид-ион окисляет закисное железо до окисного, а сам восстанавливается до ферроцианида. После этого в осадок выпадает синий пигмент переменного состава - Fe4[Fe(CN)6]3·nK4[Fe(CN)6]·mH2O, где n = 0,3-0,8; m = 12-24; упрощенно - KFe[Fe(CN)6] (берлинская лазурь, турнбулевая синь, парижская синяя).
Следует отметить, что этот же синий пигмент получается при открытии окисного железа по методу А при действии раствора ферро- цианида калия (желтая кровяная соль) на раствор соли окисного железа, как это отражено в уравнении выше. Осадок берлинской лазури нерастворим в разведенных минеральных кислотах, поэтому его получение осуществляют в кислой среде. Интересно отметить, что ионы Fe2+ с ферроцианидом калия (K4[Fe(CN)6]) образуют белый осадокFe2[Fe(CN)6], который легко окисляется различными окислителями (KBrO3, K2Cr2O7) в кислой среде и превращается в берлинскую лазурь. Ионы Fe3+ с феррицианидом калия (K3[Fe(CN)6]) осадка не дают, но раствор приобретает темно-бурую окраску. Фармакопейные методы открытия ионов Fe2+ и Fe3+, основанные на образовании берлинской лазури при действии соответственно K3[Fe(CN)6] и K4[Fe(CN)6], позволяют различать эти ионы, но с их помощью сложно отличить препарат закисного железа, содержащий примесь окисного железа, от препарата окисного железа, содержащего примесь закисного железа. В связи с этим на окисное железо в ГФ приводится также метод Б, основанный на реакции образования роданидов железа, окрашивающих раствор в красный цвет. Константы устойчивости роданидных комплексов невелики, поэтому для определения требуется высокая концентрация лиганда. В растворе образуется ряд комплексов, различающихся по максимуму поглощения и его интенсивности.
В зависимости от концентрации роданид-иона образуются комплексы различного состава с координационным числом по роданид- иону от 1 до 6:

Это одна из наиболее специфичных реакций на окисное железо. Следует иметь в виду, что она не всегда положительна, так как ряд веществ, образующих более прочные комплексы с Fe3+, чем роданид- ион, мешает появлению окраски. К таким веществам относятся фосфорная, щавелевая, винная, лимонная кислоты и их соли.
Общим реактивом для открытия ионов железа в степени окисления +2 и +3 является сульфид аммония. В обоих случаях выпадают черные осадки сульфидов железа. Некоторое различие можно заметить при растворении этих осадков в минеральных кислотах: при растворении сульфида закисного железа образуется прозрачный бесцветный раствор, а при растворении сульфида окисного железа получается мутноватый раствор вследствие образования серы. Сера частично присутствует в осадке сульфида окисного железа, а частично образуется при окислении сероводорода ионом Fe3+:
FeS + 2HCl → H2S + FeCl2
Fe2S3 + 4HCl → 2FeCl2 + 2H2S + S↓
Рассмотренные методы определения железа позволяют открыть его лишь в препаратах, содержащих простые соли железа, растворимые в воде, например железа закисного сульфат, железа закисного лактат, ферамид и др. Препараты, представляющие собой прочные комплексные соединения железа (ферроцерон, оксиферрискарбон натрия) или нерастворимые в воде (таблетки «Каферид»), предварительно минерализуют с целью перевести железо в раствор.
Выполнение реакций
Общая реакция на закисное и окисное железо.
К раствору соли закисного или окисного железа (около 0,02 г иона железа) прибавляют раствор сульфида аммония; образуется черный осадок, растворимый в разведенных минеральных кислотах.
Открытие закисного железа.
К 2 мл раствора соли закисного железа (около 0,02 г иона железа) прибавляют 0,5 мл разведенной хлористоводородной кислоты и 1 мл раствора феррицианида калия; образуется синий осадок.
Открытие окисного железа.
А. К 2 мл раствора соли окисного железа (около 0,001 г иона железа) прибавляют 0,5 мл разведенной хлористоводородной кислоты и 1-2 капли раствора ферроцианида калия; образуется синий осадок.
Б. К 2 мл раствора соли окисного железа (около 0,001 г иона железа) прибавляют 0,5 мл разведенной хлористоводородной кислоты и 1- 2 капли раствора роданида аммония; появляется красное окрашивание.
§2. Открытие иона цинка, Zn2+
Для обнаружения иона цинка в ГФXI приводятся два метода. В основе первого метода лежит реакция образования сульфида цинка. Осаждение сульфида цинка происходит из растворов, рН которых лежит в зоне 2-9. При рН <2 сульфид цинка не образуется; при рН >9 образуется тетрагидроксоцинкат-ион [Zn(OH)4] 2– В связи с этим неясным является требование ГФ относительно реакции исходного раствора соли цинка (он должен быть нейтральным). Если растворить сульфат цинка в воде, раствор, естественно, будет слабокислым из-за гидролиза соли.
Есть несколько препаратов цинка, нерастворимых в воде, например цинка окись; цинковая соль ундециленовой кислоты, входящая в состав препаратов «Ундецин», «Цинкундан». Перевод цинка в раствор из этих препаратов может быть осуществлен при обработке препаратов либо разведенной хлористоводородной кислотой, либо раствором едкого натра, однако сульфид цинка из полученных растворов не осаждается, поскольку рН их находится вне допустимой зоны. Такие растворы необходимо предварительно нейтрализовать. После этого можно и нужно добавить к предварительно нейтрализованному раствору разведенную уксусную кислоту и далее раствор сероводорода или сульфида натрия.
Второй метод основан на реакции иона цинка с ферроцианидом калия, который образует с ним белый осадок двойной соли гексацианоферрата (II) цинка и калия следующего состава:
3Zn2+ + 2K4[Fe(CN)6] → K2Zn3[Fe(CN)6]2↓ + 6K+
Этот метод удобен тем, что позволяет открыть цинк в сильнокислых растворах. Однако из щелочных растворов цинк не осаждается при действии ферроцианида калия. При действии растворов едких щелочей осадок двойной соли гексацианоферрата (II) цинка и калия растворяется:
K2Zn3[Fe(CN)6]2 + 12OHˉ → 2[Fe(CN)6]4– + 3[Zn(OH)4]2– + 2K+
Выполнение реакций
А. К 2 мл нейтрального раствора соли цинка (0,005-0,02 г иона цинка) прибавляют 0,5 мл раствора сульфида натрия или сероводорода; образуется белый осадок, нерастворимый в разведенной уксусной кислоте и легкорастворимый в разведенной хлористоводородной кислоте.
Б. К 2 мл раствора соли цинка (0,005-0,02 г иона цинка) прибавляют 0,5 мл раствора ферроцианида калия; образуется белый осадок, нерастворимый в разведенной хлористоводородной кислоте.
return false">ссылка скрыта
§3. Открытие ионов серебра, Ag+
При действии сероводорода и сульфида аммония на раствор, содержащий ионы серебра, осаждается черного цвета сульфид серебра Ag2S. Сульфид серебра образуется также при действии сероводорода на металлическое серебро в присутствии кислорода воздуха, но эта реакция протекает очень медленно:
4Ag + 2H2S + О2 = 2Ag2S ↓ + 2H2O.
Из-за очень малой растворимости Ag2S и низкого потенциала системы Ag2S/2Ag сульфид серебра может образоваться также в отсутствие кислорода воздуха:
2Ag + H2S = Ag2S ↓ + H2.
Сульфид серебра не растворяется в растворах сульфидов и полисульфидов щелочных металлов. Не растворяется он и в растворах минеральных кислот, за исключением азотной кислоты:
3Ag2S + 8HNO3 = 6AgNO3 + 2NO + 3S + 4H2O.
Однако вследствие образования комплексных соединений AgSH, Ag(SH)2- и Ag2S(SH)22- растворимость Ag2S в минеральных кислотах заметно увеличивается. Предел обнаружения серебра — 1 мкг. Ионы Cu2+, Hg2+, Bi3+, Sn ( II , IV), образующие сульфиды в сильнокислых растворах, мешают обнаружению серебра.
Хлориды, бромиды и йодиды щелочных металлов. При взаимодействии с ионами серебра они образуют творожистый осадок AgCl, AgBr и Agl белого, бледно-желтого и желтого цвета соответственно. С увеличением концентрации ионов Сl-, Вг- и I- растворимость галогенидов серебра увеличивается из-за образования комплексных соединений.Преимущественно образуются AgX2– и AgX43–в небольших количествах образуются также AgX32–. Хлорид серебра растворяется в растворе аммиака и карбоната аммония, так как в результате кислотно-основных реакций он содержит достаточное количество аммиака:
AgCl + 2NH3= Ag(NH3)2Cl
NH4+ + H2O = NH3+ Н3О+,
СО32– + Н2О = НСО3- + ОН-.
Йодид серебра в NH3 нерастворим, бромид серебра растворяется частично, что находится в соответствии с величинами произведений растворимости. Все галогениды серебра легко растворяются в растворах цианида калия или тиосульфата натрия, так как образующиеся цианидные и тиосульфатные комплексы серебра значительно устойчивее аммиачных.

Рисунок 1. Кристаллы Ag(NH3)2Cl
При медленной кристаллизации из аммиачных растворов выпадает Ag(NH3)2Cl в виде мелких характерных кристаллов — шестиугольников, треугольников и звездочек (рис.1). Предел обнаружения серебра микрокристаллоскопической реакцией - 5 мкг. Свинец и ртуть мешают. При выполнении реакции в пробирке предел обнаружения серебра - 10мкг.
Выполнение реакции.
1. К 1—2 каплям раствора, содержащего ионы серебра, добавляют 1—2 капли 30%-ного раствора уксусной кислоты и 1—2 капли раствора сульфида аммония. Образуется черный осадок сульфида серебра.
2. К 2—3 каплям испытуемого раствора, подкисленного азотной кислотой, добавляют 2—3 капли 2 М раствора НСl. Образуется аморфный белый осадок. Его центрифугируют, промывают водой и обрабатывают 2—3 каплями концентрированного раствора NH3. Каплю полученного раствора помещают на предметное стекло. Через некоторое время после испарения растворителя образуются характерные кристаллы Ag(NH3)2Cl.
Обнаружение катионов ртути (I), Hg1+. Ртуть в степени окисления + 1 существует в виде иона Hg22+.
При добавлении сульфид-иона к раствору, содержащему ионы Hg22+, образуется черный осадок, состоящий из HgS и Hg: Ртуть в степени окисления + 1 существует в виде иона Hg22+.


Поскольку ионы Hg2+ образуют малорастворимые и малодиссоции рованные соединения с большинством лигандов, возможно диспропорционирование Hg22+, как это и наблюдается при взаимодействии с сульфид-ионами. Предел обнаружения ртути - 5 мкг.
При действии аммиака на Hg2Cl2образуется черный осадок, состоящий из Hg и HgNH2Cl или его смеси с Hg2NH2Cl•H2O:

Предел обнаружения ртути — 20 мкг.
Для обнаружения Hg22+ можноиспользовать реакцию образования каломели Hg2Cl2, способной люминесцировать оранжево-красным светом в ультрафиолетовом свете. Предел обнаружения ртути — 0,005 мкг. Реакции не меш ают 200-кратные количест ва Сu, Pb, Ag, Sn (II), Bi. Интенсивность свечения каломели значительно снижается в присутствии Hg (II) , металлической ртути и оксида азота (IV).
Выполнение реакции
1. К 3-4 каплям раствора Hg2(NO3)2добавляют 2-3 капли раствора сульфида аммония. Образуется черный осадок.
2. К 3-4 каплям раствора Hg2(NO3)2добавляют 3—4 капли 2М соляной кислоты. Образуется белый осадок Hg2Cl2. Отцентрифугировав осадок, его обрабатывают 3-4 каплями 25%- ного раствора NH3. Осадок мгновенно чернеет, образуется смесь Hg и HgNH2Cl.
3. Люминесцентная реакция. На предметное стекло наносят каплю раствора, содержащего ионы ртути (I), и каплю 2М раствора НСl. Наблюдают оранжево-красное свечение каломели в ультрафиолетовом свете.
§4. Открытие иона ртути, Hg2+
Обнаружение катиона ртути (II) Hg2+. Ионы ртути (II) [Hg(H2O)]2+ в водных растворах бесцветны. Все соединения ртути (II) сильно ядовиты, поэтому при работе с ними следует принимать меры предосторожности!
Поскольку в медицинской практике находят применение препараты только окисной ртути (Hg2+), в ГФ описаны методы идентификации только ртути окисной. В основе рассматриваемых методов лежат характерные для окисной ртути реакции. Нерастворимые в воде препараты ртути предварительно обрабатывают разведенной хлористоводородной кислотой с целью перевода ртути в ионизированное состояние. При подщелачивании полученного раствора выпадает желтый осадок окиси ртути (II):

При постепенном добавлении к раствору соли окисной ртути раствора калия йодида сначала выпадает красный осадок йодида ртути (II), который при добавлении избытка реактива растворяется с образованием бледно-желтого, почти бесцветного раствора комплексной соли тетрайодмеркуроата калия:

Оба метода высокоспецифичны, просты и надежны в исполнении. Ртутьсодержащие растворы после работы сливают в специально подготовленные склянки.
B кислых растворах (6—7 М НСl) образуют черный осадок сульфида HgS. Имеются три модификации сульфида ртути: красная форма, имеющая искаженную решетку хлорида натрия с зигзагообразными цепями Hg-S- Hg, идентичная минералу киноварь; черная форма, встречающаяся в виде минерала метациннобарита, имеющая структуру цинковой обманки; киноварь, которая образуется при действии тиосульфата натрия на нейтральный раствор хлорида ртути (II).
При медленном пропускании H2S в кислые растворы соли ртути можно наблюдать образование промежуточных продуктов; белого, серого, желтого или буроватого цветов состава HgmClnSx(Hg3Cl2S2). Обычно из кислых растворов солей ртути осаждается сульфид HgS в виде черного осадка. Произведение растворимости HgS(черн) равно 1,5•10-52, однако его растворимость на самом деле значительно больше из-за побочных реакций, протекающих в растворе с образованием соединений H2S, HS-,. Hg(OH)+ и Hg(OH)2. Черный сульфид при нагревании или при действии щелочных растворов полисульфидов превращается в красную форму.
Сульфид ртути растворим в царской водке; в соляной кислоте он растворяется только в присутствии окислителей (например, пероксида водорода) или комплексообразующих ионов. Чувствительность обнаружения ртути с сульфид-ионом зависит от кислотности анализируемого раствора. Например, предел обнаружения ртути в сильнокислых растворах—10 мкг. Из растворов с концентрацией 6—7М НСl вместе со ртутью осаждаются сульфиды мышьяка (V) и меди (II).
Йодид калия при взаимодействии с ионами ртути (II) осаждает красный осадок HgI2. Имеются две модификации иодида ртути (II): красная и желтая. Красная модификация при нагревании до 150°С переходит в желтую. Йодид ртути кристаллизуется в слоистых решетках. Осадок HgI2 растворяется в избытке йодида калия, в растворах тиосульфата или цианида с образованием устойчивых комплексных ионов. В водных растворах ионы Hg2+ с галогенид-, цианид-, тиосульфат-ионами и другими анионами образуют комплексы типа HgX+, HgX2, HgX3-, HgX42-,. При более высоких содержаниях ртути в растворе образуются полиядерные комплексные соединения. Если одновременно в растворе присутствует несколько анионов разных по природе, то образуются смешаннолигандные комплексы HgXnYi, например HgClBr, HgBr2I-, HgI2Br22– и др.
При действии NH3 или ионов аммония и концентрированного раствора щелочи на раствор, содержащий комплексные ионы HgI42–, выпадает характерный красно-бурый осадок:

Эту реакцию под названием реакции Несслера используют для обнаружения Hg2+ и NH4+. Предел обнаружения ртути - 5 мкг.
Реакция с щелочами Hg2+ + 2 ОН– = HgО (желтый) + Н2О. Осадок HgO растворяется в азотной кислоте, в растворах хлоридов и иодидов щелочных металлов с образованием соответственно Hg(NO3)2, HgCl2 и комплекса [HgI4]2–:
HgO + 2 HNO3 — Hg(NO3)2 + H2O
HgO +2 Cl– + H2O - HgCl, + 2 OH–
HgO +4 I– + H2O - [HgI4]2– + 2 OH–
Выполнение реакции.
1. К 2—3 каплям раствора, содержащего ионы ртути ( II) , добавляют 3—4 капли концентрированной НСl и 3—4 капли раствора сульфида аммония. Полученный раствор нагревают в водяной бане. Образуется черный осадок HgS. Осадок центрифугируют, часть его переносят B другую пробирку и растворяют в царской водке. Оставшуюся часть осадка растворяют в смеси НСl и KI.
2. К 1—2 каплям раствора, содержащего ионы ртути (II), добавляют раствор KI по каплям до образования осадка HgI2 и избыток до растворения осадка и образования HgI42–. К полученному раствору добавляют 1—2 капли раствора NH4Cl и 1—2 капли 30%-ного раствора КОН. Образуется красно-бурый осадок.
3. К 4 каплям раствора соли окисной ртути прибавляют 1 каплю едкого натра. Образуется желтый осадок.
§5. Обнаружение катионов марганца (II), Mn2+
Висмутат натрия, оксид свинца (IV), персульфат аммония в азотнокислой среде при нагревании быстро окисляют ионы марганца (II) до марганцевой кислоты НМnО4, имеющей характерную красно-фиолетовую окраску:

Окисление персульфатом аммония проводят в присутствии катализатора ионов серебра (I), которые окисляются персульфатом аммония до ионов серебра (II)

Далее ионы серебра (II) окисляют ионы марганца (II) до перманганат иона, а ионы серебра (I) при этом регенерируются:
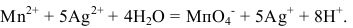
Висмутат натрия окисляет ионы марганца (II) в отличие от других окислителей без нагревания. Обнаружению марганца мешают восстановители, в том числе хлорид-ион и большие количества иона марганца (II) . Предел обнаружения марганца — 2 мкг.
Выполнение реакции
1) К капле раствора нитрата или сульфата марганца прибавляют каплю концентрированной азотной кислоты, 3—4 капли воды и немного твердого висмутата натрия. Раствор окрашивается в малиновый цвет.
2) К 5—6 каплям раствора (NH4)2S2O8 прибавляют каплю 2М раствора H2SO4, 1—2 капли концентрированной Н3РО4 (фосфорная кислота стабилизирует ионы MnO-4 и препятствует их разложению), 1—2 капли раствора AgNO3 и нагревают. В нагретую окислительную смесь вносят при помощи стеклянной палочки минимальное количество раствора, содержащего ионы Mn2+ и не содержащего хлорид-ионы, перемешивают и наблюдают красно-фиолетовую окраску раствора.
§6. Обнаружение катионов меди (II) Сu2+
В ГФ используются следующие методы обнаружения ионов меди (II).
Реакция восстановления меди (II) металлами до металлической меди – Реакцию дают металлы, расположенные в ряду напряжений металлов левее меди.
Cu2+ + Zn = Сu + Zn2+
Сu2+ + Fe = Сu + Fe2+
3 Сu2+ +2 А1 = 3 Сu +2 А13+
Гексацианоферрат (II) калия при рН ≤ 7 осаждает ионы меди в виде красно-бурого осадка Cu2Fe(CN)6, который растворим в аммиаке с образованием аммиакатов меди. Предел обнаружения меди –10 мкг. Проведению реакции мешают ионы Fe3+, Ni2+, Co2+, образующие с реагентом цветные осадки. Поэтому указанные ионы предварительно отделяют или связывают в устойчивые растворимые комплексные соединения. При очень малых концентрациях меди осадок не выпадает, но раствор окрашивается в розовый цвет.
Аммиак при взаимодействии с ионами меди сначала осаждает основные соли переменного состава зеленого цвета, легко растворимые в избытке реагента. При рН >9 образуются аммиачные комплексы меди интенсивно-синего цвета: Cu(NH3)(H2O)52+; Cu(NH3)4(H2O)22+. Предел обнаружения меди — 40 мкг.
Тетрароданомеркуриат (II) аммония в уксуснокислой среде с ионами меди в присутствии ионов цинка образует изоморфные кристаллы фиолетового цвета CuHg(SCN)4 и ZnHg(SCN) 4 (рис. 2). Чтобы эта реакция удалась, необходимо брать очень разбавленный раствор соли меди, иначе вместо фиолетового выделяется желтовато-зеленый осадок CuHg(SCN)4.

Рисунок 2. . Кристаллы CuHg(SCN)4 (a), CuIIg(SCN)4 и ZnHg(SCN)4изоморфные кристаллы (б)
Предел обнаружения меди – 2 мкг. Ионы Fe3+, Co2+, Ni2+ должны отсутствовать, так как они образуют окрашенные соединения с реагентом. Реакцию на медь можно выполнить в пробирке или как микрокристаллоскопическую. На рис. изображены кристаллы соединения CuHg(SCN)4. Если обнаружение меди проводить микрокристаллоскопическим методом с использованием соединения CuHg(SCN)4, можно обнаружить только 5 мкг.
Соляная кислота в присутствии пиридина и 2-пиколина с ионами Сu (I) образует комплексы состава CuPyCl и Сu(Ру)зСl, где Ру – пиридин или пиколин. Это соединение при минус 196°С интенсивно люминесцирует желтым цветом. Ионам Сu (I) , подобно Ag+ и Аu+ (электронная конфигурация nd10), свойственна собственная люминесценция. Она обусловлена электронными переходами между энергетическими уровнями самого иона металла.
Реакцию обнаружения меди по ее люминесценции можно проводить капельным методом на фильтровальной бумаге. Предел обнаружения меди – 0,06 мкг. Не мешают обнаружению меди 100-кратные количества Cd, Co, Zn, Ni, Fe(II, III) , Mn, Cr. Остальные катионы, за исключением Pb2+, Bi3+, Sb(III), в любых количествах не мешают обнаружению меди.
Выполнение реакции
1. К 2—3 каплям раствора, содержащего ионы меди (II) (рН ≤ 7), прибавляют 1—2 капли раствора реагента. Образуется красно-бурый осадок.
2. К 2—3 каплям раствора, содержащего ионы меди ( I I ) , добавляют большой избыток раствора аммиака до рН>9. Появление интенсивно-синего цвета раствора указывает на присутствие меди.
3. А) К 1—2 каплям раствора, содержащего ионы меди (I I ) , на предметном стекле (или в пробирке) прибавляют 2—3 капли 1%-ного раствора ацетата или сульфата цинка и 1—2 капли раствора реагента. Смесь перемешивают стеклянной палочкой. В присутствии меди появляется фиолетовый осадок.
Б) К капле раствора соли меди на предметном стекле прибавляют каплю 30%-ного раствора СН3СООН и каплю раствора реагента. Образуются характерные (в виде игольчатых звездочек) кристаллы желтовато-зеленого цвета CuHg(SCN)4, которые рассматривают под микроскопом.
4. Люминесцентная реакция. На фильтровальную бумагу наносят каплю раствора, содержащего ионы меди ( I I ) , прибавляют каплю 0,06М раствора аскорбиновой кисло ты в насыщенном растворе NaCl или КСl и каплю 0,01 М раствора пиридина (пиколина) в этаноле. Бумагу с влажным пятном пинцетом помещают в сосуд Дьюара с жидким азотом на 20—30с. В ультрафиолетовом свете наблюдают ярко-желтую люминесценцию замороженного пятна.
5. Поместите одну каплю раствора медного купороса на железную или цинковую пластинку. Наблюдайте образование красного налета свободной меди.
§7. Обнаружение катиона кадмия, Cd2+.
Сероводород или сульфиды щелочных металлов при рН~0,5 образуют с ионами кадмия желтый осадок сульфида кадмия. Осадок не растворим в сульфиде и гидроксиде натрия, но растворим в концентрированных соляной и азотной кислотах:


Предел обнаружения кадмия—100 мкг. Мешают ионы металлов, образующие в этих условиях нерастворимые сульфиды Сu2+, Hg2+, Bi3+, Sn(I I, IV), Sb(III, V) и др.
Дифенилкарбазид I в нейтральных и слабокислых растворах образует с ионами кадмия сине-фиолетовое окрашивание или красно- фиолетовый осадок; при этом, по-видимому, образуется комплексное соединение состава II с дифенилкарбазоном, который является продуктом окисления днфенилкарбазида:

Предел обнаружения кадмия — 100 мкг. Мешающее влияние ионов меди ( I I ) , ртути ( I I ) , свинца устраняют йодидом или тиоцианатом.
8-(Бензолсульфониламино)хинолин I или 8-(n-толуолсульфониламино)хинолин II с ионами кадмия при рН~8 образует комплексное соединение III , флуоресцирующее ярко-зеленым светом:

Интенсивность свечения максимальна через 1—2 мин.
Люминесцентную реакцию на кадмий можно проводить в пробирке или на фильтровальной бумаге. Предел обнаружения с I (0,03 мкг) ниже, чем со II (0,05 мкг). Уменьшают интенсивность свечения Fe(II, III ) , Co, Ni, Мп, Сu. Влияние этих катионов устраняют экстракцией соединения кадмия хлороформом. Флуоресцирующие соединения в условиях обнаружения кадмия образует цинк, но интенсивность свечения в 10 раз меньше, чем соединений кадмия.
Тиоцианат аммония (калия) в уксуснокислом растворе при рН4—5 с ионами кобальта (II) образует окрашенные синий цвет комплексные соединения различного состава общей формулы Co (N CS)n(2-n)+ , где n = 1, 2, 3, 4. Кислород содержащие растворители (эфир, ацетон, изоамиловый спирт) экстрагируют темно-синие малоустойчивые комплексы кобальта, по-видимому, состава Co(NCS)42-. Для понижения диссоциации комплексных соединений необходимо вводить большой избыток тиоцианата. Предел обнаружения кобальта — 3 мкг.
Обнаружению кобальта мешают ионы железа (III) , которые с NCS- образуют окрашенные в красный цвет комплексные соединения; различного состава. Комплекс Fe(NCS)3 экстрагируется теми же органическими растворителями, что и комплексы кобальта. Мешающее действие ионов железа (III) устраняют добавление фторид-ионов, образующих с ионами железа (III) бесцветное устойчивое комплексное соединение.
Нитрит калия в уксуснокислом растворе при рН 4—5 образует с ионами кобальта (III) желтый осадок:
Со(СН3СОО)2+7KNO2+2СН3СООН=K3Co(NO2)6+NO+H2O+4CH3COOK.
В разбавленных растворах осадок образуется при нагревании и стоянии. Эта реакция часто используется для отделения кобальта от мешающих ионов. Предел обнаружения кобальта — 0,4 мкг.
Микрокристаллоскопическая реакция основана на образовании (~0,5М НСl) ярко-синих кристаллов малорастворимого соединения CoHg(SCN)4 при действии на раствор соли кобальта (II) раствора тетрароданомеркуриата(II) аммония (рис. ). Предел обнаружения кобальта понижается в присутствии ионов цинка из-за образования из о морфных кристаллов ZnH g(SCN)4 и CoHg(SCN)4. Предел обнаружения кобальта — 0,1 мкг. Многие ионы Аg+, Pb2+, Cd2+, Zn2+, Fe2+, Ni2+, Cu2+, Sn(II) осаждаются реагентом, однако синие розетки или иглы кристаллов соединения кобальта различимы под микроскопом даже в присутствии значительных количеств посторонних ионов. Ионы железа (III) маскируют фторид-ионами.

Рисунок 3. Кристаллы CoHg(SCN)4
Акваионы кобальта (II) октаэдрической структуры [Со(Н2О)6]2+ окрашены в розовый цвет, поэтому разбавленные водные растворы солей кобальта (II) также имеют розовую окраску. Однако при выпаривании водных растворов Со2 их окраска меняется на синюю, характерную для комплексов кобальта (II) тетраэдрической структуры. Соединения Со(П) легко окисляется до соединений Со (III), причем в ряде случаев - уже кислородом воздуха (растворенным в воде), что необходимо ;учитывать при проведении качественных реакций на кобальт (II). В водных растворах кобальт (II) и кобальт (III) присутствуют исключительно в форме комплексных соединений. Комплексы Со(Ш) устойчивее комплексов Со (II).
Выполнение реакции.
1. К 1—2 каплям раствора, содержащего ионы кадмия, прибавляют каплю раствора сульфида натрия, выпадает желтый осадок.
2. На фильтровальную бумагу наносят каплю насыщенного раствора дифенилкарбазида, каплю исследуемого раствора и держат ее 2—3мин над склянкой с концентрированным раствором аммиака, появляется сине-фиолетовое окрашивание. В присутствии мешающих ионов предварительно к насыщенному этанольному раствору реагент добавляют кристаллический KNCS и KI до насыщения. Этим раствором пропитывают фильтровальную бумагу и высушивают. Далее проводят реакцию, как указано выше.
3. Люминесцентная реакция.
1) В пробирке к 2—3 каплям раствора, содержащего ионы кадмия, добавляют 2—3 капли 25%-ного раствора аммиака (рН~8), 3—5 капель 0,01%-ного этанольного (ацетонового) раствора реагента I или II . Через 1—3 мин наблюдают зеленую флуоресценцию в ультрафиолетовом свете. Если необходимо, проводят экстракцию при рН~8, прибавляя к, анализируемому раствору 1 мл хлороформа. Экстрагируют в течение 1—2 мин и наблюдают зеленое свечение экстракта.
2) На фильтровальную бумагу наносят каплю исследуемого раствора, каплю 25%-ного раствора аммиака и каплю 0,01%-ного этанольного (ацетонового) раствора реагента. В ультрафиолетовом свете наблюдают зеленую флуоресценцию образовавшегося пятна.
4. К 2—3 каплям раствора, содержащего ионы кобальта (II), добавляют твердый тиоцианат аммония (калия), твердый фторид аммония, 5—7 капель изоамилового спирта и встряхивают. Слой изоамилового спирта окрашивается в синий цвет.
5. К 2—3 каплям раствора, содержащего ионы кобальта (II), добавляют 2 капли 2 М раствора CH3CОOH, 2 капли раствора ацетата натрия и твердый нитрит калия. Смесь нагревают несколько минут на водяной бане. Образуется желтый осадок.
§8. Обнаружение катиона никеля (II) Ni2+
Диметилглиоксим образует с ионами никеля (II) в интервале рН 5-10 малорастворимое в воде комплексное соединение характерного ало-красного цвета структуры II :
Предел обнаружения никеля – 3,2 мкг.
С диметилглиоксимом образуют комплексные соединения также ионы меди (II) (оранжево-желтого цвета), железа (II) (красноватого цвета), кобальта (II) (коричнево-красного цвета). Устойчивость их комплексных соединений изменяется в ряду Fe<Co<Ni<Cu. Однако диметилглиоксиматы указанных элементов более растворимы в воде, чем соединение никеля. Поэтому малые количества этих элементов не мешают обнаружению никеля. В присутствии же больших количеств ионов Сu2+, Со2+ и Fe2+ обнаружение никеля затруднено . Если предварительно о кислить Fe(II) до Fe(III) и Со(II) до Со (III), никель можно обнаружить в присутствии 200-кратных количеств этих элементов. При обнаружении никеля в аммиачных растворах в присутствии ионов металлов, осаждающихся аммиаком и образующих окрашенные гидроксиды, необходимо добавить цитраты или тартраты для предотвращения выпадения гидроксида.
Аквокомплексы никеля (II)[Ni(H2O)6]2+ окрашены в зеленый цвет, поэтому водные растворы солей никеля (II) имеют зеленую окраску. В растворе никель (II) присутствует только в форме комплексных соединений.
Выполнение реакции .
1) К 1—2 каплям раствора, содержащего ионы никеля (II), добавляют 1—2 капли 1%-ного этанольного раствора диметилглиоксима и 1—2 капли 2 М раствора аммиака. Образуется характерный ало-красный осадок.
2) Обнаружение в присутствии ионов Fe3+, Со2+ и Сu2+. На бумагу, пропитанную диметилглиоксимом, наносят последовательно каплю исследуемого раствора, каплю насыщенного раствора тартрата натрия. Бумагу затем погружают в разбавленный раствор аммиака, где ее осторожно приводят в движение. Окрашенные диметилглиоксиматы кобальта и меди растворяются, на бумаге остается красное пятно диметилглиоксимата никеля.
§9. Обнаружение ионов хрома (III), Cr3+
Пероксид водорода в щелочной среде окисляет Сr(III) до Сr (VI): 
Образуется желтый раствор хромата натрия. При действии на растворы хроматов пероксида водорода в зависимости от условий опыта образуются разнообразные пероксокомплексы хрома, например голубой CrO(O2)2Х (I) (Х - молекулы воды или кислородсодержащего органического растворителя) и фиолетовый, вероятно, состава СrО(О2)2ОН– (II). Эти комплексы имеют форму пентагональной пирамиды с атомом кислорода в вершине

Голубой CrO(O2)2Х образуется при обработке кислого раствора бихромата пероксидом водорода: 
Производные СrО(О2)2ОН- образуются при действии Н2О2 на нейтральные растворы бихроматов: 
В водных растворах пероксидные соединения хрома неустойчивы; они устойчивы в органических растворителях (диэтиловом эфире, амиловом спирте и др.):


Предел обнаружения хрома - 10 мкг. Реакция селективна для хрома. Ванадий мешает обнаружению хрома при отношении V:Cr =5:l.
Этилендиаминтетраацетат натрия (ЭДТА) I с ионами хрома (III) при рН 4—5 образует комплексное соединение фиолетового цвета состава CrY–, где Y4– — анион ЭДТА, со структурой II

При комнатной температуре реакция идет очень медленно, так как аквакомплексы хрома Сr(Н2О)6инертны. Период полуобмена молекул воды τ1/2 в гексааквакомплексах хрома равен 50ч. При нагревании скорость реакции образования комплексов хрома с ЭДТА увеличивается. При рН 7-9 образуются комплексы состава Cr(OH)Y2– и фиолетовая окраска комплекса CrY– при подщелачивании раствора переходит в синюю:

Окрашенные комплексные соединения ЭДТА образует с катионами, обладающими хромофорными свойствами (Fe3+, Cu2+ , Co2+ , Ni2+ ), поэтому они могут мешать обнов. Затем добавляют 1каплю 30%-ного или 6—8 капель 3%-ного раствора пероксида водорода и нагревают. Образуется желтый раствор хромата. К части полученного раствора после охлаждения добавляют 1 каплю 3%-ного раствора пероксида водорода, несколько капель эфира и по каплям при встряхивании серную кислоту (1:4). Образующееся пероксидное соединение хрома экстрагируется эфиром, эфирный слой окрашивается в синий цвет.
2. К 3-4 каплям раствора, содержащего ионы хрома (III), добавляют 3-5 капель 30%-ного раствора уксусной кислоты, 12-15 капель 5%-ного раствора ЭДТА (избыток ЭДТА обязателен), проверяют рН раствора (рН 4-5) и нагревают в водяной бане. В присутствии хрома (III) появляется фиолетовое окрашивание.
Лабораторное заняие 12
Итоговая контрольная работа № 2
1. Каким требованиям должны удовлетворять общие реакции на подлинность лекарственных веществ?
2. Висмута нитрат основной легкорастворим в концентрированной азотной кислоте. Можно ли открыть висмут в этом растворе реакцией с сероводородом?
3. Йодид висмута черного цвета легкорастворим в растворе йодида калия с образованием желто-оранжевого раствора. Объясните это явление.
4. Препараты железа (II) сульфата могут содержать примесь железа (III) сульфата, который всасывается из желудочно-кишечного тракта гораздо хуже, чем железа (II) сульфат, что снижает эффективность препарата. Предложите метод определения примеси железа (III) сульфата в препаратах железа (II) сульфата.
5. Общей реакцией подлинности на железо нельзя открыть его в препарате «Железо восстановленное» без предварительной минерализации препарата. Предложите методику минерализации препарата и подходящую общую реакцию подлинности на железо, приемлемую для последующего его открытия.
6. С какой целью при открытии иона калия к реакционной смеси добавляют спирт?
7. Предложите методику открытия кальция в препарате «бепаск».
8. С какой целью при открытии магния к реакционной смеси добавляют хлорид аммония? Можно ли вместо хлорида аммония использовать сульфат аммония?
9. Предложите методику открытия ртути в препарате «ртути окись желтая».
10. Ртути окись желтая практически нерастворима в воде, но легко растворяется в растворе йодида калия. Объясните это явление.
11. Сульфат цинка с желтой кровяной солью образует осадок, а с красной кровяной солью не реагирует. Однако, если к раствору, содержащему сульфат цинка и красную кровяную соль, добавить калия йодид, образуется тот же осадок и йод. Объясните это явление.
12. Каким методом отличают арсенаты от арсенитов?
13. Напишите уравнение реакции бромида калия с хлорамином, лежащую в основе общей реакции подлинности на бромид-ион.
14. Можно ли использовать указанную выше реакцию для открытия брома в бромкамфоре?
15. Как можно отличить хлорид серебра от бромида серебра?
16. Напишите уравнение реакции йодида калия с нитритом натрия в присутствии разведенной серной кислоты.
17. Как химическими методами отличить карбонат натрия от гидрокарбоната натрия?
18. Можно ли идентифицировать нитрит натрия и нитрат натрия при их совместном присутствии?
19. Какие соединения мешают открытию фосфат-иона по реакции с молибдатом аммония в азотной кислоте?
20. Предложите методы, позволяющие отличить калия хлорид от калия бромида