Горючее – сложное вещество с известным элементным составом
Состав таких веществ выражается в массовых долях (w, %) каждого элемента. При горении кислород воздуха расходуется на окисление углерода С, водорода Н, серы S и других горючих составляющих.
Рассчитаем, какой теоретический объем воздуха необходим для сгорания 1 кг каждого элемента при нормальных условиях.
1 кг х м3
С + (О2 + 3,76N2) = СО2 + 3,76N2
12 кг 4,76×22,4 м3
Vв(С)теор = х = 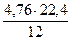 = 8,885 м3 – объем воздуха для сгорания 1 кг углерода.
= 8,885 м3 – объем воздуха для сгорания 1 кг углерода.
1 кг х м3
Н + 0,25(О2 + 3,76N2) = 0,5Н2О + 0,25×3,76N2
1 кг 0,25×4,76×22,4 м3
Vв(Н)теор = х = 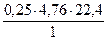 = 26,656 м3 – объем воздуха для сгорания 1 кг водорода.
= 26,656 м3 – объем воздуха для сгорания 1 кг водорода.
1 кг х м3
S + (О2 + 3,76N2) = SО2 + 3,76N2
32 кг 4,76×22,4 м3
Vв(S)теор = х = 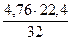 = 3,332 м3 – объем воздуха для сгорания 1 кг серы.
= 3,332 м3 – объем воздуха для сгорания 1 кг серы.
Углерод, водород и сера являются основными составляющими большинства органических соединений. Значительное число органических веществ имеют в своем составе кислород, и, следовательно, воздуха на горение будет затрачено меньше.
Рассчитаем объем воздуха, в котором содержится 1 кг кислорода.
32 кг О2 - 4,76×22,4 м3 воздуха
1 кг - х м3
Vв(О)теор = х = 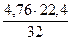 = 3,332 м3 – объем воздуха, содержащий 1 кг кислорода.
= 3,332 м3 – объем воздуха, содержащий 1 кг кислорода.
Сопоставим полученные значения.
Vв(Н)теор : Vв(С)теор : Vв(S)теор :Vв(О)теор =
= 26,665 : 8,885 : 3,332 : 3,332 = 1 : 1/3 : 1/8 : 1/8
Теоретическое количество воздуха для сгорания 1 кг вещества сложного элементного состава в общем виде можно записать следующим образом:
Vвтеор = Vв(С)теор × 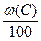 + Vв(Н)теор ×
+ Vв(Н)теор ×  + Vв(S)теор ×
+ Vв(S)теор ×  - Vв(О)теор ×
- Vв(О)теор × 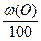 , м3 (7)
, м3 (7)
где
w (С), w (Н), w (S), w (О) – массовые доли элементов в веществе, %.
После подстановки в формулу (7) полученных выше расчетных значений теоретический объем воздуха для сгорания заданной массы (m)вещества сложного элементного состава при нормальных условиях определяется по формуле:
Vвтеор =m ×0,267 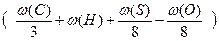 , м3/кг. (8)
, м3/кг. (8)
| Расчет объема воздуха, необходимого для горения вещества сложного элементного состава | Пример 4. Определить объем воздуха, необходимого для полного сгорания 5 кг торфа следующего состава (в %): С – 56,4 %, Н – 5,04 %, О – 24,0 %, S – 0,06 %, N – 3,6 %, зола – 10,9 %. Горение протекает при a = 1,5, условия нормальные. |
1. По формуле (8) определяем теоретический объе воздуха, необходимый для горения данной массы образца торфа:
Vвтеор = 5 ×  = 27,7 м3
= 27,7 м3
2. С учетом коэффициента избытка воздуха реально на сгорание данной массы образца торфа будет затрачено воздуха
Vвпр = Vвтеор × a = 27,7 × 1,5 = 41,6 м3.