Электролитическая диссоциация
Теоретические основы. Вещества, которые в расплавах или растворах полярных растворителей диссоциируют на ионы, называются электролитами: Na2CO3  2 Na+ + CO3
2 Na+ + CO3 
Процесс диссоциации количественно характеризуют степенью диссоциации: a =  ,
,
где n - количество вещества, С - концентрация.
Если степень диссоциации электролита a > 30%, то такой электролит называется сильным. К сильным электролитам относятся соли, сильные кислоты (HCl, H2SO4, HNO3, HClO4 и некоторые другие), щелочи (основания щелочных и щелочноземельных металлов NaOH, KOH, RbOH, CsOH, FrOH, Ca(OH)2, Sr(OH)2, Ba(OH)2). Диссоциация сильных электролитов протекает необратимо и в одну стадию. Например:
Al2(SO4)3  2 Al3+ + 3 SO4
2 Al3+ + 3 SO4 
Если степень диссоциации электролита a < 3%, то электролит называют слабым. К слабым электролитам относятся молекулы воды, гидроксида аммония NH4OH, слабых кислот и оснований. Диссоциация слабых электролитов - процесс обратимый и ступенчатый, для него устанавливается состояние химического равновесия, которое характеризуется константой равновесия - константой диссоциации.
Например, диссоциация фосфорной кислоты - трехступенчатый процесс:
1 ступень: H3PO4  H+ + H2PO4
H+ + H2PO4 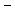 ; K1 =
; K1 = 
2 ступень: H2PO4 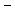
 H+ + HPO4
H+ + HPO4  ; K2 =
; K2 = 
3 ступень: HPO4 
 H+ + PO4
H+ + PO4  ; K3 =
; K3 = 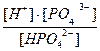
 |
H3PO4  3H+ + PO4
3H+ + PO4  ; K =
; K = 
[H+], [H2PO4 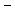 ], [HPO4
], [HPO4  ], [PO4
], [PO4  ], [H3PO4] - равновесные концентрации ионов;
], [H3PO4] - равновесные концентрации ионов;
К1, К2, К3 - ступенчатые константы диссоциации;
К - общая константа диссоциации.
Добавление в раствор слабых электролитов одноименных ионов вызывает смещение равновесия реакции диссоциации в сторону ее уменьшения (эффект одноименного иона).
Обменные реакции в растворах происходят между ионами сильных электролитов и молекулами слабых электролитов. Равновесие реакций обмена в растворах смещено в сторону образования осадков, газов, молекул слабых электролитов.
В ионном виде реакции обмена записывают следующим образом: сильные растворимые в воде электролиты пишут в виде ионов; слабые электролиты, осадки и газы записывают в виде молекул:
2NaNO2 + H2SO4  Na2SO4 + 2HNO2
Na2SO4 + 2HNO2
растворимая сильная растворимая слабая
в воде соль кислота в воде соль кислота
(реакция в молекулярном виде)
2Na+ + 2NO2 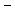 + 2H+ + SO42
+ 2H+ + SO42 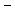
 2Na+ + SO42
2Na+ + SO42 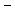 + 2HNO2
+ 2HNO2
(полное ионное уравнение реакции)
2NO2 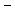 + 2H+
+ 2H+  2HNO2
2HNO2
(сокращенное ионное уравнение реакции)
Свойства химических соединений в растворах определяются характером их диссоциации:
HCl  H+ + Cl
H+ + Cl 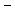 (кислоты при диссоциации дают ионы Н+);
(кислоты при диссоциации дают ионы Н+);
NaOH  Na++OH
Na++OH 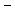 (основания при диссоциации дают ионы ОН
(основания при диссоциации дают ионы ОН 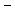 );
);
NaCl  Na++Cl
Na++Cl 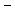 (cоли при диссоциации дают катионы металлов и анионы кислотных остатков).
(cоли при диссоциации дают катионы металлов и анионы кислотных остатков).
Существуют электролиты, которые могут участвовать в химических реакциях как в роли основания, так и в роли кислоты. Такие электролиты называются амфотерными. К ним относятся оксиды и основания некоторых металлов: цинка, алюминия, свинца, олова, хрома(III) и некоторых других. Эти оксиды и основания способны реагировать как с кислотами, так и с основаниями, образуя в качестве продуктов реакции соли:
Al(OH)3 + 3HCl  AlCl3 + 3H2O
AlCl3 + 3H2O
Al(OH)3 + NaOH  NaAlO2 + 2H2O
NaAlO2 + 2H2O
Al(OH)3 + 3NaOH  Na3[Al(OH)6]
Na3[Al(OH)6]
Sn(OH)2 + 2HCl  SnCl2 + 2H2O
SnCl2 + 2H2O
Sn(OH)2 + 2NaOH  Na2SnO2 + 2H2O
Na2SnO2 + 2H2O
Sn(OH)2 + 2NaOH  Na2[Sn(OH)4]
Na2[Sn(OH)4]
Цель работы. Изучить реакции, идущие в растворах электролитов.
Порядок работы.
Опыт 1. Ионизирующее действие воды
В сухой пробирке перемешайте небольшие количества кристаллических карбоната натрия Na2CO3 и щавелевой кислоты H2C2O4. Идет ли реакция? Добавьте 2 мл дистиллированной воды. Запишите наблюдения.
Опыт 2. Реакции с образованием осадков
В отдельные пробирки налейте по 2 мл растворов: а) серной кислоты; б) сульфата какого-либо металла. В каждую пробирку добавьте 2-3 капли раствора хлорида бария. Запишите наблюдения.
Опыт 3. Реакции с образованием газов
В отдельные пробирки налейте по 2 мл растворов: а) карбоната калия; б) карбоната натрия. Добавьте в каждую пробирку 3-4 капли разбавленной соляной кислоты. Запишите наблюдения.
Опыт 4. Сильные и слабые электролиты
В отдельные пробирки налейте по 2 мл разбавленных растворов: а) соляной кислоты; б) уксусной кислоты. В каждую пробирку положите по грануле цинка. Сравните интенсивность выделения газа в двух пробирках.
Опыт 5. Ослабление диссоциации слабого электролита
(эффект одноименного иона)
а). В пробирку налейте 4 мл разбавленной уксусной кислоты и добавьте 2 капли метилоранжа. Отлейте половину раствора в другую пробирку и добавьте в нее несколько кристаллов ацетата натрия. Сравните цвет растворов в пробирках.
б). В пробирку налейте 4 мл разбавленного водного раствора аммиака и добавьте 2 капли фенолфталеина. Отлейте половину раствора в другую пробирку и добавьте в нее несколько кристаллов хлорида аммония. Сравните цвет растворов в пробирках.
Опыт 6. Амфотерные основания
В пробирку налейте 3 мл раствора хлорида цинка. Осторожно добавьте 2 капли раствора гидроксида натрия до образования осадка гидроксида цинка. Разделите осадок на 2 части и испытайте его растворимость в соляной кислоте и гидроксиде натрия. Запишите наблюдения.
Форма лабораторного отчета.
1. Название лабораторной работы.
2. Краткое описание, цель работы.
3. Номер и название опыта.
4. Уравнение реакции: а) в молекулярной форме; б) в полной ионной форме; в) в сокращенной ионной форме.
5. Наблюдения.
6. Обсуждения.
7. Выводы.
Типовые задачи.
1. Напишите уравнения реакций диссоциации следующих электролитов: AlCl3, H2SO3, NaHCO3. Для обратимых процессов запишите выражения константы равновесия.
2. Вычислите концентрацию ионов водорода в 0,1 М растворе соляной кислоты, если степень ее диссоциации равна 98%.
3. Закончите уравнения реакций, расставьте коэффициенты, запишите уравнения в ионно-молекулярной и сокращенной форме:
| а) AgNO3 + BaCl2 ® | б) Ca(OH)2 + HCl ® |
| в) Na2SO3 + H2SO4 ® | г) CaCO3 + HNO3 ® |
| д) K2SO4 + NaOH ® | e) Pb(OH)2 + KOH ® |
| ж)Al2(SO4)3+NaOH(изб.)® | з) AgNO3 + H2S ® |
4. Вычислите ионную силу раствора, содержащего смесь 0,01 М AlCl3 и 0,1 М Na2SO4.
5. Вычислите ионную силу раствора, содержащего смесь 0,01 М Cr2(SO4)3 и 1М NaCl.
6. Вычислите активность ионов Са2+ в 0,1 М растворе СаСl2.
7. Вычислитеь активность ионов Nа+ в 0,1 М растворе Nа3PO4.