Неэлектролитов
551. Сколько граммов сахара содержится в 250 см3 раствора, осмотическое давление которого при температуре 7 °C составляет 283,6 кПа? Вычислите молярность раствора.
Ответ: 10,42 г; 0,12 М.
552. Сколько граммов глюкозы следует растворить в 260 г воды для получения раствора, температура кипения которого превышает температуру кипения чистого растворителя на 0,05°?
Ответ: 4,5 г.
553. Вычислите давление пара раствора, в 468 г которого содержится 18 г глюкозы при температуре 25 °C. Давление насыщенного водяного пара при температуре 25 °C составляет 3167,7 Па.
Ответ: 3155,03 Па.
554. Определите молекулярную массу эфира, если при температуре 30 °C давление пара раствора, содержащего 3,08 г анилина в 370 г эфира, равно 85 792 Па, а давление пара растворителя при той же температуре составляет 86 365 Па.
Ответ: 74,39 г/моль.
555. Температура кипения ацетона равна 56,1 °C (Кэ = = 1,73 (К · кг/моль)). Вычислите температуру кипения 8 %-ного раствора глицерина в ацетоне.
Ответ: 57,74 °C.
556. Вычислите температуру кипения и температуру замерзания водного раствора фруктозы с массовой долей 5 % мас. (Кэ = = 0,52 (К · кг/моль); Кк = 1,86 (К · кг/моль)).
Ответ: 100,15 °C; –0,54 °C .
557. Вычислите давление насыщенного пара над раствором при температуре 20 °C, если раствор содержит 6,4 г нафталина (С10Н8) и 90 г бензола (С6Н6). Давление насыщенного пара над чистым бензолом при данной температуре составляет 9953,82 Па.
Ответ: 9522,49 Па.
558. Рассчитайте молярную массу неэлектролита, если 28,5 г этого вещества, растворенного в 785 г воды, вызывают понижение давления пара воды над раствором на 52,37 Па при температуре 25 °C. Давление пара над чистой водой принять равным 7375,9 Па.
Ответ: 92 г/моль.
559. Осмотическое давление раствора, в 250 мл которого содержится 0,66 г мочевины, равно 111,1 кПа при температуре 33 °C. Вычислите молярную массу мочевины.
Ответ: 60,45 г/моль.
560. Давление пара эфира при температуре 30 °C равно 8,64 · 104 Па. Какое количество (моль) неэлектролита надо растворить в 50 моль эфира, чтобы понизить давление пара при данной температуре на 2666 Па?
Ответ: 0,015 моль.
561. Раствор, состоящий из 9,2 г глицерина (С3Н8О3) и 400 г ацетона, кипит при температуре 56,38 °C. Чистый ацетон кипит при температуре 56 °C. Вычислите эбуллиоскопическую константу ацетона.
Ответ: 1,52 К · кг/моль.
562. Определите криоскопическую постоянную воды, если известно, что водный раствор с концентрацией неэлектролита 0,001 моль/кг замерзает при температуре –0,00186 °C.
Ответ: 1,86 К · кг/моль.
563. Определите осмотическое давление раствора сахарозы при 0 °C, если при 20 °C осмотическое давление этого же раствора равно 1,066 · 105 Па.
Ответ: 99,32 кПа.
564. Вычислите молярную концентрацию раствора сахара С12Н22О11, который при температуре 27 °C имеет осмотичес-
кое давление, равное 1,56 · 105 Па, и замерзает при температуре
-0,119 °C.
Ответ: 0,063 М.
565. Осмотическое давление раствора, в 0,25 л которого содержится 0,66 г мочевины, равно 111 439 Па при температуре 33 °С. Вычислите молекулярную массу мочевины. Сколько граммов мочевины следует растворить в 75 г воды, чтобы температура кристаллизации понизилась на 0,465 °С (Кк = 1,86 К · г/ моль)?
Ответ: 60,27 г/моль; 1,13 г.
566. Вычислите массовую процентную концентрацию водного раствора глицерина, зная, что этот раствор кипит при температуре 100,39 °С.
Ответ: 6,45 % мас.
567. Вычислите температуру кристаллизации 2 %-ного раствора этилового спирта, зная, что Кк = 1,86 К · кг/моль.
Ответ: –0,83 °C.
568. Массовая доля неэлектролита в водном растворе 63 % мас. Рассчитайте молекулярную массу этого неэлектролита, если при температуре 20 °С давление водяного пара над раствором равно 1399,4 Па. Давление паров воды при данной температуре равно 2335,42 Па.
Ответ: 76,47 г/моль.
569. Для предотвращения замерзания в зимнее время к водным растворам добавляют глицерин. Допустив, что закон Рауля применим к подобным растворам, вычислите, сколько граммов глицерина нужно прибавить к 100 г воды, чтобы раствор не замерзал при –5 °С?
Ответ: 24,73 г.
570. Рассчитайте молярную массу неэлектролита, если 28,5 г этого вещества, растворенного в 785 г воды, вызывают понижение давления пара воды над раствором на 52,37 Па при температуре 25 °С. Давление пара над чистым растворителем при этой температуре равно 7375,9 Па.
Ответ: 92,04 г/моль.
571. Для приготовления 30 л антифриза взято 9 л глицерина (С3Н8О3). Чему равна температура замерзания приготовленного антифриза? Плотность глицерина 1261 кг/м3.
Ответ: –7,09 °C.
572. Давление пара над раствором, содержащим 5,2 г некоторого вещества в 117 г воды, при температуре 70 °С равно 3,07 · 105 Па. Определите молярную массу вещества.
Ответ: 54,54 г/моль.
573. При химическом анализе сталей навеску металла растворяют и селен выделяют из раствора экстракцией смесью циклогексанола и пентанола. Давление пара пентанола при 20 °С равно 5 мм рт. ст. Понижение давления пара 20 %-ного раствора циклогексанола С6Н12О в пентаноле равно 0,9 мм рт. ст. Чему равна молярная масса пентанола (давлением циклогексанола пренебречь)?
Ответ: 88 г/моль.
574. Водные растворы перекиси водорода применяют в гидрометаллургии редких металлов в качестве окислителей, устойчивых при низких температурах. Определите температуру замерзания раствора, содержащего 0,0509 г Н2О2 в 18,789 г воды, если Кк = 1,86 К · кг/моль.
Ответ: –0,151 °C.
575. Расплав, содержащий 0,2976 г Hg2Cl2 в 50 г HgCl2, плавится на 0,43 °C ниже, чем чистая двухлористая ртуть (264,5 °C). Определите криоскопическую постоянную HgCl2.
Ответ: 19,58  .
.
576. Вычислите количество этиленгликоля (С2Н6О2), которое необходимо прибавить на каждый килограмм воды для приготовления антифриза с точкой замерзания –15 °С.
Ответ: 8,07 моль.
577. Определите температуру затвердевания сплава железа с кремнием, если сплав содержит 14,5 % мас. кремния. Температура затвердевания чистого железа равна 1530 °С, а криоскопическая постоянная железа составляет 13,18  .
.
Ответ: 1610 °C.
578. Определите массовое соотношение между марганцем и железом в сплаве, если понижение температуры затвердевания железа в данном сплаве составляет 4 К, а криоскопическая постоянная железа равна 13,18  .
.
Ответ:  .
.
579. Какова температура плавления сплава железа с углеродом, если сплав содержит 6 % мас. углерода? Температура плавления чистого железа равна 1530 °С, а криоскопическая постоянная железа 13,18  .
.
Ответ: 1600 °C.
580. Температура замерзания олова 231,61 °С. Криоскопическая постоянная олова равна 34,61  . При растворении 1,5163 г меди в 440 г олова температура затвердевания расплава понизилась до 229,69 °С. Вычислите молярную массу меди в расплаве.
. При растворении 1,5163 г меди в 440 г олова температура затвердевания расплава понизилась до 229,69 °С. Вычислите молярную массу меди в расплаве.
Ответ: 62,12 г/моль.
581. Раствор камфоры массой 0,552 г в 17 г эфира кипит при температуре на 0,461° выше, чем чистый эфир. Эбуллиоскопическая константа эфира – 2,16. Определите молекулярную массу камфоры.
Ответ: 151,16 г/моль.
582. Раствор, приготовленный из 2 кг этилового спирта и 8 кг воды, залили в радиатор автомобиля. Вычислите температуру замерзания раствора.
Ответ: –10,11 °C.
583. Определите массу воды, которую следует взять для растворения сорбита (С6Н8(ОН)6) массой 5 г, для получения раствора, замерзающего при температуре –0,2 °C.
Ответ: 255 г.
584. Некоторые фосфоросодержащие материалы перерабатывают хлорированием газообразным хлором. При этом получают оксохлорид фосфора POCl3, содержащий примеси. Определите молекулярную массу трихлорида железа, если раствор, состоящий из 2,06 г трихлорида железа и 80 г POCl3, затвердевает при температуре 0,7 °С. Температура плавления чистого POCl3 равна 1,3 °С, криоскопическая постоянная оксохлорида фосфора равна 7,57 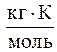 .
.
Ответ: 324 г/моль.
585. Чему равна температура затвердевания раствора 1,4 г трихлорида алюминия в 55 г POCl3, если температура плавления чистого POCl3 равна 1,3 °С, криоскопическая постоянная оксохлорида фосфора равна 7,57 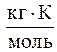 , а молекула трихлорида алюминия в растворе димерна (Al2Cl6)?
, а молекула трихлорида алюминия в растворе димерна (Al2Cl6)?
Ответ: 0,57 °С.
586. Осмотическое давление раствора, в 250 мл которого содержится 2,3 г растворенного неэлектролита, при 27 °С равно 249 кПа. Вычислите молярную массу растворенного вещества.
Ответ: 92,16 г/моль.
587. Давление пара воды при 28 °С составляет 3780 Па. Сколько граммов сахара следует растворить в 720 г воды для получения раствора, давление пара которого на 18,7 Па меньше давления пара воды? Вычислите процентное содержание сахара в растворе.
Ответ: 67,68 г; 8,59 %.
588. При температуре 0 °С давление пара эфира С4Н10О составляет 2465 Па. Найдите для этой температуры давление пара 10 %-ного раствора бензойной кислоты С6Н5СООН в эфире.
Ответ: 2298,87 Па.
589. Давление пара воды при 10 °С составляет 1228 Па. В каком количестве воды следует растворить 23 г глицерина для получения раствора, давление пара которого составляет 1200 Па при той же температуре?
Ответ: 197,34 г.
590. Сколько моль неэлектролита растворено в 2 кг воды, если раствор замерзает при температуре –0,93 °С?
Ответ: 1 моль.
591. Понижение давления пара над раствором, содержащим 0,4 моль анилина в 3,04 кг сероуглерода, при некоторой температуре равно 1003,7 Па. Давление пара сероуглерода при той же температуре равно 1,0133 · 105 Па. Вычислите молекулярную массу сероуглерода.
Ответ: 76 г/моль.
592. Определите моляльность водного раствора неэлектролита, кипящего при той же температуре, что и раствор, содержащий 8,6 г другого неэлектролита (М = 344 г/моль) в 250 г воды.
Ответ: 0,1 моль/кг.
593. Чему равно осмотическое давление 5 %-ного водного раствора глюкозы (ρ = 1,02 г/мл) при 310 К, который используется для внутривенных вливаний при кровопотерях? Будет ли этот раствор изотоничен плазме крови (Росм. плазмы крови = 730 кПа)?
Ответ: 730 кПа; да.
594. Чему равно осмотическое давление раствора с массовой долей глицерина 1 % мас. (ρ = 1,0006 г/мл)? Будет ли этот раствор изотоничен раствору с осмотическим давлением 500 кПа?
Ответ: 268 кПа; нет.
595. При 10 °C давление пара воды равно 1227,8 Па. В какой массе воды надо растворить 16 г СН3ОН, чтобы понизить давление пара до 1200 Па?
Ответ: 397,5 г.
596. Водный раствор кипит при 374 К. Чему равно внешнее давление, если давление пара воды при этой температуре равно 787,5 мм рт. ст., а мольная доля нелетучего растворенного вещества равна 0,05?
Ответ: 748,1 мм рт. ст.
597. Определите атмосферное давление, если раствор 51,3 г сахара в 120 г воды закипает при 99,5 °С. Давление пара чистой воды при данной температуре равно 99 540 Па.
Ответ: 97 350 Па.
598. Давление паров чистых веществ А и В при некоторой температуре равно, соответственно, 350 и 760 мм рт. ст. Определите общее давление над смесью, полученной путем смешения 0,5 моль А с 1,5 моль В.
Ответ: 657,5 мм рт. ст.
599. Бензол и толуол образуют идеальный раствор. При 30 °С давление пара чистого бензола равно 120,2 мм рт. ст., а чистого толуола – 40 мм рт. ст. Определите общее давление пара над раствором, полученным путем смешения 100 г бензола с 2,5 моль толуола.
Ответ: 67,2 мм рт. ст.
600. Определите атмосферное давление, если раствор 6,4 г нафталина в 117 г бензола закипает при 80 °С. Давление пара чистого бензола при указанной температуре 100 500 Па.
Ответ: 97 258 Па.