ГЕННАЯ ИНЖЕНЕРИЯ
методические указания
к проведению практических занятий
для студентов IV курса
специальности 080401.65 «Товароведение и экспертиза товаров»
(в области таможенной деятельности)
АСТРАХАНЬ, 2011
Составитель:
Афанасьев В.Е., к.б.н., доцент преподаватель кафедры «Прикладная биология и микробиология»
Рецензент:
Цибизова М.Е., к.т.н., зав. кафедрой «Пищевая биотехнология и технология продуктов питания»
Генная инженерия: методические указания к проведению практических занятий для студентов IV курса специальности 080401.65 «Товароведение и экспертиза товаров» (в области таможенной деятельности) / АГТУ; Сост.: В.Е. Афанасьев — Астрахань, 2011. — 56 с.
Методические указания к проведению практических занятий по дисциплине «Генная инженерия» для IV курса специальности 080401.65 «Товароведение и экспертиза товаров» (в области таможенной деятельности).
Данные методические указания содержат описания методов, используемых для создания гибридных ДНК, введения их в реципиентные клетки, при скрининге клонов, секвенировании и амплификации ДНК. Приведен список вопросов, предусмотренных рабочей программой дисциплины «Генная инженерия» для самостоятельного изучения студентами, вопросы итогового контроля и список литературы, рекомендуемой для освоения курса.
Методические указания утверждены на заседании методического совета по специальности 080401.65 «Товароведение и экспертиза товаров» (в области таможенной деятельности) «29» 04. 2011 г., протокол № 11.
© Астраханский государственный технический университет
СОДЕРЖАНИЕ
Введение…………………………………………………………………………….4
Методы конструирования рекомбинантных ДНК in vitro ……………………... 5
Методы введения рекомбинантных ДНК в клетки ……………………………... 9
Методы идентификации клонов, содержащих рекомбинантные ДНК ………... 13
Методы секвенирования ………………………………………………………….. 17
Амплификация последовательности ДНК in vitro ……………………………… 20
Генетически модифицированные микроорганизмы и их использование……... 23
Получение трансгенных растений, устойчивых к неблагоприятным факторам внешней среды…………………………………………………………………….. 26
Получение трансгенных растений с улучшенными пищевыми свойствами….. 32
Конструирование трансгенных растений – продуцентов целевых белков……. 36
Создание и применение трансгенных животных………………………………... 41
Генотерапия………………………………………………………………………... 44
Краткий словарь терминов………………………………………………………... 47
Вопросы для самостоятельного изучения……………………………………….. 53
Вопросы итогового контроля……………………………………………………... 54
Список рекомендуемой литературы……………………………………………… 56
ВВЕДЕНИЕ
Генная инженерия(синонимы: генетическая инженерия, ДНК-технологии)– это отрасль биологической технологии, задачей которой является конструирование in vitro новых молекулярных генетических систем и последующее встраивание их в геномы организмов. Иными словами, методами генной инженерии в лабораторных условиях генетический материал из одного организма (который принято называть источником или донором генов) переносится в другой организм (называемый хозяином или реципиентом). Целью данных манипуляций является получение организмов с новыми заданными полезными для человека генетически обусловленными свойствами.
Перенос генов методами генной инженерии дает возможность преодолевать межвидовые барьеры и осуществлять передачу отдельных наследственных признаков от одних организмов другим, не родственным им (например, от животных бактериям), чего нельзя достичь методами традиционной селекции.
Вне зависимости от применяемых конкретных методов, типовой генноинженерный эксперимент можно представить в виде последовательности из четырех этапов:
1) получение фрагмента (или смеси фрагментов) ДНК путем расщепления исходной молекулы с помощью специфических ферментов – эндонуклеаз рестрикции (рестриктаз);
2) конструирование in vitro рекомбинантных молекул ДНК, состоящих из фрагментов, полученных на первом этапе, и небольших автономно реплицирующихся в клетке-реципиенте структур (плазмид, фагов, вирусов), носящих название векторов;
3) введение рекомбинантных молекул ДНК в клетку-реципиент;
4) отбор клонов, несущих нужную рекомбинантную молекулу.
Важнейшим источником донорских молекул ДНК, используемых в генной инженерии, являются фрагменты генетического материала различных организмов. Вторым источником могут быть двунитевые дезоксирибонуклеиновые кислоты, полученные на основе однонитевой ДНК комплементарной мРНК эукариотических организмов (дн-кДНК). Подобные копии применяются для экспрессии в бактериях важных с медицинской точки зрения белков человека и животных. Третий источник – искусственные молекулы ДНК, полученные путем химико-ферментативного синтеза.
Практическое занятие №1
Тема: Методы конструирования рекомбинантных ДНК in vitro
Конструирование рекомбинантных молекул ДНК, независимо от выбранного метода, сводится к следующим задачам:
1) Получение целевого фрагмента (или смеси фрагментов) ДНК путем разрезания с помощью рестриктаз молекулы ДНК, выделенной из конкретного организма.
2) Разрезание векторной молекулы с помощью рестриктазы в определенном участке (сайте рестрикции).
3) Вставка и последующее вшивание целевого фрагмента ДНК в вектор в месте разреза.
Впервые подобная операция была произведена в 1972 г. группой американских генетиков из Стенфордского университета под руководством Пола Берга. Ими была получена in vitro гибридная молекула, состоящей из ДНК вируса SV40 и ДНК фага λdvgal. Использованный при этом алгоритм действий получил название коннекторного метода. В 1980 г. за свое открытие Пол Берг был удостоен Нобелевской премии в области химии.
Принцип коннекторного метода (см. рис. 1). К 3'-концам одного из рекомбинируемых in vitro фрагментов ДНК с помощью фермента терминальная трансфераза достраивают одноцепочечные сегменты определенной длины, состоящие из адениновых нуклеотидов (олиго(dA)-сегменты), а к концам другого фрагмента — комплементарные им олиго(dT)-сегменты (состоящие из тиминовых оснований) примерно такой же длины. При смешении полученных таким образом фрагментов формируются кольцевые структуры за счет водородных связей между олиго(dA)- и олиго(dT)-последовательностями. Одноцепочечные бреши гибридных молекул ДНК застраивают с помощью ДНК-полимеразы и цепи ковалентно сшивают в лигазной реакции.

|
| Рис. 1. Схема коннекторного метода создания рекомбинантных ДНК |
На следующий год после экспериментов П. Берга, другой американский биохимик С. Коэн с сотрудниками предложил более простой метод конструирования гибридных молекул ДНК, основанный на применении двух ферментов: рестриктазы и ДНК-лигазы. Рестриктазно-лигазный метод быстро завоевал популярность и используется до сих пор как наиболее простой и надежный.
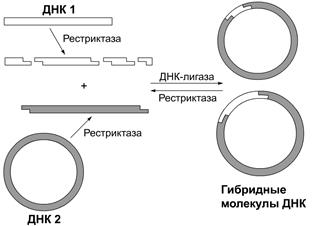
Принцип рестриктазно-лигазного метода. Данный метод состоит из трех этапов (см. рис. 2):
return false">ссылка скрыта1) рестриктазой класса II специфически разрезают молекулы ДНК на фрагменты, имеющие идентичные взаимокомплементарные липкие концы;
2) препараты различных молекул ДНК, гидролизованных одной и той же рестриктазой, смешивают, и при определенных условиях липкие концы разных фрагментов ДНК реассоциируют за счет комплементарного взаимодействия;
3) с помощью ДНК-лигазы происходит ковалентное связывание ассоциированных фрагментов ДНК.
|
| Рис. 2. Схема рестриктазно-лигазного метода создания рекомбинантных ДНК |
Рестриктазно-лигазный метод, по сравнению с коннекторным методом, находит более широкое применение в генно-инженерных манипуляциях, поскольку он более прост биохимически и, кроме того, дает возможность легко выщепить встроенный фрагмент из гибридной молекулы ДНК, что часто бывает важно при переносе фрагмента в другое генетическое окружение.
Данный метод позволяет использовать в каждом конкретном эксперименте одновременно две рестриктазы. Комбинируемые молекулы ДНК при этом могут иметь разные липкие концы. В этом случае фрагменты объединяются в строго определенной ориентации относительно друг друга. При смешении же фрагментов, полученных после гидролиза одной рестриктазой, возможны различные их ориентации в формирующихся гибридных молекулах ДНК. Более того, в процессе лигазной реакции может происходить ковалентное объединение не только двух, но и трех, а также большего числа фрагментов.
По такой схеме могут быть ковалентно соединены in vitro два и более любых фрагмента, полученных при гидролизе молекул ДНК одной и той же рестриктазой. Однако в первоначальном виде метод имеет существенное ограничение, связанное с тем, что с помощью рестриктаз (особенно одного фермента) в каждом конкретном случае можно получить лишь специфический, строго определенный набор фрагментов изучаемой ДНК. Для преодоления этого недостатка была разработана модификация, основанная на использовании линкерных молекул (линкеров)— синтетических сегментов ДНК, содержащих в своем составе последовательности, узнаваемые рестриктазами. Метод предложили Р. Шеллер с сотрудниками в 1977 г. Он позволяет достаточно просто рекомбинировать in vitro практически любые фрагменты ДНК.
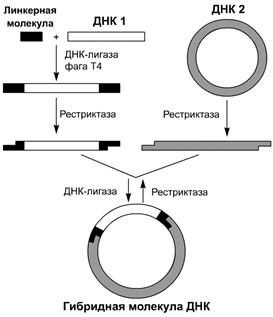
Модификация рестриктазно-лигазного метода с использованием линкеров.Разработанный подход включает следущие операции (рис. 3):
1) по тупым или липким концам фрагмента ДНК, который предполагается рекомбинировать, с помощью лигазы фага Т4 пришивают короткие синтетические двухцепочечные сегменты, имеющие участки узнавания определенной рестриктазы;
2) полученный фрагмент обрабатывают выбранной рестриктазой, в результате чего образуются липкие концы;
3) полученный фрагмент рекомбинируют in vitro с другими молекулами ДНК по обычной схеме рестриктазно-лигазного метода.
|
| Рис. 3. Схема создания рекомбинантных ДНК с использованием линкерных молекул |
Использование линкерных молекул делает рестриктазно-лигазный метод рекомбинации фрагментов ДНК in vitro универсальным, поскольку исходные фрагменты можно получать самыми различными способами.
Практическое занятие №2
Тема: Методы введения рекомбинантных ДНК в клетки
Для введения в клетку рекомбинантных ДНК, сконструированных на основе бактериальных и дрожжевых плазмид или вирусов эукариот, разработано множество различных по своей эффективности и сложности методов. Процесс проникновения экзогенной ДНК в клетку называется трансформацией, а трансформированные клетки принято называть трансформантами. Термином трансфекция обозначается введение в клетки ДНК или РНК вируса с последующим образованием вирусного потомства. Эффективность трансформации обычно невысока. Рекомбинантный геном включается в среднем лишь в одну из примерно 1000 клеток. Однако данный недостаток компенсируется применением эффективных методов скрининга, позволяющих быстро идентифицировать трансформированные клетки.
Трансформация чужеродной ДНК происходит только в компетентные клетки, то есть в те клетки, стенки которых стали проницаемыми для ДНК.
Метод CaCl2-зависимой трансфекции. Разработан М. Манделем и А. Хигом в 1970 г. Клетки бактерий подвергаются обработке ледяным (0° С) раствором CaCl2 с последующим выдерживанием при 42°С в течение 1,5 минут (тепловой шок). При этом происходит локальное разрушение клеточной стенки и клетки становятся способными к поглощению молекул ДНК из внешней среды. Наиболее успешно происходит поглощение фаговой ДНК, несколько хуже – плазмидной. Эффективность метода составляет до 10–4 БОЕ на одну молекулу ДНК фага λ.
Метод ЭДТА-лизоцимных сферопластов. Сферопласты — живые бактериальные или дрожжевые клетки, с почти полностью разрушенной клеточной стенкой. Обычно сферопласты бактерий получают путем обработки клеток раствором бактерицидного фермента лизоцима. Лизоцим гидролизует пептидогликан стенок бактерий, разрушая полисахаридные цепи до дисахаридных фрагментов. Внешняя мембрана грамнегативных бактерий защищает пептидогликановый слой от воздействия ферментов. Поэтому перед использованием лизоцима клетки грамнегативных бактерий обрабатывают комплексообразующим агентом этилендиамининтетраацетатом (ЭДТА), который связывает двухвалентные ионы, стабилизирующие внешнюю мембрану. В результате часть липополисахаридов высвобождается из мембраны и она становится проницаема для лизоцима.
Эффективность метода составляет до 10–3 БОЕ на одну молекулу ДНК фага λ, что на порядок выше, чем при использовании метода CaCl2-зависимой трансфекции, однако, из-за сложности и плохо воспроизводимых результатов данный метод не получил широкого распространения.
Электропорация. Это физический метод повышения компетентности клеток путем кратковременного (5-20 мс) воздействия на них электрическим полем высокой напряженности (1-15 кВ/см). При этом в результате электропробоя происходит образование пор в липидных мембранах. Количество трансформантов при этом может достигать 80 % выживших клеток — столь высокой результативности не удается добиться иными существующими методами.
В настоящее время электропорация благодаря простоте и эффективности становится наиболее популярным методом трансформации как про-, так и эукариотических клеток, чему способствует также серийное производство электропораторов.
ДЭАЭ-декстрановый метод. Применяется для введения ДНК в клетки млекопитающих. Открыт в 1968 г. Дж. Мак-Катченом и Дж. Пагано.
Поликатион диэтиламиноэтилдекстран (ДЭАЭ-декстран) значительно увеличивает эффективность трансфекции клеток животных нуклеиновой кислотой вируса SV40. Очищенную ДНК вируса SV40 инкубируют сначала в растворе с ДЭАЭ-декстраном, варьируя его концентрацию от 100 до 3000 мкг/мл. Затем эту смесь наносят на монослой клеток, который через определенный промежуток времени отмывают от поликатиона и заливают средой. В процессе последующей инкубации на монослое появляются бляшки лизированных клеток. Эффективность трансфекции ДНК вируса SV40 таким методом составляет (1-10) · 106 БОЕ на 1 мкг ДНК. На эффективность трансфекции влияют молекулярная масса (наилучшие результаты достигаются при использовании поликатиона с молекулярной массой 106 Да) и концентрация применяемого ДЭАЭ-декстрана.
Механизм действия ДЭАЭ-декстрана окончательно не установлен, но известно, что он связывается с нуклеиновыми кислотами и частично предохраняет их от деградации нуклеазами. ДЭАЭ-декстран также взаимодействует с клеточной мембраной и, по-видимому, за счет этого увеличивает эффективную концентрацию ДНК на поверхности клеток и стимулирует пиноцитоз, хотя сам при этом клетками не захватывается.
ДЭАЭ-декстрановый метод довольно прост и дает высоковоспроизводимые результаты. К недостаткам метода можно отнести то, что для некоторых культур клеток ДЭАЭ-декстран может быть токсичен при использовании его в высокой концентрации. Кроме того, эффективность трансфекции может существенно зависеть от качества препарата ДЭАЭ-декстрана.
Кальций-фосфатный метод.Является модификацией ДЭАЭ-декстранового метода. На монослой клеток КВ, предварительно обработанных ДЭАЭ-декстраном, наносят ДНК аденовируса Аd5 в растворе СаCl2. При этом эффективность трансфекции повышается в 10-100 раз. Аналогичные результаты получаются, когда клетки не обрабатывают ДЭАЭ-декстраном. Поскольку в питательной среде присутствуют фосфаты, при добавлении раствора хлорида кальция образуется осадок фосфата кальция. Удаление этого осадка из среды приводит к потере инфекционности ДНК. Таким образом, трансфекция происходит в результате соосаждения вирусной ДНК и образующихся микрокристаллов фосфата кальция на клеточный монослой.
На примере ДНК вируса простого герпеса показано, что сразу после соосаждения с фосфатом кальция вирусная ДНК становится устойчивой к разрушению ультразвуком, но комплекс фосфат кальция – ДНК остается чувствительным к ДНКазе в течение 4 ч. При взаимодействии этого комплекса с культурой клеток животных ДНК становится устойчивой к ДНКазе уже в течение первого часа. ДНК образует с фосфатом кальция прочный комплекс, который при оптимальных условиях поглощают практически все реципиентные клетки. Эффективность поглощения клетками комплекса фосфат кальция – ДНК в значительной степени зависит от рН, при котором формировался этот комплекс, и концентрации ДНК. Важно, чтобы осадок фосфата кальция получился мелкодисперсным. Но даже в оптимальных условиях проведения трансфекции данным методом лишь в 1-5 % клеток комплекс достигает ядра. По-видимому, проникновение ДНК из цитоплазмы в ядро является критическим этапом, наиболее сильно влияющим на эффективность трансфекции клеток вирусной ДНК.
Кальций-фосфатный метод обычно более эффективен, чем ДЭАЭ-декстрановый, при трансфекции линейными вирусными ДНК и заметно уступает последнему при использовании кольцевых молекул ДНК. Вероятно, образование микрокристаллов фосфата кальция и соосаждение с ними молекул ДНК сопровождается нарушением структуры части этих макромолекул. Особенно данный эффект сказывается на лабильных кольцевых молекулах ДНК, которые после разрыва цепей и перехода в линейную форму уже не инфекционны. ДЭАЭ-декстрановый метод, как более мягкий, обеспечивает значительно большую эффективность проникновения кольцевых молекул ДНК в клетки животных в неповрежденном виде, хотя в целом доля клеток, поглотивших ДНК при обработке ДЭАЭ-декстраном, существенно меньше, чем при трансфекции кальций-фосфатным методом.
Метод инфекции. Под инфекцией в данном случае подразумевается введение в клетку рекомбинантных ДНК, упакованных в вирусные частицы (рекомбинанты, сконструированные с использованием λ-векторов или космид).
Для упаковки используют рекомбинантные молекулы, вектором в которых выступает ДНК фагов, утративших в результате мутации способность инициировать синтез белков-капсомеров. При помещении ДНК таких фагов в концентрированный экстракт лизогенных по данному вирусу клеток (в них содержаться все необходимые белки), происходит сборка in vitro вирусных частиц. Сформированными таким способом частицами можно заражать бактериальные клетки и получить фаговое потомство.
В капсид упаковываются молекулы ДНК, близкие по размеру фаговому геному, поэтому в бактериальные клетки попадает лишь ДНК заданного размера. Кроме того, в капсиды не упаковываются многочисленные побочные продукты лигазной реакции.
Метод позволяет эффективно клонировать чужеродную генетическую информацию в клетках бактерий.
Микроинъекция вирусных молекул ДНК.Метод впервые воспроизведен А. Грессманом в 1970 г. при введения молекул ДНК в культивируемые клетки млекопитающих. Процедура заключается во введении в клетку (цитоплазму или ядро) малых объемов жидкости (около 10–8 мкл) с помощью стеклянного микрокапилляра. Эксперимент проводится на предметном столике микроскопа с применением микроманипуляторов и микрошприцев. Используя эту методику, удалось изучить биологическую активность молекул ДНК разных вирусов. К достоинствам метода относится то, что определенное количество препарата ДНК можно ввести в выбранную область клетки, в частности в ядро. Недостатком метода является его сложность и невысокая производительность. Кроме того, по-видимому, он применим лишь к небольшим молекулам ДНК, так как при продавливании через микрокапилляр целостность больших молекул ДНК будет нарушаться вследствие гидродинамического сдвига. В силу отмеченных недостатков метод микроинъекции ДНК используется крайне редко.
Практическое занятие №3
Тема: Методы идентификации клонов, содержащих рекомбинантные ДНК
Идентификация клонов, несущих нужные гибридные (рекомбинантные) молекулы ДНК, называется скринингом.
Фенотипический скрининг. Этот метод требует наличия в гибридной молекуле одного или более маркёров. Под маркёром в данном случае понимается ген, кодирующий легко обнаруживаемый фенотипический признак. Клоны, имеющие данный признак (или признаки) являются обладателями нужной гибридной молекулы.
Часто в качестве маркёров выступают гены, обуславливающие устойчивость клеток к определенным антибиотикам или антиметаболитам. При высеве на питательную среду, содержащую этот антибиотик или антиметаболит, будут расти только клетки трансформантов. Особенно хорошо данная система селекции отработана для бактерий, так как получены векторные плазмиды, детерминирующие устойчивость трансформированных клеток сразу к нескольким антибиотикам. Если векторная плазмида определяет устойчивость к двум антибиотикам и при встройке в нее экзогенного фрагмента ДНК нарушается одна из генетических детерминант устойчивости к антибиотикам, то клоны клеток, содержащих такие гибридные ДНК, легко отличить от трансформантов, включающих исходный вектор, на средах с каждым антибиотиком в отдельности.
Например, если векторная плазмида детерминирует устойчивость одновременно к тетрациклину и ампициллину (ТсrАрr) и при встройке в нее чужеродного фрагмента нарушается ген устойчивости к ампициллину, то гибридная плазмида будет обусловливать фенотип клетки-хозяина ТсrАрs, т. е. устойчивость к тетрациклину и чувствительность к ампициллину. Плазмиды после встройки в них фрагментов ДНК вводят в клетки, культуру высевают на чашки сагаризованной питательной средой, в которую добавлен тетрациклин. При этом вырастают колонии клеток, содержащих или исходную векторную плазмиду, или гибридные плазмиды. Затем колонии перепечатывают на чашки с ампициллином и чашки с тетрациклином. Те колонии, которые после перепечатки будут расти на среде с тетрациклином и не дадут роста на среде с ампициллином, содержат гибридные плазмиды. Простота манипуляций обусловила широкое использование данного типа векторов для клонирования самых различных фрагментов ДНК. Однако такие плазмиды не позволяют осуществлять прямой отбор гибридных клонов — сразу после высева трансформантов на селективную среду и появления колоний.
В последние годы получен ряд векторных плазмид, предназначенных для прямой селекции трансформантов, содержащих гибридные плазмиды. Такие векторы обычно имеют гены, потенциально летальные для чувствительных клеток-реципиентов, и могут трансформировать эти клетки только после инактивации данных генов встраиванием в них фрагментов ДНК.
Скрининг с помощью гибридизации. Нужную нуклеотидную последовательность в образце ДНК можно обнаружить с помощью ДНК-зонда, спаривающегося только с искомой последовательностью. Для этого ДНК сначала переводят в одноцепочечную форму, подвергнув ее тепловой обработке или воздействию щелочью. В этих условиях водородные связи между основаниями разрываются и цепи расходятся (происходит денатурация). Если теперь медленно снизить температуру, то произойдет их воссоединение (ренатурация). При этом, если в растворе присутствует одноцепочечный ДНК-зонд, он тоже будет ренатурировать с ДНК, специфически спариваясь с комплементарными участками. В результате образуется гибридная ДНК, т. е. двухцепочечная молекула, цепи которой принадлежат двум разным ДНК (рис. 4).

|
| Рис. 4. ДНК-гибридизация |
Принцип метода. ДНК-мишень подвергают денатурации и одноцепочечные молекулы необратимо «пришивают» к твердой подложке (нитроцеллюлозному или найлоновому фильтру). Эту процедуру обычно проводят при высокой температуре. Провести гибридизацию непосредственно на поверхности питательной гелевой среды, на которой культивировались микроорганизмы, невозможно, поскольку зонд не может в нее проникнуть. Перенос ДНК из геля на фильтр носит название Саузерн-блоттинга в честь Эдвина Саузерна, который изобрел этот метод.[1] Затем фильтр инкубируют с одноцепочечным ДНК-зондом, меченным радиоизотопом или другой меткой. Если нуклеотидные последовательности зонда и ДНК-мишени комплементарны, то происходит их спаривание (т. е. гибридизация). Гибридные молекулы можно визуализировать радиоавтографическим или другим методом, зависящим от природы метки.
Радиоавтографический метод широко применяется для локализации радиоактивного материала. Для регистрации радиоактивных зон на исследуемый образец накладывают рентгеновскую пленку, в которой под действием радиоактивного излучения из бромида серебра образуется металлическое серебро. «Засвеченные» участки, соответствующие радиоактивным зонам, наблюдаются визуально после проявления пленки.
Если комплементарность между зондом и ДНК-мишенью отсутствует, то гибридизации не происходит, и результат получается отрицательным.
Обычно размер зонда варьирует от 100 до 1000 п. н., хотя можно использовать как более крупные зонды, так и зонды меньшего размера. Для гибридизации, т. е. для образования стабильного комплекса, необходимо, чтобы на участке длиной 50 нуклеотидов совпадало более 80% из них, но это зависит от условий реакции.
Радиоиммунологический скрининг.Данный метод применяется в случае, если клонируемый ген активно экспрессируется в клетке-хозяине. Продукцию экспрессии гена — белок или его часть, можно обнаружить иммунологическими методами.
В основу метода положена способность молекул иммуноглобулинов связываться с полистиролом или поливинилом. Необходимым условием является наличие у исследуемого белка не менее двух антигенных детерминант, что дает ему возможность связывать по крайней мере две разные молекулы иммуноглобулинов.
Принцип метода. Колонии трансформантов перепечатывают идентичным образом на две чашки с агаризованной питательной средой и чашки инкубируют до получения колоний необходимого размера. Затем на одной из чашек лизируют бактериальные клетки и прижимают к поверхности среды поливиниловый диск с адсорбированными на нем специфическими антителами. При этом на диске происходит иммуносорбция антигена. После промывания диска на него наносят 125I-меченные антитела (препарат поликлональных иммуноглобулинов) к белку искомого гена. Таким образом, при наличии в чашке специфического белка (антигена), на фильтре образуется комплекс «антитело 1-антиген-антитело 2». Первое антитело служит для прикрепления комплекса к фильтру, второе является маркером, позволяющим выявить колонии, в которых образовался комплекс, методом радиоавтографии.
Из соответствующих колоний с матричных чашек бактерии пересевают на питательные среды и проводят анализ содержащихся в них гибридных плазмид.
Практическое занятие №4
Тема: Методы секвенирования
Генетическая инженерия как отрасль биотехнологии во многом обязана своим успешным развитием появлению относительно простых методов, позволяющих достаточно быстро определить последовательность нуклеотидов в исследуемых фрагментах ДНК.
Дидезоксинуклеотидный метод секвенирования ДНК.Дидезоксинуклеотид — это полученный искусственным путем нуклеотид, лишенный 2'- и 3'-гидроксильных групп при углеродных атомах сахарного кольца (рис. 5, А). У дезоксинуклеотида, входящего в норме в состав ДНК, отсутствует только 2'-гидроксильная группа (рис. 5, Б).

|
| Рис. 5. Отличие дидезоксинуклеотида от дезоксинуклеотида А – дидезоксинуклеотид: отсутствуют 2' и 3'-гидроксильные группы в дезоксирибозном кольце; Б – дезоксинуклеотид: отсутствует только 2'-гидроксильная группа. |
Удлинение цепи во время репликации ДНК происходит в результате присоединения очередного нуклеозидтрифосфата к 3'-гидроксильной группе последнего нуклеотида растущей цепи. И если таким очередным присоединяемым звеном является дидезоксинуклеотид, то синтез ДНК останавливается, поскольку следующий нуклеотид не может образовать фосфодиэфирную связь. Остановка синтеза ДНК — это ключевой этап дидезокси-метода, но чтобы осуществить секвенирование в полном объеме, необходимо выполнить целый ряд условий.
Первый шаг стандартной процедуры дидезокси-секвенирования состоит в гибридизации синтетического олигонуклеотида длиной 17–20 звеньев со специфическим участком одной из цепей клонирующего вектора, соседствующим со вставкой. Этот олигонуклеотид является праймером, поставляющим 3'-гидроксильную группу для инициации синтеза. Раствор с праймером распределяют по четырем пробиркам, в каждой из которых находятся четыре дезокси-нуклеотида, dATP, dСТР, dGТР и dTТР (один из них — изотопно меченный), и один из четырех дидезоксинуклеотидов (ddАТР, ddСТР, ddGТР или ddTТР). Концентрацию каждого дидезоксинуклеотида подбирают таким образом, чтобы он оказался включенным по всем позициям в смеси растущих цепей, а не только в первой встретившейся ему позиции. По окончании ферментативного синтеза при участии ДНК-полимеразы в каждой пробирке оказывается уникальный набор олигонуклеотидов, каждый из которых содержит праймерную последовательность.
Далее в пробирки добавляют формамид, чтобы обеспечить расхождение цепей, и проводят электрофорез в полиакриламидном геле на четырех дорожках (по числу пробирок). Это позволяет разделить одноцепочечные фрагменты ДНК, даже если они различаются по длине всего на один нуклеотид. На радиоавтографе обнаруживается набор полос, отвечающих меченым фрагментам ДНК, сопоставление которых позволяет прямо «прочитать» нуклеотидную последовательность секвенируемого сегмента ДНК.
Секвенирование ДНК с помощью вектора на основе фага М13.Метод основывается на применении фага М13 E. coli в качестве вектора. ДНК этого фага представляет собой одноцепочечную кольцевую молекулу. Когда им инфицируют E. coli, сначала образуется двухцепочечная репликативная форма фаговой ДНК, а одноцепочечные кольцевые молекулы, которые затем упаковываются в вирионы, синтезируются на этой двухцепочечной молекуле как на матрице. Клетки, инфицированные М13, не подвергаются лизису; в них непрерывно образуются новые одноцепочечные молекулы ДНК М13, которые, проходя через клеточную мембрану, одеваются белковой оболочкой и выходят в окружающую среду. ДНК М13 содержит несущественную часть, которую можно заменить нужным фрагментом ДНК; при этом инфекционность рекомбинантных вирусных частиц сохранится.
М13-система имеет следующие преимущества: выделенная двухцепочечная репликативная форма может функционировать как плазмида, а одноцепочечная фаговая ДНК — использоваться в качестве матрицы для секвенирования ДНК. Все это позволяет использовать фаг М13 как комбинированную систему для клонирования и секвенирования ДНК.
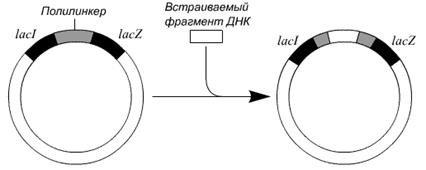
Принцип метода. Обычно нужный фрагмент ДНК длиной примерно 500 п. н. встраивают в полилинкер, который является частью клонированного в РФ-ДНК фага М13 модифицированного гена lacZ' (рис. 6). Рекомбинантной вирусной ДНК трансформируют компетентные клетки E. coli и высевают их на чашки со средой, содержащей субстрат X-Gal. При его гидролизе β-галактозидазой образуется продукт, имеющий синюю окраску. На чашках появляются белые (бесцветные) и синие колонии. Первые отвечают клеткам, инфицированным фагом М13 со вставкой, нарушившей рамку считывания гена lacZ', вторые — клеткам, инфицированным фагом М13 с функциональным геном lacZ', не несущим вставки. Из белых колоний выделяют фаговые частицы, а из них — одноцепочечную ДНК со вставкой. Для секвенирования последней отжигают выделенную ДНК с праймером, который гибридизуется с последовательностью вблизи вставки, затем проводят дидезокси-секвенирование, электрофорез и радиоавтографию и «прочитывают» нуклеотидную последовательность вставки.
|
| Рис. 6. Вставка фрагмента ДНК в репликативную форму ДНК фага М13 |
Практическое занятие №5
Тема: Амплификация последовательности ДНК in vitro
Для решения широкого круга задач, связанных с изучением и модификацией генома, довольно часто возникает необходимость получения множества копий определенного фрагмента ДНК. Процесс многократного копирования данного фрагмента называется амплификацией.
Амплификация ДНК методом ПЦР. Ферментативный метод амплификации фрагментов ДНК, получивший название полимеразной цепной реакции (ПЦР), был разработан К. Маллисом с сотрудниками в 1985 г.
Процедура состоит из многократного последовательного повторения трех реакций: денатурации, ренатурации и синтеза (рис. 7).
К целевому образцу двунитевой ДНК добавляют в избыточном количестве два синтетических олигонуклеотида-праймера, размером около 20 нуклеотидов, каждый из которых комплементарен одному из 3'-концов антипараллельных цепей целевого сегмента ДНК.
Препарат подвергают термической денатурации, выдерживая его при температуре 95º С в течение 1 минуты, затем медленно охлаждают до ~55º С. При этом в процессе отжига (ренатурации), происходит гибридизация олигонуклеотидов-праймеров с комплементарными последовательностями нитей целевой ДНК. После этого вносят фермент ДНК-полимеразу и дезоксинуклеозидтрифосфаты, служащие «строительным материалом», что запускает реакцию синтеза комплементарных цепей целевой ДНК.
После завершения синтеза, вновь повторяют денатурацию и ренатурацию, что приводит к гибридизации праймеров, находящихся в избытке, не только с цепями исходной ДНК, но и с вновь синтезированными. Внесение в препарат новой порции ДНК-полимеразы инициирует второй цикл полимеразной реакции. При использовании термостабильных полимераз (например, Taq, выделенной из термофильных бактерий Thermus aquaticus), повторного внесения фермента в каждом новом цикле не требуется.
Многократное повторение описанной процедуры позволяет провести 30 и более циклов ферментативного синтеза. При этом число амплифицируемых сегментов ДНК с каждым циклом удваивается (увеличивается экспоненциально). Таким образом, используя ПЦР, можно in vitro обогащать препарат ДНК целевым фрагментом в миллион и более раз.
Все реакции проводят в пробирках, погруженных в термостат. Смена температурного режима и его поддержание осуществляется автоматически. Каждый цикл обычно длится 3–5 мин.

|
| Рис. 7. Схема амплификации ДНК методом ПЦР (показаны первые два цикла) |
К недостаткам метода можно отнести то, что при полимеразной реакции происходят ошибочные включения некомплементарных нуклеотидов в цепь с частотой 1,1 · 10–5 в одном цикле. Синтезированные последовательности ДНК, содержащие ошибки, в следующих циклах ПЦР амплифицируются экспоненциально. После 30 циклов частота ошибок в амплифицированной ДНК может достигать 0,25 %.
Преодолеть данную проблему можно добавлением в препарат дополнительного фермента — полимеразы GB-D, выделенной из Pirococcus sp. GB-D обладает корректирующей 3'–5'-эндонуклеазной активностью и может удалять ошибочно введенные некомплементарные нуклеотиды из растущей цепи ДНК.
Метод ПЦР находит самое разнообразное использование в молекулярной биотехнологии. Он используется для секвенирования, для повышения эффективности клонирования целевых фрагментов геномов, для детекции патогенных микроорганизмов, для тонкого анализа хромосомной рекомбинации и т.д. С помощью этого метода удалось клонировать фрагменты митохондриальной ДНК из ископаемых останков человека возраст которых семь тысяч лет! В генетическом анализе, позволяющем установить отцовство или выявить преступника, также используется метод ПЦР.
Практическое занятие №6
Тема: Генетически модифицированные микроорганизмы и их использование
Началом промышленной генетической инженерии принято считать 1980 год (всего через 8 лет после работы Берга!), когда в США был выдан первый патент на модифицированный штамм микроорганизма, способного разлагать нефть. Еще через два года был разрешен для клинического использования полученный из бактерии первый лекарственный препарат – человеческий инсулин.
Сейчас прикладная промышленная микробиология развивается по нескольким основным направлениям:
1) производство продуктов биосинтеза трансгенных микроорганизмов, например, антибиотиков, гормонов, ферментов и витаминов;
2) использование биомассы микроорганизмов – производство медицинских вакцин, различных дрожжей, белково-витаминных концентратов и заквасок для получения кисломолочных продуктов и силосования кормов;
3) биотехнологии, основанные на уникальных способностях некоторых бактерий производить органические кислоты, этанол, углеводы и метан. Сюда же можно отнести и переработку некоторых отходов с возможностью получения полезных соединений, в первую очередь, горючих газов.