Решение.
рН = - lg[Н+] = -lg(2×10-2) = 1.70
Решая обратную задачу, по известному значению рН легко найти концентрации водородных и гидроксид-ионов.
Пример 2. Вычислить [Н+] и [ОН-] раствора, рН которого равен 10.33.
Решение.
[Н+] = 1×10-10.33 = 4.7×10-11 М.
рОН = 14 - 10.33 = 3.67.
[ОН-] = 1×10-3.67 = 2.1×10-4 М.
Сильные кислоты (НХ) и сильные основания (МОН) в водных растворах практически полностью диссоциированы.
| HX = H+ + X- | (1.12) |
| MOH = M+ + OH- | (1.13) |
Концентрации Н+ и ОН- в этих растворах в первом приближении можно считать равными общей концентрации СА кислоты (НХ) и соответственно основания (МОН). Следовательно,
| pH = -lgCHX | (1.14) |
| pOH = -lgCMOH | (1.15) |
Эти выражения являются приближенными. В более строгих расчетах концентрацию электролитов следует заменять активностью ионов. Между концентрацией иона и активностью его существует следующая зависимость:
| aA = γA×CA | (1.16) |
где γA - коэффициент активности. Коэффициент активности зависит от ионной силы раствора (μ)

| (1.17) |
где 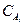 - концентрации ионов - катионов и анионов (М),
- концентрации ионов - катионов и анионов (М),  - заряды ионов.
- заряды ионов.
Если 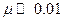 , коэффициент активности в водных растворах рассчитывается по формуле
, коэффициент активности в водных растворах рассчитывается по формуле

| (1.18) |
При 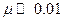 расчет проводится по более сложному уравнению
расчет проводится по более сложному уравнению

| (1.19) |
Для сильных электролитов только в очень разбавленных растворах (~ 0.0001 М) γA = 1 и аА = СА. Коэффициент активности можно не учитывать также для недиссоциированных молекул.
Для простоты расчетов в дальнейшем во всех случаях, кроме оговоренных, вместо активностей используются концентрации.
Пример 3. Вычислить рН 0.0018%-ного раствора хлороводородной кислоты.
Решение. Найдем концентрацию НС1, выраженную в М, учитывая, что молекулярная масса НС1 36.46:

рН = - lg(4.94×10-4) = 3.31.
Пример 4.В 250 мл раствора содержится 0.1 г гидроксида натрия. Вычислить рН раствора.
Решение. Найдем концентрацию NaOH, выраженную в моль/л. Молекулярная масса NaOH 40.

Ионная сила 0.01 М раствора гидроксида натрия равна:
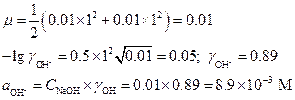
pOH = -lg(8.9×10-3) = 2.05
pH = 14-2.05 = 11.95
Пример 5. К 3 л воды прибавлен 1 г HNO3 (ρ = l.4). Вычислить рН раствора.
Решение. По таблицам находим, что в 100 г азотной кислоты (ρ = 1.4) содержится 65.3 г HNO3. Тогда концентрация HNO3 в М будет равна

pH = -lg(3.4×10-3) = 2.47
В случае слабых кислот константа равновесия реакции {1.2) может быть выражена следующим уравнением:

| (1.20) |
где Ка - константа диссоциации кислоты НА.
Если общую концентрацию кислоты обозначить СНА, а равновесную [НА], то
| [НА] = СНА - [Н+]. | (1.21) |
Из уравнения (1.2) следует, что [Н+] = [А-]. Тогда выражение константы диссоциации слабой кислоты можно записать следующим образом:

| (1.22) |
Отсюда легко найти концентрацию [Н+]

| (1.23) |
Если кислота диссоциирована в незначительной степени ( 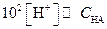 ), то приближенно можно считать, что.
), то приближенно можно считать, что.
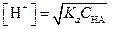
| (1.24) |
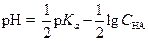
| (1.25) |
Слабое основание, как и слабая кислота, в водных растворах диссоциирует неполностью

| (1.26) |
как и для слабой кислоты,
| [BOH] = СBOH - [OН-]. | (1.27) |
Поскольку [В+] = [ОН-], уравнение для константы диссоциации слабого основания будет иметь вид

| (1.28) |
и

| (1.29) |
Когда [OH-] << Свон (102 [ОН-] < Свон), можно принять

| (1.30) |

| (1.31) |

| (1.32) |
Пример 6.Вычислить рН 0.017 М раствора муравьиной кислоты.
Решение.

|
CHCOOH = 0. = 1.7×10-2 М

рН = -lg(1.7×10-3 ) = 2.76.
Пример 7.Вычислить рН 0.06 М раствора аммиака.