Расчет свободной энергии Гиббса и энтропии вещества при давлении, отличном от давления при стандартных условиях
Молярные энтальпия  , теплоемкости
, теплоемкости  и внутренняя энергия
и внутренняя энергия  зависят только от температуры:
зависят только от температуры: 
Молярные энтропия 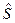 , свободная энергия Гиббса
, свободная энергия Гиббса  , свободная энергия Гельмгольца
, свободная энергия Гельмгольца  зависят от температуры и давления.
зависят от температуры и давления.
Установим связь между величинами:  и их значениями при стандартном состоянии
и их значениями при стандартном состоянии 
 которые определяются с использованием справочных материалов.
которые определяются с использованием справочных материалов.
Получим сначала выражение для свободной энергии Гиббса. Из объединенного выражения 1 –го и 2 –го законов термодинамики для простой, закрытой ТС и для обратимых процессов для 1 моля вещества имеем:

При T=const (dT = 0) получаем 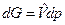 , где
, где 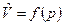 . Откуда после интегрирования для конечного процесса в диапазоне давлений от р0 до р имеем
. Откуда после интегрирования для конечного процесса в диапазоне давлений от р0 до р имеем
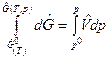 , или
, или 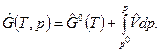 (1)
(1)
где  -молярная свободная энергия Гиббса при р0=1физ.атм,
-молярная свободная энергия Гиббса при р0=1физ.атм, 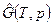 - то же при давлении
- то же при давлении  . Зависимость (1) справедлива для газообразных и конденсированных веществ при Т=const.
. Зависимость (1) справедлива для газообразных и конденсированных веществ при Т=const.
Для идеального газа,  . Следовательно,
. Следовательно, 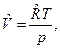 а интеграл в (1) будет равен
а интеграл в (1) будет равен 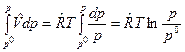 . Обозначив через
. Обозначив через 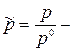 безразмерное давление; где р0 = 101325Па; ~ тильда, получим для идеального газа формулу для расчета свободной энергии Гиббса при давлении р≠р0:
безразмерное давление; где р0 = 101325Па; ~ тильда, получим для идеального газа формулу для расчета свободной энергии Гиббса при давлении р≠р0:
 , (2)
, (2)
Если вещество находится в газовой смеси, то для i-ого компонента смеси идеальных газов имеем:
 , (3)
, (3)
где нормированное парциальное давление  и нормированное давление смеси
и нормированное давление смеси 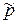 связаны соотношением
связаны соотношением  , учитывающим молярную долю
, учитывающим молярную долю  i-го газа,
i-го газа, 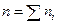 , а давление смеси газов определяется законом Дальтона
, а давление смеси газов определяется законом Дальтона 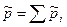 .Для получения формулы для расчета
.Для получения формулы для расчета 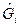 , выраженной через молярные доли, представим формулу (3) в виде:
, выраженной через молярные доли, представим формулу (3) в виде:
 (4)
(4)
Обозначим  - молярную свободную энергию Гиббса i-го газа при давлении смеси. Тогда получим
- молярную свободную энергию Гиббса i-го газа при давлении смеси. Тогда получим
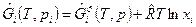 . (5)
. (5)
Молярные свободные энергии Гиббса конденсированных веществ от давления не зависят, поскольку можно пренебречь их объемами по сравнению с объемами газообразных компонентов. Тогда формула для расчета 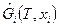 конденсированных веществ примет вид:
конденсированных веществ примет вид:
 , (6)
, (6)
где хi – молярная доля i-го вещества относительно фазы, в которой оно находится(к числу молей своей фазы), 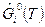 — молярная свободная энергия Гиббса чистого конденсированного вещества, при p=p0=101325Па.
— молярная свободная энергия Гиббса чистого конденсированного вещества, при p=p0=101325Па.
Влияние давления на энтропию может быть определено из выражения для молярной свободной энергии Гиббса для i-го компонента идеального газа при давлении p ≠p0
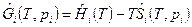 ,
,
из которого следует, что
 (7)
(7)
где  . (8)
. (8)
После подстановки (8) в (7) и учитывая, что 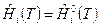 , получим:
, получим:
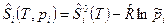 . (9)
. (9)
Для i-го компонента конденсированного вещества по аналогии с выражением (9) можно получить формулу для расчета энтропии при p ≠p0
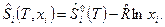 (10)
(10)
Величина  - берется из справочника при р0 =101325 Па.
- берется из справочника при р0 =101325 Па.