Энтальпия
В термодинамике важную роль играет величина суммы внутренней энергии системы U и произведения давления системы р на величину объема системы V, называемая энтальпией и обозначаемая Н:
H = U + pV. (2.29)
Так как входящие в нее величины являются функциями состояния, то и сама энтальпия является функцией состояния и поэтому может быть представлена в виде функции двух любых параметров состояния:
Н = y1 (р, V); H = y2 (V, Т);
Н = y3 (р, Т).
Так же как внутренняя энергия, работа и теплота, энтальпия измеряется в джоулях.
Энтальпия обладает свойством аддитивности. Величина
h = u + pv, (2.30)
называемая удельной энтальпией (h =H/m), представляет собой энтальпию системы, содержащей 1 кг вещества, и измеряется в Дж/кг.
Поскольку энтальпия есть функция состояния, dH является полным дифференциалом, и, следовательно, изменение энтальпии в любом процессе определяется только начальным и конечным состояниями тела и не зависит от характера процесса.
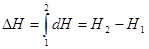 .
.
Физический смысл энтальпии ясен из следующего простого примера. В цилиндре под поршнем находится газ Его давление уравновешивается грузом весом pF.
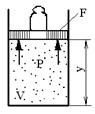
Полная энергия Е расширенной системы, состоящей из газа и поршня с грузом, складывается из внутренней энергии газа U и потенциальной энергии поршня с грузом, равной pFy = pV, так что E = U + pV = H.
Член pV численно равен работе, которую нужно совершить, чтобы ввести объем V газа из вакуума в пространство с давлением р. Он характеризует потенциальную энергию газа, сжатого внешним давлением.
Следовательно, энтальпия любой термодинамической системы представ-ляет собой сумму внутренней энергии системы и потенциальной энергии источника внешнего давления.
Уравнение (2.11), с учетом (2.5),
dq = du + p×dv
в случае, когда единственным видом работы является работа расширения, с учетом очевидного соотношения
p×dv = d(pv) – v×dp
может быть записано в виде
dq = d(u +pv) – v×dp,
или dq = dh – v×dp. (2.31)
Из этого соотношения следует, что если давление системы сохраняется неизменным, т.е. осуществляется изобарный процесс (dp=0), то dqp = dh (2.32)
и qp = h2 – h1, (2.33)
т.е. теплота, подведенная к системе при постоянном давлении, расходуется только на изменение энтальпии данной системы.
Для идеального газа с учетом (2.18) и (1.3) получим:
dh = du+d(pv) = сv dT + R dT =
= (cv + R) dT=cp dT. (2.34)
Начало отсчета энтальпии, так же как и внутренней энергии, примем равным 0 ˚С:
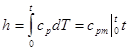 . (2.35)
. (2.35)
При расчетах практический интерес представляет изменение энтальпии в конечном процессе:
Dh = h2 – h1 = 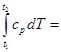
 . (2.36)
. (2.36)