Ориентирующее действие заместителей в бензольном ядре.
| Название субстрата | Формула соединения | Заместитель | Эффекты заместителя | Распределение ē плотности | Характер заместителя | Влияние на SЕ | Положения, которые направляется входящая группа | Формулы продуктов реакции SЕ | Род ориентакта |
| Толуол | CH3–метил | +I | ЭД, ↑ē плотность в кольце | облегчает | орто– пара– | I | |||
| Фенол | OH–гидрокси | –I +M | ЭД, +М > –I | облегчает | орто– пара– | I | |||
| Анилин | NH2–амино | –I +M | ЭД, +М > –I | облегчает | орто– пара– | I | |||
| Хлор-бензол | Cl–хлор | –I +M | ЭА, +М < –I, ↓ē плотность в кольце | затрудняет | орто– пара– | I | |||
| Бром-бензол | Br–бром | –I +M | ЭА, +М < –I | затрудняет | орто– пара– | I | |||
| Бензойная кислота | –карбоксил | –I –M | ЭА | затрудняет | мета– | II | |||
| Бензаль-дегид | Альдегидная | –I –M | ЭА | затрудняет | мета– | II | |||
| Нитро-бензол | нитро– | –I –M | ЭА | Затрудняет | мета– | II |

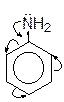 Пример 1. Бромирование анилина.
Пример 1. Бромирование анилина.



 Схема реакции: + Br2 o-броманилин + HBr
Схема реакции: + Br2 o-броманилин + HBr
n-броманилин
 Механизм реакции:
Механизм реакции:
I. Образование Е+: Br – Br + FeBr3 → Br+ + FeBr4–
 II. Образование π-комплекса
II. Образование π-комплекса
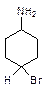


 III. Образование σ–комплекса + и +
III. Образование σ–комплекса + и +


 IV. Восстановление ароматичности за счет выброса протона, образование продукта реакции
IV. Восстановление ароматичности за счет выброса протона, образование продукта реакции
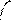 |
 + – n+
+ – n+
 | |||
 | |||



 + – n+
+ – n+
 H+ + FeBr4– = HBr + FeBr3
H+ + FeBr4– = HBr + FeBr3
Пример 2. Метилирование бензойной кислоты.
 |  | ||
AlCl3
Схема реакции: + CH3Cl → + HCl
катализатор
м–метил
Механизм реакции:
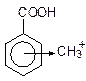 I. Образование Е+: CH3 – Cl + AlCl3 → CH3+ + AlCl4
I. Образование Е+: CH3 – Cl + AlCl3 → CH3+ + AlCl4
 II. Образование π–комплекса:
II. Образование π–комплекса:
 III. Образование σ–комплекса: +
III. Образование σ–комплекса: +


 IV. Восстановление ароматичности за счет выброса протона, образование продукта реакции
IV. Восстановление ароматичности за счет выброса протона, образование продукта реакции
 + – n+ H+ + AlCl4– = HCl + AlCl3
+ – n+ H+ + AlCl4– = HCl + AlCl3
(катализатор после реакции
выделяется в неизменном виде).
SE in vivo
 Йодирование тирозина в ходе биосинтеза йодсодержащих гормонов щитовидной железы.
Йодирование тирозина в ходе биосинтеза йодсодержащих гормонов щитовидной железы.
 +I2 +I2
+I2 +I2


 CH2 – CH – COOH →
CH2 – CH – COOH →  CH2 CH – COOH → фермент фермент
CH2 CH – COOH → фермент фермент
3-йодтирозин
 CH2 CH – COOH
CH2 CH – COOH
3,5-дийодтирозин