Закон Гесса.
Г.И.Гесс (1840) описал закон, получивший его имя и являющийся основным законом термохимии. Закон Гесса устанавливает, что если из данных исходных веществ можно различными путями получить заданные конечные продукты, то независимо от путей получения, т.е. от вида промежуточных реакций, суммарный тепловой эффект для всех путей будет одним и тем же.
Иначе говоря, тепловой эффект химических реакций зависит только от вида и состояния исходных веществ и конечных продуктов, но не зависит от пути перехода.
Закон Гесса является вполне строгим только для процессов, протекающих при постоянном объеме (когда тепловой эффект равен ΔU) или при постоянном давлении (когда тепловой эффект равен ΔН). Для этих процессов он легко выводится из общего уравнения первого начала (закон Гесса был установлен раньше, чем было введено уравнение первого начала).
Для большей наглядности в качестве исходных веществ возьмем кислород и уголь (считая его чистым углеродом), а в качестве конечного продукта СО2 (рис.1). Переход от исходных веществ к конечному можно осуществить, непосредственно сжигая уголь до СО2. Но можно также провести процесс в две стадии, получая в первой из них СО и сжигая затем СО во второй стадии до СО2. (При работе газогенераторного двигателя, например в газогенераторном автомобиле, горючее сжигается в генераторе до СО, а уже СО сгорает до СО2 в цилиндрах мотора).
Все эти три процесса находят широкое применение в практике. Закон Гесса позволяет связать тепловые эффекты этих трех процессов простым уравнением:
ΔН1=ΔН2+ΔН3
пользуясь которым легко определить один из них, если другие два известны. В нашем случае можно сравнительно легко измерить тепловые эффекты первого и третьего процессов, но сжигание угля до окиси углерода при невысоких температурах затруднительно. Поэтому возможность определить его тепловой эффект расчетным путем является весьма ценной. Из предыдущего получаем:
ΔН2=ΔН1 -ΔН3 (1.4)
Численные значения ΔН1и ΔН2 зависят от вида применяемого угля. Величина ΔН3 с этим, очевидно, не связана. Количество теплоты, выделяющейся при сгорании одного моля СО при постоянном давлении, составляет 67,636 ккал (при 25°С).
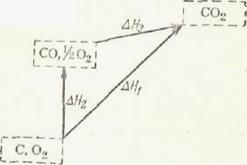
Рис.1. Схема, иллюстрирующая закон Гесса в приложении к реакции окисления угля до СО2
Пусть, например, нас интересует величина ΔН2 при 25 °С для угля, для которого при этой температуре ΔН1 равно —94,0 ккал/моль. Согласно уравнению, определяем:
ΔН2= — 94,0 + 67,6 = — 26,4 ккал/моль
Закон Гесса широко применяется при различных термохимических расчетах; он дает возможность вычислить тепловые эффекты процессов, для которых экспериментальные данные отсутствуют, а во многих случаях - и для таких, для которых они не могут быть измерены в нужных условиях, или когда процессы еще не осуществлялись. Это относится как к химическим реакциям, так и к процессам растворения, испарения, кристаллизации, адсорбции и др. Однако, применяя данный закон, следует строго соблюдать условия, лежащие в его основе.
Прежде всего необходимо, чтобы в обоих процессах были действительно одинаковы начальные состояния и действительно одинаковы конечные состояния. При этом одинаковыми должны быть не только химические составы продуктов, но и условия их существования (температура, давление и пр.) и агрегатное состояние, а для кристаллических веществ – также и кристаллическая модификация. Так, образование одного моля газообразной и одного моля жидкой Н2О из Н2 и О2 при 25 °С сопровождается выделением соответственно 57,798 и 68,317 ккал; разность составляет 10,519 ккал и равна теплоте испарения моля воды в этих условиях. При точных расчетах в случае, если какие-либо из веществ, участвующих в реакциях, находятся в высокодисперсном (т. е. сильно раздробленном) состоянии, существенной оказывается иногда даже и одинаковость степени дисперсности веществ и пр.
Очевидно, тепловой эффект будет различен также в зависимости от того, будут ли получаемые или исходные вещества находиться в чистом состоянии или в растворе, отличаясь на величину теплоты растворения.
Опытное определение тепловых эффектов.
Для определения тепловых эффектов, сопровождающих химические реакции, применяются специальные приборы, называемые калориметрами. Калориметрическое определение ведется так, чтобы вся химическая энергия выделялась в виде теплоты или частично затрачивалась па совершение внешней работы расширения газа, которая может быть учтена. Химическая реакция ведется в сосуде Дьюара. Он представляет собой стеклянный сосуд с посеребренными изнутри двойными стенками, из пространства между которыми выкачан воздух, вследствие чего стенки сосуда почти не проводят теплоты. Для более равномерного теплообмена с окружающей средой сосуд все же помещают обычно в большой термостат, наполненный водой. Во время опыта температура термостата поддерживается постоянной. Сосуд покрыт медной крышкой с тремя отверстиями: для термометра, мешалки и для пробирки. В сосуд и пробирку помещают навески реагирующих веществ, где они находятся до тех пор, пока не уравняется температура всех частей прибора. Определив температуру реагирующих веществ до начала реакции, проводят реакцию и определяют температуру в калориметре после реакции.
Зная теплоемкость системы (которая определяется предварительно), можно вычислить количество тепла, приобретенного содержимым калориметра по время реакции, и отсюда — тепловой эффект реакции.
При экспериментальном определении тепловых эффектов химических реакций возникают ошибки и неточности, обусловленные главным образом теплообменом прибора с внешней средой. Чтобы уменьшить теплообмен, ведут реакцию возможно быстрее и температуру калориметра в начале опыта поддерживают по возможности равной температуре воздуха и лаборатории. При определении изменения температуры тоже может появиться ряд неточностей. Большей частью для измерения температуры пользуются специальными калориметрическими термометрами. Кроме того, так как не весь столбик ртути находится при той температуре, какая имеется в калориметре, необходимо делать поправку на «выступающий столбик». Об этих поправках, а также о предосторожностях, которые необходимо соблюдать, чтобы получить верные результаты, сказано подробно в специальных руководствах по практическому проведению термохимических измерений.
На основе калориметрических определений накоплено много данных о тепловых эффектах различных химических реакций, процессов растворения, плавления, испарения и пр.