Термодинамические основы холодильных машин
Рабочее вещество в циклах холодильных машин участвует в различных термодинамических процессах. От того, как совершаются эти процессы, зависит эффективность машины. Термодинамический анализ эффективности работы машины основывается на первом и втором законах термодинамики. Этот анализ позволяет указать на те элементы машины, улучшение которых способно больше всего повлиять на рост общей эффективности.
Первый закон термодинамики является одним из самых общих выражения закона сохранения и превращения энергии. В случае, когда осуществляется подвод теплоты к телу, температура тела повышается, а вследствие увеличения объёма тела производится внешняя работа. Следовательно, подведённая к телу теплота расходуется на увеличение внутренней энергии тела U и на совершение работы L:
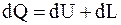 . .
|
Внутренняя энергия представляет собой сумму кинетической и потенциальной энергии частиц, составляющих систему.
В общем случае:
 . .
|
Для идеального газа:
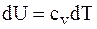 .
.
Работа представляет собой одну из форм превращения энергии. Во многих случаях единственным видом работы является работа расширения против сил внешнего давления:
dl = Pdv.
В конечном процессе (1–2) работа расширения (сжатия):
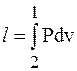 . .
|
В общем случае:
l = f(P, v),
а величина vdP является величиной технической работы.
Для условий адиабатного процесса 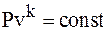 работа расширения может быть выражена:
работа расширения может быть выражена:
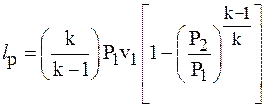 . .
|
Работа сжатия может быть выражена:
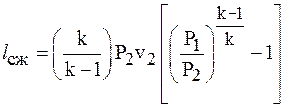 , ,
|
где 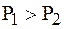 .
.
В политропных процессах расширения (сжатия) k = n.
Второй закон термодинамики формулирует необратимость всех реальных процессов.
Обратимыми процессами следует считать такие процессы, которые можно провести в прямом, а затем в обратном направлении через ту же последовательность промежуточных состояний.
Второй закон в холодильной технике устанавливает, что теплота не может самостоятельно переходить от системы с меньшей температурой к системе с большей температурой. Перенос теплоты от системы с меньшей температурой к системе с большей температурой можно осуществить затратой работы или подводом другой энергии.
Направление процесса теплообмена системы с окружающей средой характеризуется параметром состояния – энтропией:
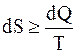 .
.
Для обратимых круговых процессов и для адиабатически изолированных систем:
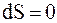 .
.
Потеря работоспособности из-за необратимости реальных процессов определяется уравнением:
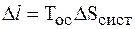 , ,
|
где 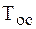 – температура окружающей среды;
– температура окружающей среды; 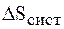 – изменение энтропии системы.
– изменение энтропии системы.