Обратный осмос и ультрафильтрация
Обратный осмос - это способ разделения растворов путем их фильтрования под давлением через полупроницаемые мембраны, пропускающие растворитель и задерживающие молекулы или ионы растворенных веществ.
Ультрафильтрацией называется процесс разделения, фракционирования и концентрирования растворе] с помощью полупроницаемых мембран.
При ультрафильтрации исходный раствор разделяется на два принципиально новых продукта: низкомолекулярный (фильтрат) и высокомолекулярный (концентрат).
Фильтрат проходит сквозь мембрану и удаляется через дренажную систему, а высокомолекулярный продукт концентрируется.
Примеры: позволяет выделять молочные белки из вторичных продуктов молочной промышленности и ценные вещества из других растворов. Ультрафильтрация заменяет пастеризацию пива. При этом из пивг удаляются бактерии и высокомолекулярные вещества, ухудшающие его качество и снижающие стабильность. Стоимость обработки пива ультрафильтрацией в 2,5 раза ниже, чем пастеризацией. Обратным осмосом концентрируют яичный белок. При этом не происходит денатурирование протеинов и получают яичный белок с содержанием до 30 % протеинов.
Теоретические основы разделения обратным осмосом и ультрафильтрацией
В основе метода разделения растворов обратным осмосом лежит явление самопроизвольного перехода растворителя через полупроницаемую мембрану в раствор (рис. 1). Если давление над раствором ниже осмотического ( ), то растворитель будет переходить в раствор до достижения осмотического равновесия в системе.
), то растворитель будет переходить в раствор до достижения осмотического равновесия в системе.
Равновесное состояние наступает, когда гидростатическое давление между раствором и растворителем, определяемое разностью уровней, станет равным осмотическому давлению ( ).
).
Если после достижения осмотического равновесия со стороны раствора приложить давление, превышающее осмотическое ( ), то растворитель начнет переходить из раствора в обратном направлении. В этом случае будет иметь место обратный осмос. Растворитель, прошедший через мембрану, называют фильтратом.
), то растворитель начнет переходить из раствора в обратном направлении. В этом случае будет иметь место обратный осмос. Растворитель, прошедший через мембрану, называют фильтратом.

Дв. с. процесса обратного осмоса является перепад давления  \, где
\, где  — избыточное давление под раствором;
— избыточное давление под раствором;  — осмотическое давление раствора. Если в процессе обратного осмоса наблюдается некоторый переход через мембрану растворенного вещества, то при расчете дв. с. следует учитывать осмотическое давление фильтрата
— осмотическое давление раствора. Если в процессе обратного осмоса наблюдается некоторый переход через мембрану растворенного вещества, то при расчете дв. с. следует учитывать осмотическое давление фильтрата  , прошедшего через мембрану. Тогда
, прошедшего через мембрану. Тогда  ;.
;.
Для приближенного расчета осмотического давления может быть использована формула Вант -Гоффа:
 ,
,
где:  - мольная доля растворимого вещества.
- мольная доля растворимого вещества.  — газовая постоянная: Т— абсолютная температура раствора, К.
— газовая постоянная: Т— абсолютная температура раствора, К.
Осмотические давления растворов могут достигать десятков МПа. Давление в обратноосмотических установках должно быть значительно больше осмотического, так как эффективность процесса определяется дв. с. — разностью между рабочим и осмотическим давлением. Так, при осмотическом давлении морской воды, содержащей 35% солей, равном 2,45 МПа, рабочее давление в опреснительных установках должно составлять около 7,85 МПа.
Ультрафильтрацию применяют при разделении систем, в которых молекулярная масса растворенных в растворителе компонентов значительно превышает молекулярную массу растворителя. При разделении водных растворов ультрафильтрацию используют, когда растворенные компоненты имеют молекулярную массу 500 и выше. Дв. с. ультрафильтрации — разность рабочего и атмосферного Р. Обычно ультрафильтрацию проводят при невысоких Р, равных 0,1... 1,0 МПа.
Ультрафильтрация протекает под действием перепада давления до мембраны и после неё. В зависимости от назначения процесса ультрафильтрации применяют мембраны, которые пропускают растворитель и преимущественно низкомолекулярные соединения (при разделении высоко- и низкомолекулярных соединений), растворитель и определенные фракции высокомолекулярных соединений (при фракционировании высокомолекулярных соединений), только растворитель (при концентрировании высокомолекулярных соединений).
Разделение обратным осмосом и ультрафильтрацией происходит без фазовых превращений. Работа  (Дж) расходуется на создание давления в жидкости и продавливание ее через мембраны:
(Дж) расходуется на создание давления в жидкости и продавливание ее через мембраны:

где:  — р-та на сжатие жидкости, Дж;
— р-та на сжатие жидкости, Дж;  — р-та на продавливание жидкости через мембрану, Дж.
— р-та на продавливание жидкости через мембрану, Дж.
Так как жидкость несжимаема, величиной  обычно пренебрегают. Р-та на продавливание ж-ти:
обычно пренебрегают. Р-та на продавливание ж-ти:

где  — перепад давления на мембране; Н/м2;
— перепад давления на мембране; Н/м2; 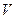 — объем продавливаемой жидкости м3.
— объем продавливаемой жидкости м3.
Сравним работы на продавливание 1 м3 воды через мембрану и работу на испарение 1 м3 воды.
В первом случае при давлении р = 4,9 МПа работа на продавливание составляет 4,90 МДж, во втором случае (при г (уд. теплота парообразования)=2260 кДж/кг) она равна 2270 МДж. Из сравнения этих величин видно, что расход энергии на разделение об. ос. значительно ниже, чем на испарение ж-ти.
Разделение методами обратного осмоса и ультрафильтрации принципиально отличается от обычного фильтрования. При обратном осмосе и ультрафильтрации образуются два раствора: концентрированный и разбавленный, в то время как при фильтровании осадок откладывается на фильтровальной перегородке. В процессе обратного осмоса и ультрафильтрации накопление растворенного вещества у поверхности мембраны (вследствие концентрационной поляризации) недопустимо, так как при этом резко снижаются селективность (разделяющая способность) и проницаемость (удельная производительность) мембраны, сокращается срок ее службы.
Селективность  (в %) процесса разделения на полупроницаемых мембранах определяется по формуле (
(в %) процесса разделения на полупроницаемых мембранах определяется по формуле ( , где
, где 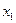 и
и  — концентрации растворенного вещества соответственно в исходном растворе и фильтрате. Иногда
— концентрации растворенного вещества соответственно в исходном растворе и фильтрате. Иногда  называют коэффициентом солезадержания.
называют коэффициентом солезадержания.
Проницаемость  [в л/м2ч)] при данном давлении выражается соотношением
[в л/м2ч)] при данном давлении выражается соотношением  , где
, где 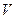 — объем фильтрата, л;
— объем фильтрата, л; 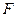 —рабочая площадь поверхности мембраны, м2;
—рабочая площадь поверхности мембраны, м2; 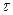 — продолжительность процесса, ч.
— продолжительность процесса, ч.
Мембраны должны обладать следующими свойствами: высокой разделяющей способностью (селективностью); высокой удельной производительностью (проницаемостью); постоянством своих характеристик в процессе эксплуатации; химической стойкостью в разделяющей среде; механической прочностью; невысокой стоимостью.
На селективность и проницаемость мембран большое влияние оказывает гидратирующая способность ионов. Гидратация заключается в том, что ионы растворенного вещества окружены растворителем и движутся с некоторой его частью, взаимодействующего с ним. Молекулы воды, расположенные в непосредственной близости от ионов растворенного вещества, образуют гидратную оболочку. На поверхности и внутри капилляров мембраны образуется слой связанной воды толщиной  физико-механические свойства которой отличаются от характеристик жидкости в объеме.
физико-механические свойства которой отличаются от характеристик жидкости в объеме.