Механизм присоединения-отщепления
Механизм этой реакции состоит из двух стадий:
1. атака нуклеофила по углеродному атому, связанному с галогеном, с образованием анионного сигма-комплекса;
2. реароматизация – отщепление аниона галогена от sp3-углерода в анионном s-комплексе.
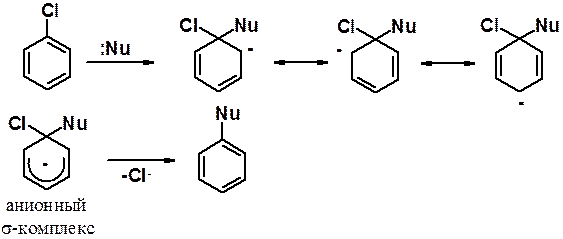
Строение анионного s-комплекса подобно строению s-комплекса, образующегося в ходе реакции ароматического электрофильного замещения. Один углерод находится в тетраэдрической гибридизации и не участвует в делокализации p-электронов. На пяти sp2-углеродах делокализованы 6 p-электронов.
Анионные s-комплексы часто называют комплексами Мейзенгеймера, который в 1902 г первым среди химиков-органиков выделил промежуточный продукт реакции.
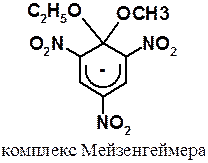
Энергетическая диаграмма реакции показана на рис. 25.1.
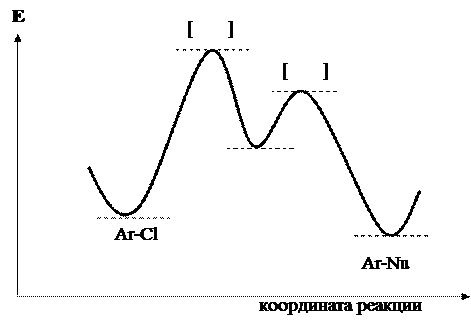

Рис. 25.1. Энергетическая диаграмма реакции присоединения-отщепления
Первая стадия (образование s-комплекса) является лимитирующей. Это доказано влиянием природы галогена на скорость замещения. Если образование или разрыв связи углерод-галоген происходит в лимитирующей стадии, скорость реакций будет зависеть от природы галогена. В эксперименте выраженной зависимости скорости реакции от природы галогена не обнаружено. Следовательно, разрыв связи углерод-галоген происходит в быстрой стадии реакции.
Акцепторые группы обладают дезактивирующими свойствами в реакциях ароматического электрофильного замещения. Поскольку в реакциях присоединения-отщепления ароматический цикл атакует частица с противоположным знаком, очевидно, что в реакциях с нуклеофилами акцепторы – активирующие заместители, доноры – дезактивирующие.
Наличие в положениях 2 или/и 4 или/и 6 электроноакцепторных групп увеличивает реакционную способность галогена в реакциях присоединения-отщепления. Причем, чем больше акцепторов в указанных положениях, тем легче замещается галоген.
Если в положениях 2 или/и 4 или/и 6 расположены электронодонорные группы, реакционная способность галогена в реакциях присоединения-отщепления снижается. Причем, чем больше доноров в указанных положениях, тем труднее происходит замещение галогена.
Если акцепторные или донорные группы расположены в положениях 3 или/и 5 их активирующее или дезактивирующее действие выражено очень слабо.
Для объяснения изменений реакционной способности ароматических галогенопроизводных надо рассмотреть стабильность промежуточно образующегося в реакции анионного s-комплекса, который ближе всего по энергии к вышей энергетической точке реакции – активированному комплексу первой стадии реакции. Рассмотрим на примере нитрогруппы.
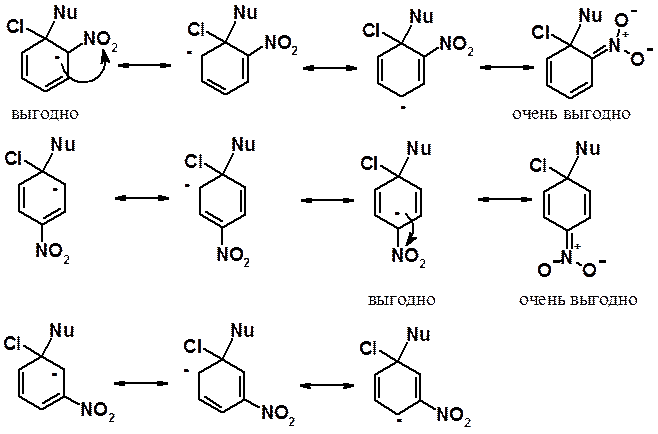
Если акцепторная группировка расположена в орто- или пара-положениях, можно отметить две выгодные граничные структуры, наличие которых позволяет сделать вывод о стабилизационном влиянии акцептора на анионный s-комплекса. Если нитрогруппа или любой акцептор находятся в мета-положении к галогену, такого выраженного стабилизирующего действия они не оказывают. Незначительная активация вызывается только общим - I-эффектом.
Влияние донорных группировок.
При расположении донорной группы в орто- или пара-положениях, можно отметить две невыгодные граничные структуры, наличие которых позволяет сделать вывод о дестабилизационном влиянии донорной группы на анионный s-комплекс и уменьшении подвижности галогена. Наличие донора в мета-положении к галогену, выраженного дестабилизирующего действия они не оказывают. Некоторая дезактивация атома галогена вызывается только общим + I-эффектом.

Увеличение числа акцепторных группировок приводит к большей стабилизации комплекса Мейзенгеймера, за счет уменьшения электронной плотности в бензольном кольца. Сам комплекс Мейзенгеймера – твердое устойчивое вещество красного цвета.
При наличии в молекуле нескольких донорных групп ситуация обратная.