Свойства.
Кислые соли проявляют свойства кислот, взаимодействуют с металлами, оксидами металлов, гидроксидами металлов, солями.
Например:
2KНSO4 + Mg = H2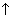 + MgSO4 + K2SO4,
+ MgSO4 + K2SO4,
2KHSO4 + MgO = H2O + MgSO4 + K2SO4,
2KHSO4 + 2NaOH = 2H2O + K2SO4 + Na2SO4,
2KHSO4 + Cu(OH)2 = 2H2O + K2SO4 + CuSO4,
2KHSO4 + MgCO3 = H2O + CO2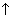 + K2SO4 + MgSO4,
+ K2SO4 + MgSO4,
2KHSO4 + BaCl2 = BaSO4 + K2SO4 + 2HCl.
+ K2SO4 + 2HCl.
Любую соль можно получить соответствующей реакцией нейтрализации. Например, сульфит натрия образуется в реакции между сернистой кислотой и основанием (едким натром). При этом на 1 моль кислоты требуется взять 2 моля основания:
| H2SO3 | + | 2 NaOH | = | Na2SO3 | + | 2 H2O |
| сульфит натрия (средняя соль) |
Если взять только 1 моль основания – то есть меньше, чем требуется для полной нейтрализации, то образуется кислая соль – гидросульфит натрия:
| H2SO3 | + | NaOH | = | NaHSO3 | + | H2O |
| гидросульфит натрия (кислая соль) |