Измерение теплоемкости материалов
Цель работы: Экспериментальное определения теплоемкости материалов.
Оборудование: Весы, разновес, калориметр, цилиндр металлический с известной теплоемкостью, мензурка, нагреватель, крючок.
Краткая теория:
Все макроскопические тела и системы тел помимо механической энергии, обусловленной их движением и взаимодействием, обладают энергией, зависящей от их внутреннего состояния. Эту энергию, являющуюся энергией движения и взаимодействия между собой всех частиц, из которых состоит тело, называют внутренней.
К внутренней энергии, относится кинетическая энергия теплового движения молекул и атомов, входящих в состав данного тела, кинетическая энергия электронов, движущихся в атомах вокруг ядер, потенциальная энергия взаимодействий между собой молекул, атомов, электронов и ядер, нуклонов в ядре и т.д. В понятие внутренней энергии не входит кинетическая и потенциальная энергия данного тела как единого целого.
Внутренняя энергия однозначно определяется совокупностью параметров, характеризующих состояние данной системы, т.е. является однозначной функцией состояния этой системы.
Внутреннюю энергию принято обозначать буквой U.
В тепловых явлениях, протекающих при температурах, далеких от температур фазовых переходов, изменение внутренней энергии DU связано с изменением кинетической и потенциальной энергии молекул, а остальные компоненты внутренней энергии при этом не изменяются. Поэтому в подобных процессах можно считать, что внутренняя энергия тела равна сумме кинетических энергий хаотического теплового движения всех молекул относительно центра масс этого тела и потенциальных энергий взаимодействия всех молекул между собой.
При изменении состояния тела его внутренняя энергия изменяется. Например, при повышении температуры тела его внутренняя энергия увеличивается, так как увеличивается средняя кинетическая энергия движения молекул этого тела. С понижением температуры внутренняя энергия тела уменьшается.
Внутренняя энергия тел может изменятся различными способами. Например, внутренняя энергия изменяется при совершении механической работы внешними силами над данным телом при его деформации, а также без совершения работы, когда тело находится в контакте с другим елом (или средой), имеющим более высокую или более низкую температуру, чем данное тело.
Процесс изменения внутренней энергии тела без совершения механической работы называют теплообменом или теплопередачей. Существуют три вида теплопередачи: конвекция, теплопроводность и излучение.
При теплообмене не происходит превращение энергии из одного вида в другой. Процесс теплообмена состоит в том, что часть внутренней энергии от более горячего тела передается менее горячему телу (или среде).
Для характеристики процессов теплопередачи введено понятие количества теплоты называют величину, являющуюся количественной мерой изменения внутренней энергии тела в процессе теплообмена.
Необходимо помнить, что тело может отдавать или получать только энергию, а количество теплоты Q является лишь численным эквивалентом энергии, отданной или полученной телом в процессе теплообмена.
Количество теплоты зависит от рода процесса и не является функцией состояния системы.
Количество теплоты, необходимое для нагревания тела, происходящего без фазовых превращений (без изменения агрегатного состояния вещества):
 (1)
(1)
где с - удельная теплоемкость тела, определяемая отношением количества переданной теплоты к массе m тела, и произошедшему при этом изменению температуры DT, m - масса тела, DT - разность конечной и начальной температур данного тела.
Количество теплоты, которое нужно сообщить телу, чтобы повысить его температуру на один Кельвин называется теплоемкостью этого вещества. При остывании на один Кельвин, тело отдает такое же количество теплоты. Теплоемкость тела пропорциональна массе тела и зависит от вещества, из которого оно состоит. В системе единиц СИ теплоемкость измеряется в Дж/К.
Для характеристики тепловых свойств вещества принимают теплоемкость единицы массы этого вещества. Эта характеристика называется удельной теплоемкостью. Она равна отношению теплоемкости данного тела к его массе. Удельная теплоемкость с системе СИ измеряется в Дж/(кг×К).
Экспериментально удельную теплоемкость металлического тела определяется при помощи калориметра и термометра. Простейший калориметр состоит из отполированного металлического стакана, поставленного внутри другого стакана на пробках (с целью тепловой изоляции). Внутренний стакан наполняется водой или другой жидкостью с известной удельной теплоемкостью. Тело, нагретое до определенной температуры t, опускают в калориметр. Пусть до опускания тела температура жидкости в калориметре была t1, а после того, как установится тепловое равновесие жидкости и опущенного в него тела их общая температура станет равной q.
Из закона сохранения энергии следует, что:
Q = Q1 +Q2,, (2)
где количество теплоты Q, отданное нагретым телом, равно сумме количества теплоты Q1, полученного водой, и Q2, полученного калориметром.
Учитывая (1) перепишем (2) в виде:
сm(t-q) = c1m1(q-t1) +c2m2(q-t1), (3)
где c1 и m1 - удельная теплоемкость и масса воды в калориметре, c2 и m2 - удельная теплоемкость и масса калориметра. Это уравнение называется уравнением теплового баланса. Из него найдем удельную теплоемкость тела:
 (4)
(4)
Можно подойти к решению этой задачи по другому, предположим, что потери энергии в рамках одного эксперимента, будут одинаковы. Тело с известной удельной теплоемкостью, нагретое до определенной температуры t, опускают в калориметр, температура в котором изменяется. Тогда уравнение теплового баланса примет вид:
cm(t-q) = c1m1(q-t1) + Qпотери,, (5)
где Qпотери - количество теплоты, получаемое калориметром и окружающей средой, следовательно:
Qпотери, = cm(t-q) - c1m1(q-t1). (6)
Если тело с неизвестной удельной теплоемкостью, нагретое до той же температуры, опустить в калориметр, тогда уравнение теплового баланса примет вид:
cx mx (t-qx) = c1m¢1(q - t¢1) + Qпотери,, (7)
где m¢1 - масса воды в калориметре, а t¢1 - температура воды в данном эксперименте. Тогда:
 (8)
(8)
Подставив значение (6) в (8) получим:
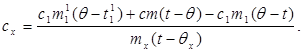 (9)
(9)
Таблица 1.
| Вещество | Удельная теплоемкость некоторых веществ. с, кДж/(кг×К) |
| Алюминий | 0,92 |
| Железо | 0,46 |
| Латунь | 0,38 |
| Медь | 0,38 |
| Никель | 0,46 |
| Олово | 0,25 |
| Свинец | 0,13 |
| Вода | 4,2 |