ВОЛНОВЫЕ СВОЙСТВА ЭЛЕКТРОНА
В 1924 г. французский физик Луи де Бройль (1892—1987) предположил, что все частицы вещества, подобно свету, обладают волновыми свойствами. Связь между волновыми и корпускулярными свойствами частиц такая же, как и между соответствующими свойствами света. Энергия частицы Е равна энергии кванта волнового поля с частотой v, т. е. Е = h v, где h — постоянная Планка, а импульс частицы р = hk, где к — волновое число, h =h/2n. Поведение частиц, так же как при рассмотрении фотонов, описывалось с помощью волнового поля, интенсивность которого определяла вероятность того, что частица может быть обнаружена в определенной области пространства. Гипотеза де Бройля основывалась на сходстве уравнений, описывающих поведение лучей света и частиц вещества, и носила исключительно теоретический характер. Для ее подтверждения или опровержения требовались экспериментальные факты.
Первое опытное подтверждение гипотезы де Бройля было получено в опытах американских исследователей Девиссона и Джермера в 1927 г., изучавших рассеяние электронов на монокристалле никеля. Схема эксперимента приведена на рисунке.
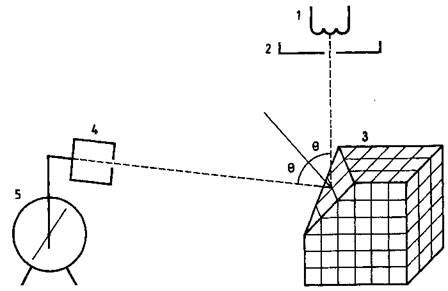
Схема эксперимента Девиссона и Джермера
Электроны, вылетающие из раскаленной нити 1, попадали в ускоряющее электрическое поле, создаваемое между электродами 1 и 2, с разностью потенциалов U, в котором они приобретали кинетическую энергию mv2/2 = eU.
Пройдя отверстие в электроде 2, электроны попадали на кристалл никеля J, на котором происходило их рассеяние. При помощи детектора, ведерка Фарадея 4, соединенного с электрометром 5, измерялось число электронов, рассеянных на угол 6 от нормали к грани кристалла. Меняя положение детектора, можно было исследовать зависимость числа рассеянных электронов от угла θ при различных значениях энергии электронов.
В опытах Девиссона и Джермера были установлены два замечательных факта:
наблюдалась зависимость числа рассеянных электронов от угла рассеяния, причем максимум числа электронов при данном значении ускоряющего напряжения соответствовал максимуму дифракционной картины, если считать кристалл никеля дифракционной решеткой, а электронам приписать длину волны в соответствии с гипотезой де Бройля;
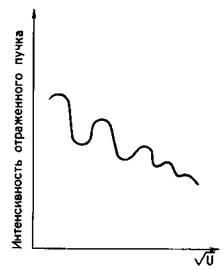
при данном угле падения и изменении скорости электронов l>, что достигалось изменением напряжения U, ускоряющего электроны, интенсивность отраженного пучка периодически изменялась (рис. 113).
|
| Зависимость числа дифрагированных электронов от ускоряющего напряжения |
Электроны вели себя так, будто они были волнами. По результатам эксперимента удалось установить, что длина волны электронов в точности соответствовала предположению Луи де Бройля.
Позже Д ж. П. Т о м с о н у, сыну Дж. Дж. Томсона, удалось получить дифракционную картину, пропуская электроны с энергией нескольких десятков тысяч эВ через тонкие металлические пленки .

|
| Дифракция электронов |
Электронная дифракционная картина очень похожа на рентгеновскую картину дифракции. Чтобы доказать, что она не вызвана вторичными рентгеновскими лучами, возникающими при торможении электронов в веществе, вдоль фотопластинки, где образовывалась электронная дифракционная картина, создавалось магнитное поле. При этом дифракционная картина смещалась поперек поля. Если бы картина создавалась рентгеновскими лучами, то никакого смещения не было бы. Усилия Дж. П. Томсона и К. Дж. Девиссона были отмечены в 1937 г. Нобелевской премией.
Позже дифракцию наблюдали и для более тяжелых заряженных частиц, а также для нейтральных атомов.
В 1949 г. советские физики Л. М. Биберман, Н. Г. Сушкин, В. А. Фабрикант, пропуская через дифракционное устройство слабый по интенсивности поток электронов, обнаружили явление дифракции. В опыте промежуток времени между последовательными прохождениями электронов сквозь мишень в 3 • 104 раз превышал время прохождения отдельного электрона через экспериментальную установку. Этот эксперимент можно интерпретировать так, что каждый электрон дифрагирует, проходя через дифракционную решетку, а вероятность его обнаружения на экране за решеткой определяется волновой функцией, описывающей поведение электрона в свободном пространстве.
Эксперименты по дифракции электронов и других микрочастиц вещества с очевидностью убеждают в том, что вещество, так же как и электромагнитное поле, обладает волновыми свойствами. Это обстоятельство является чрезвычайно удивительным, так как находится в резком противоречии со сложившимися представлениями об окружающем нас физическом мире.
Действительно, модель корпускулы—частицы, с помощью которой в классической физике описывали движение макроскопических тел, подразумевает локализацию этих тел в пространстве, при этом координаты частицы и ее скорость могут быть определены одновременно в любой момент времени. Однако эксперименты по дифракции электронов разрушают эти представления, так как невозможно представить себе электрон проходящим через две щели сразу, как это следует из результатов таких экспериментов.
Переход на язык классического волнового описания поведения электрона также мало что дает, так как электрон во всех экспериментах регистрируется всегда целиком, и все попытки определить, через какую щель в опыте по дифракции все-таки он проходит, оканчиваются неудачей.
Единственным выходом из создавшегося положения явился отказ от классических моделей волны или частицы при описании свойств микрообъектов. С точки зрения такого подхода электрон, так же как и фотон или какой-то другой микрообъект, не является ни волной, ни частицей. Микрообъекты представляют собой квантовые образования; их поведение можно описать с помощью волновой функции, интенсивность которой пропорциональна вероятности нахождения частицы в определенной области пространства в определенный момент времени. Раздел физики, в котором изучается поведение микрочастиц, получил название квантовой механики. С помощью квантовой механики получены наиболее убедительные результаты при объяснении физики атомов и молекул и закономерностей их спектров.