Пример 4.
На реакцию с 13,61 г дигидрофосфата калия израсходовано 5,61 г гидроксида калия. Вычислите молярную массу эквивалента дигидрофосфата калия и напишите уравнения реакции.
Решение.
Молярную массу эквивалента дигидрофосфата калия можно рассчитать по закону эквивалентов:
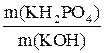 =
=  ,
,
Мэкв.(KH2PO4) =  .
.
Молярная масса эквивалента гидроксида калия рассчитывается из соотношения (пример 1.3):
Мэкв.(KOH) =  =
=  = 56,1 г/моль,
= 56,1 г/моль,
Мэкв.(KH2PO4) = 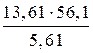 = 136,1 г/моль.
= 136,1 г/моль.
Чтобы написать уравнения реакции, необходимо рассчитать число молей дигидрофосфата калия, вступивших в реакцию. Для этого разделим молекулярную массу дигидрофосфата калия на его молярную массу эквивалента:

 =
=  =1 моль.
=1 моль.
Уравнение реакции имеет вид
KH2PO4 + KOH = K2HPO4 + H2O.
Задания
1. Определите эквивалент и молярную массу эквивалента фосфора, кислорода и брома в соединениях PH3, H2O, HBr.
2. Молярная масса эквивалента трехвалентного металла равна 9 г/моль. Вычислите мольную и атомную массу металла, молярную массу эквивалента его оксида и процентное содержание кислорода в оксиде.
3. Из 1,35 г оксида металла получается 3,15 г его нитрата. Вычислите молярную массу эквивалента металла. Ответ: 32,5 г/моль.
4. Из 1,35 г гидроксида металла получается 2,85 г его сульфата. Вычислите молярную массу эквивалента металла. Ответ: 9 г/моль.
5. Оксид трехвалентного элемента содержит 31,58 % кислорода. Вычислите молярную массу эквивалента, мольную массу и атомную массу этого элемента.
6. Один оксид марганца содержит 22,56 % кислорода, а другой – 50,50 %. Вычислите молярную массу эквивалента и стехиометрическую валентность марганца в этих оксидах. Составьте формулы оксидов.
7. Выразите в молях: а) 6,02×1022 молекул С2Н2; б) 1,80×1014 атомов N2;
в) 3,01×1023 молекул NH3. Чему равна мольная масса указанных веществ?
8. Вычислите эквивалент и молярную массу эквивалента Н3РО4 в реакциях образования: а) гидрофосфата; б) дигидрофосфата; в) ортофосфата.
9. В 2,48 г оксида одновалентного металла содержится 1,84 г металла. Вычислите молярные массы эквивалента металла и его оксида. Чему равна мольная и атомная масса этого металла?
10. 3,04 г некоторого металла вытесняют 0,252 г водорода, 26,965 г серебра и 15,885 г меди из соединений этих элементов. Вычислите молярные массы эквивалентов указанных металлов. Ответ: 12,16 г/моль, 107,86 г/моль, 63,54 г/моль.
11. Оксид металла содержит 28,57 % кислорода, а его фторид 48,72 % фтора. Вычислите молярные массы эквивалента металла и фтора. Ответ: 20,0 г/моль, 19,0 г/моль.
12. Напишите уравнения реакций Fe(OH)3 с хлороводородной (соляной) кислотой, при которых образуются следующие соединения железа: а) дигидроксохлорид; б) гидроксохлорид; в) трихлорид. Вычислите эквивалент и молярную массу эквивалента Fe(OH)3 в каждой из этих реакций.
13. Избытком гидроксида калия подействовали на растворы: а) дигидрофосфата калия; б) дигидроксонитрата висмута(III). Напишите уравнения реакций этих веществ с КОН и определите их эквиваленты и молярные массы эквивалентов.
14. Вещество содержит 38,0 % серы и мышьяк. Молярная масса эквивалента серы 16,0 г/моль. Вычислите молярную массу эквивалента и стехиометрическую валентность мышьяка, составьте формулу данного сульфида.
15. Избытком хлороводородной (соляной) кислоты подействовали на растворы: а) гидрокарбоната кальция; б) гидроксодихлорида алюминия. Напишите уравнения реакций этих веществ с НСl и определите их эквиваленты и молярные массы эквивалентов.
16. При окислении 16,74 г двухвалентного металла образовалось 21,54 г оксида. Вычислите молярные массы эквивалентов металла и его оксида. Чему равна мольная и атомная масса металла?
17. При взаимодействии 3,24 г трехвалентного металла с кислотой выделяется 4,03 л водорода (н. у.). Вычислите молярную массу эквивалента, мольную массу и атомную массу металла.
18. Исходя из мольной массы углерода и воды, определите абсолютную массу атома углерода и молекулы воды. Ответ: 2,0×10–23 г, 3,1×10–27 г.
19. Какой объем при н. у. занимает молярная масса эквивалента кислорода? Вычислите мольную и атомную массу двухвалентного металла, если на окисление 6,34 г этого металла пошло 0,68 л кислорода (н. у.).
20. На нейтрализацию 0,943 г фосфористой кислоты Н3РОз израсходовано 1,291 г КОН. Вычислите эквивалент, молярную массу эквивалента и основность кислоты. Ответ: 0,5 моль, 41 г/моль, 2.
Строение атома