Основные понятия химии 8 класс 2 четверть
| Термин | Определение |
| 1. Количество вещества – | Физическая величина, определяющая количество структурных частиц (атомов, молекул, ионов). n |
| 2. Моль – | Количество вещества, содержащее столько же структурных частиц (атомов, молекул, ионов) сколько содержится атомов в углероде-12 массой 0,012 кг. |
| 3. Число Авогадро– | 6∙1023 моль-1 Постоянная величина, равная отношению числа структурных частиц к соответствующему количеству вещества. |
| 4. Молярная масса – | 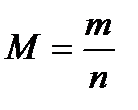 Постоянная величина, равная отношению массы вещества к соответствующему количеству вещества. Постоянная величина, равная отношению массы вещества к соответствующему количеству вещества.
|
| 5. Молярный объем – |
 . Постоянная величина, равная отношению объема вещества к соответствующему количеству вещества. . Постоянная величина, равная отношению объема вещества к соответствующему количеству вещества.
|
| 6. Молярный объем газа при н.у. – | 22,4 л/моль при 0°С и 101,325 кПа. |
| 7. Бинарные соединения – | Сложные вещества, состоящие из двух элементов. |
| 8. Степень окисления – | Условный заряд атомов химических элементов в соединении, вычисленный на основе предположения, что все соединения (и ионные, и ковалентно-полярные) состоят только из ионов. |
| 9. Оксиды – | Бинарные соединения, в которых кислород имеет степень окисления –2. |
| 10. Основания – | Сложные вещества, состоящие из катионов металлов и связанных с ними гидроксид-анионов. |
| 11. Кислоты – | Сложные вещества, состоящие из катионов водорода и анионов кислотного остатка. |
| 12. Соли – | Сложные вещества, состоящие из катионов металлов и анионов кислотного остатка. |
| 13. Формулы кислот – | HCl хлороводородная (соляная), HF фтороводородная (плавиковая), HBr бромоводородная, HI иодоводородная, H2S cероводородная, HNO3 азотная, H2SO4 серная, H2SO3 сернистая, H2CO3 угольная, H2SiO3 кремниевая, H3PO4 фосфорная. |
| 14. Названия анионов солей – | Cl- хлориды, F- фториды, Br- бромиды, I- иодиды, S2- сульфиды, NO3 - нитраты, SO4 2- сульфаты, SO3 2- сульфиты, CO3 2- карбонаты, SiO3 2-силикаты, PO4 3- фосфаты. |
| 15. Правила определение степеней окисления - | 1. В простых веществах степень окисления равна 0. 2. Алгебраическая сумма степеней окисления в нейтральной молекуле равна 0, в сложном ионе – заряду иона. |
| 16. Постоянные степени окисления | +1 щелочные металлы (Li, Na, K, Rb, Cs) и Ag +2 все металлы II группы кроме ртути +3 Al -1 F -2 O (кроме гидридов металлов) |