Задача. Рассчитать массовую долю раствора, содержащего 50 г хлорида кальция и 250 г воды.


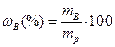
Задача. В 150 г воды растворено 30 г кристаллогидрата  . Вычислить массовую долю кристаллогидрата и безводного сульфата железа (II) в растворе.
. Вычислить массовую долю кристаллогидрата и безводного сульфата железа (II) в растворе.
Решение. 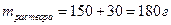
 или 16,7%
или 16,7%
Молярная масса  . Равна 278 г/моль, а
. Равна 278 г/моль, а 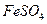 - 152 г/моль. В 30 г кристаллогидрата содержится 16,4 г безводной соли. Тогда
- 152 г/моль. В 30 г кристаллогидрата содержится 16,4 г безводной соли. Тогда 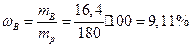
Задача. При 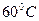 насыщенный раствор
насыщенный раствор 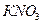 содержит 52,4% соли. Найти коэффициент растворимости соли при этой температуре.
содержит 52,4% соли. Найти коэффициент растворимости соли при этой температуре.
Решение. Коэффициент растворимости находим из пропорции:
На 47,6 г воды приходится 52,4 г 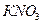 .
.
На 100 г « Х г 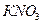
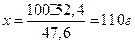
Таким образом, растворимость 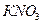 при
при 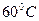 равна 110 г в 100 г воды.
равна 110 г в 100 г воды.
Задача. Вычислить моляльность, нормальность и молярность 15%-ного раствора (по массе) серной кислоты, если г/мл.
Решение. Для расчета используем 100 г раствора, который содержит 15 г серной кислоты.
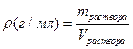
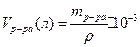
 объем раствора в литрах.
объем раствора в литрах.
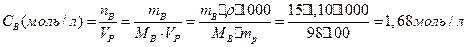
Моляльную конц. рассчитываем по формуле

Нормальность раствора рассчитываем по формуле
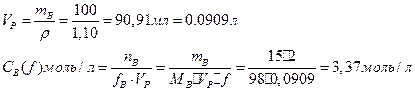
Молярную долю рассчитываем по выражению

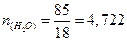
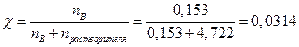
ЗАДАЧИ ДЛЯ САМОСТОЯТЕЛЬНОЙ РАБОТЫ
- При упаривании раствора хлорида натрия массой 500г с массовой долей соли 1% получен новый раствор массой 150г. Вычислите массовую долю и молярную долю соли в новом растворе.
- Вычислите рН 3,8% раствора HCl (r=1,017 г/мл).Какой объем 2М раствора гидроксида калия потребуется для нейтрализации 10мл указанного раствора HCl.
3. Вычислите рН, молярную, моляльную и моль-эквивалентную концентрации 20% раствора серной кислоты плотностью 1,12 г/мл.
- Сколько воды надо добавить к раствору массой 3кг и с массовой долей соли 20% для получения раствора с массовой долей 15%?
- Вычислите молярную, моляльную концентраци и молярную долю гидроксида натрия в растворе, содержащем 12 г гидроксида натрия в 50 г воды (rр-ра = 1,2 г/мл).
6. Сколько воды необходимо прибавить к 80 мл 20%-го раствора хлорида натрия (ρ= 1,148 г/мл), чтобы получить 10%- й раствор (r=1,07 г/мл)? Вычислите молярную концентрацию последнего.
- Вычислите молярность, моляльность и мольную долю вещества в растворе Н3РО4 с массовой долей 30% и плотностью 1,18 г/мл.
- Растворимость гидрокарбоната натрия в воде при 25°С 24,8г. Вычислите массовую долю и молярную концентрацию этого раствора, если r=1,1 г/мл.
- Вычислите произведение растворимости PbBr2при 25°C, если растворимость соли при этой температуре равна 1,32×10-2 моль/л.
- Вычислите массы воды и CaCl2×6H2O, необходимые для приготовления 500 мл раствора хлористого кальция с массовой долей соли 40% и плотностью 1,4 г/мл. Определите молярную и моляльную концентрацию раствора.
- Растворимость сульфата натрия в воде при 25°С 27,9г. Вычислите массовую долю и моляльную концентрацию этого раствора, если r=1,28 г/мл.
- Растворимость хлорида натрия при 20°С составляет 35,9г, а при 60°С- 37,22г. Вычислите массу осадка, который образуется при охлаждении 500г раствора насыщенного при 60°С до 20°С.
- Вычислите произведение растворимости хромата серебра (Ag2CrO4), если при 18°С в 500мл воды растворяется 0,0166г этой соли.
14. Вычислите объем концентрированной серной кислоты H2SO4 с плотностью 1,84 г/мл и массовой долей 98% следует взять для получения 800мл раствора с концентрацией 3М?
- Сколько воды надо добавить к раствору массой 3кг и с массовой долей соли 20% для получения раствора с массовой долей 5 %?
2. 6. Определить массовую долю вещества в растворе, полученном смещением 300 г 25%-ного и 400 г 40%-ного (по массе) растворов этого вещества
- Вычислите молярную, моляльную концентрации и мольную долю нитрата натрия в 10% растворе (r= 1,06 г/мл).
- 4Сколько воды надо добавить к раствору массой 3кг и с массовой долей соли 20% для получения раствора с массовой долей 15%?
- Вычислите объем 37% раствора азотной кислоты (r=1,23г/мл), необходимый для приготовления 1л 25% (r=1,14г/мл).
- Вычислите молярную, моляльную, моль-эквивалентную концентрацию 10% раствора серной кислоты с плотностью 1,06 г/мл.
- 3. Вычислите молярную и моляльную концентрации 20 и 40% растворов этанола в воде, если плотности растворов равны 0,969 и 0,935 г/мл соответственно. Плотность этанола равна 0,789 г/мл.
8. Вычислите объем воды, который необходимо прибавить к 10 мл 20%-го раствора хлорида натрия (ρ= 1,152 г/мл), чтобы получить 4%-й раствор?
- Растворимость сульфата натрия в воде при 25°С 27,9г. Вычислите массовую долю и моляльную концентрацию этого раствора, если r=1,28 г/мл.
10. Вычислите молярную, моляльную, моль-эквивалентную концентрацию 15% раствора фосфорной кислоты с плотностью 1,085 г/мл.
- При упаривании раствора хлорида натрия массой 500г с массовой долей соли 1% получен новый раствор массой 150г. Вычислите массовую долю и молярную долю соли в новом растворе.
- Вычислите массы воды и CaCl2×6H2O, необходимые для приготовления 500 мл раствора хлористого кальция с массовой долей соли 40% и плотностью 1,4 г/мл. Определите молярную и моляльную концентрацию раствора.
- Вычислите молярность, моляльность и мольную долю вещества в растворе Н3РО4 с массовой долей 30% и плотностью 1,18 г/мл.
- 4. Вычислите молярную и моляльную концентрации 10% раствора ортофосфорной кислоты, если r=1,055 г/мл.
15. 4. Вычислите молярную, моляльную концентрации и рН 10% раствора гидроксида натрия плотностью 1,05 г/мл.
- 3. Вычислите молярную и моляльную концентрацию 20% раствора NH4Cl (r=1,057 г/мл). Рассчитать мольную долю соли.
- Рассчитайте молярную, моляльную концентрации и рН 10% раствора гидроксида натрия плотностью 1,05 г/мл.
18. Вычислите объем 37% раствора азотной кислоты (r=1,23г/мл), необходимый для приготовления 1л 25% (r=1,14г/мл).
- Растворимость гидрокарбоната натрия в воде при 25°С 24,8г. Вычислите массовую долю и молярную концентрацию этого раствора, если r=1,1 г/мл.
- Вычислите произведение растворимости PbBr2при 25°C, если растворимость соли при этой температуре равна 1,32×10-2 моль/л.
- Плотность раствора карбоната калия 1,22 г/мл. Из 1 л раствора действием соляной кислоты выделено 33,6 л СО2.Вычислите моляльную концентрацию раствора и мольную долю соли.
- Вычислите молярную, моляльную, моль- эквивалентную концентрацию 10% раствора сульфата меди (r=1,04 г/мл).
- 5. Вычислите произведение растворимости хромата серебра (Ag2CrO4), если при 18°С в 500мл воды растворяется 0,0166г этой соли.
24. Вычислите объем концентрированной серной кислоты H2SO4 с плотностью 1,84 г/мл и массовой долей 98% следует взять для получения 800мл раствора с концентрацией 3М?
25. 6. К 100мл 10% раствора NaCl (r= 1,12 г/мл) прилили 100 мл 0,02 М раствор нитрата серебра. Вычислите концентрацию Cl- и Ag+ в растворе, если ПР(AgCl)= 1,8×10-10.
- При упаривании раствора хлорида натрия массой 500г с массовой долей соли 1% получен новый раствор массой 150г. Рассчитать массовую долю и молярную долю соли в новом растворе.
27. Сколько воды необходимо прибавить к 80 мл 20%-го раствора хлорида натрия (ρ= 1,148 г/мл), чтобы получить 10%- й раствор (r=1,07 г/мл)? Рассчитайте молярную концентрацию последнего.