Непредельные углеводороды ряда этилена, общая формула состава. Электронное и пространственное строение, химические свойства этилена
Непредельные углеводороды ряда этилена, или алкены, – это углеводороды с общей формулой CnH2n, молекулы которых содержат одну двойную связь. Атомы C, связанные двойной связью, находятся в состоянии sp2-гибридизации, двойная связь является сочетанием  - и
- и  -связей. По своей природе
-связей. По своей природе  -связь резко отличается от
-связь резко отличается от  -связи;
-связи;  -связь менее прочная вследствие перекрывания электронных облаков вне плоскости молекулы.
-связь менее прочная вследствие перекрывания электронных облаков вне плоскости молекулы.
Простейшим алкеном является этилен. Структурная и электронная формулы этилена имеют вид:

В молекуле этилена подвергаются гибридизации одна s- и две p-орбитали атомов C (sp2-гибридизация). Таким образом, каждый атом C имеет по три гибридных орбитали и по одной негибридной p-орбитали. Две из гибридных орбиталей атомов C взаимно перекрываются и образуют между атомами C  -связь. Остальные четыре гибридных орбитали атомов C перекрываются в той же плоскости с четырьмя s-орбиталями атомов H и также образуют четыре
-связь. Остальные четыре гибридных орбитали атомов C перекрываются в той же плоскости с четырьмя s-орбиталями атомов H и также образуют четыре  -связи. Две негибридные p-орбитали атомов C взаимно перекрываются в плоскости, которая расположена перпендикулярно плоскости
-связи. Две негибридные p-орбитали атомов C взаимно перекрываются в плоскости, которая расположена перпендикулярно плоскости  -связей, т.е. образуется одна
-связей, т.е. образуется одна  -связь. Под действием реагентов
-связь. Под действием реагентов  -связь легко разрывается.
-связь легко разрывается.
Этилен – первый член гомологического ряда алкенов.

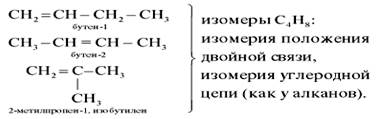
Но молекула бутена-2 может находиться в виде двух пространственных форм – цис- и транс-:

Цис- и трансизомеры, имея различное расположение атомов в пространстве, отличаются многими физическими и химическими свойствами. Таким образом, для алкенов возможны два вида структурной изомерии: изомерия углеродной цепи и изомерия положения двойной связи. Возможна также геометрическая изомерия. Этилен (этен) – бесцветный газ с очень слабым сладковатым запахом, немного легче воздуха, малорастворим в воде. По химическимсвойствам этилен резко отличается от этана, что обусловлено электронным строением его молекулы. Имея в молекуле двойную связь, состоящую из  - и
- и  -связей, этилен способен присоединять два одновалентных атома или радикала за счет разрыва
-связей, этилен способен присоединять два одновалентных атома или радикала за счет разрыва  -связи.
-связи.
• Способность к реакциям присоединения характерна для всех алкенов.
1. Присоединение водорода (реакция гидрирования):
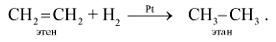
2. Присоединение галогенов (реакция галогенирования):
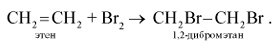
При добавлении к алкену брома (в виде бромной воды) бурая окраска брома быстро исчезает. Эта реакция является качественной на двойную связь.
3. Присоединение галогеноводородов (реакция гидрогалогенирования):

Если исходный алкен несимметричен, то реакция протекает по правилу Марковникова.
Присоединение галогеноводородов к непредельным соединениям идет по ионному механизму.
4. Присоединение воды (реакция гидратации):

Этой реакцией пользуются для получения этилового спирта в промышленности.
• Для алканов характерны реакции окисления:
1. Этилен легко окисляется уже при обычной температуре, например при действии перманганата калия. Если этилен пропускать через водный раствор перманганата калия KMnO4, то характерная фиолетовая окраска последнего исчезает, происходит окисление этилена перманганатом калия (качественная реакция на двойную связь):
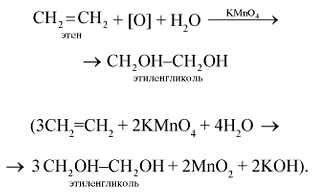
2. Этилен горит светящимся пламенем с образованием оксида углерода(IV) и воды:
C2H4 + 3O2 —> 2CO2 + 2H2O.
3. Большое промышленное значение имеет частичное окисление этилена кислородом воздуха:

• Для этилена, как и для всех непредельных углеводородов, характерны реакции полимеризации. Они протекают при повышенной температуре, давлении и в присутствии катализаторов:
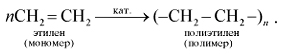
Полимеризация – это последовательное соединение одинаковых молекул в более крупные.
Таким образом, для этилена и его гомологов характерны реакции присоединения, окисления и полимеризации.
3. Как распознать кислоту и щелочь среди трех выданных растворов веществ.
ВЫПОЛНЕНИЕ:
Берем пробу № 1 из трех выданных пробирок
Добавляем раствор метилового оранжевого. В кислой среде окраска розовая, в щелочной – желтая
Берем пробу № 2 и добавляем раствор лакмуса. В кислой среде окраска красная, в щелочной синяя
БИЛЕТ 3