Ионное произведение воды. Водородный показатель
В чистой воде незначительная часть молекул Н2О диссоциирована на ионы:
Н2О 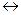 Н++ОН-
Н++ОН-
Измерением электропроводности воды установлено, что при t=22 оС концентрация ионов Н+ и ОН- в чистой воде составляет 10-7г-ион/л:
[Н+]=[ОН-]= 10-7г-ион/л
Произведение концентраций ионов водорода и гидроксила воды называется ионным произведением воды и численно равно 10-14. Ионное произведение воды – величина постоянная не только для воды, но и для разбавленных водных растворов любых веществ. Обозначим эту величину КH2O: КН2О=10-14
1) В нейтральных растворах концентрация ионов водорода и гидроксила одинакова и равна 10-7г-ион/л:
[Н+]=[ОН-]= 10-7 г-ион/л
2) В кислых растворах концентрация ионов водорода выше, чем ионов гидроксила:
[Н+]>[ОН-]
3) В щелочных растворах концентрация ионов гидроксила выше, чем концентрация ионов водорода:
[Н+]<[ОН-]
Но как бы ни менялись концентрации ионов водорода и гидроксила, их произведение остается постоянным и равным (при t=22 оC) 10-14.
Поэтому, зная концентрацию одного из ионов воды, можно вычислить концентрацию другого иона. Пусть концентрация ионов водорода равна:
[Н+] =5*10-4 г-ион/л, тогда концентрация ионов гидроксила:
[ОН-]=  =
= 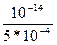 =2*10-11 г-ион/л или 2*10-11 моль/л
=2*10-11 г-ион/л или 2*10-11 моль/л
Реакцию водного раствора принято количественно характеризовать концентрацией ионов водорода. Удобно вместо концентрации ионов водорода указывать взятый с обратным знаком показатель степени, в которую надо возвести число 10, чтобы получить числовое значение концентрации. Эта величина называется водородный показатель и обозначается рН.
Математически рН – это десятичный логарифм концентрации ионов водорода, взятый с обратным знаком:
рН=-lg[H+]
1) В нейтральном растворе рН = 7;
2) В кислом растворе рН < 7;
3) В щелочном растворе рН > 7
Зная рН раствора, можно вычислить концентрации ионов Н+ и ОН-. И, наоборот, по величине концентрации ионов Н+ и ОН- можно вычислить рН раствора.
Примеры решения задач
Пример 1. Вычислить водородный показатель – рН водного раствора КОН, содержащегося в растворе с концентрацией 4,2*10-3 моль/л.
Решение:
Концентрация ионов ОН- равна концентрации самой щелочи в растворе:
[OH-] = 4,2 *10-3 г-ион/л
Определим концентрацию ионов Н+:
[Н+]= 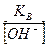 =
= 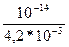 =0,24 *10-11г-ион/л
=0,24 *10-11г-ион/л
Водородный показатель раствора КОН равен: рН=-lg[H+]=-lg 0,24*10-11=11,62.
Пример 2. Определить концентрацию ионов ОН- в растворе, рН которого равен 3,28.
Решение:
рН= -lg [H+]
lg[H+]=-3,28
[H+]=5,25*10-4моль/л или 5,25 *10-4 г-ион/л
Концентрация ионов ОН-:
[ОН-]= 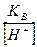 =
= 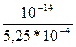 =0,19*10-10 моль/л или 0,19*10-10 г-ион/л
=0,19*10-10 моль/л или 0,19*10-10 г-ион/л
Пример 3 Определить рН 0,17н раствора СН3СООН, константа диссоциации которой равна 1,75*10-5.
Решение:
Константа и степень диссоциации слабого электролита связаны между собой законом разбавления Оствальда:
α=  =
=  =
=  =10-2
=10-2
Определим концентрацию ионов водорода в растворе СН3 СООН:
[Н+]=С* α = 0,17*1*10-2= 0,17*10-2 моль/л или 0,17*10-2 г-ион/л
Водородный показатель СН3СООН:
рН=-lg[H+]=-lg 0,17*10-2=2,77