Тема 3.1. Гравиметрический анализ
Химическое равновесие в анализе. Константа химического равновесия. Применение закона действующих масс к системе «насыщенный раствор - осадок». Понятие о произведении растворимости.
Принцип метода гравиметрии. Гравиметрические методы отгонки (прямой и косвенный). Типы гравиметрических определений. Этапы гравиметрического анализа (взятие навески, растворение навески и подготовка раствора для анализа, осаждение определяемого вещества и отделение его от раствора, фильтрование и промывание осадка, высушивание или прокаливание).
Условия образования и растворения осадка.
Приборы и посуда для гравиметрического анализа.
Расчеты в гравиметрическом анализе.
Общая оценка гравиметрического метода.
Практическая работа № 2
Расчет количества вещества в гравиметрическом анализе.
Методические указания к теме 3.1.
При изучении данной темы, прежде всего, необходимо усвоить закон действующих масс и его применение к системе «насыщенный раствор-осадок», т.к. реакции осаждения труднорастворимых соединений и их растворения широко применяют в аналитической химии для обнаружения ионов и их разделения.
В насыщенном водном растворе малорастворимого в воде сильного электролита устанавливается равновесие между кристаллами твердого вещества (осадком) и его ионами, находящимися в растворе.
Например,
АgСl(тв)D Аg+ + Сl‾
Выражение, отражающее приведенное равновесие, имеет вид:
[Аg+] [Сl‾] = ПРАgСl ,
где [Аg+] и [Сl‾] – равновесные концентрации соответствующих ионов в насыщеном растворе, моль/л;
ПРАgСl – произведение растворимости хлорида серебра.
Таким образом, произведение растворимости – произведение молярных концентраций катионов и анионов малорастворимого сильного электролита в его насыщенном растворе или данной температуре.
Для малорастворимого электролита с формулой МgАh:
ПРМgАn = [Мh+]g [Аg-]h
Использование произведения растворимости позволяет сделать важные для аналитического процесса выводы и произвести необходимые расчеты.
В насыщенном растворе малорастворимого соединения произведение концентраций ионов в растворе равно произведению растворимости. Например, для соединения МА:
[М+] [А‾] = ПРМА
Для этого же соединения, если произведение концентраций его ионов в растворе меньше произведения растворимости, т.е. [М+] [А‾] < ПРМА, раствор не насыщен. Осадок при этом не образуется.
Если произведение концентраций ионов в растворе будет больше произведения растворимости, т.е. [М+] [А‾] > ПРМА, из раствора будет выпадать осадок.
После рассмотрения вышеуказанных вопросов необходимо перейти к изучению гравиметрических методов анализа.
Гравиметрический анализ - совокупность методов количественного анализа, основанных на выделении определяемого количества в виде какого-либо соединения и определения его массы.
В гравиметрическом анализе используются методы:
- отгонки определяемого вещества в виде какого-либо летучего соединения;
- осаждения из раствора в виде малорастворимого соединения.
Чаще всего в гравиметрическом анализе используют методы осаждения, которые включают несколько последовательных операций:
1. Осаждение определяемого компонента в виде малорастворимого соединения, называемого осаждаемой формой.
2. Отделение осадка от раствора фильтрованием.
3. Промывание осадка.
4. Нагревание осадка для удаления воды или его прокаливание для превращения осадка в подходящую для взвешивания химическую формулу, называемую гравиметрической.
5. Взвешивание полученного осадка (гравиметрической формы)
Необходимо усвоить сущность каждой операции гравиметрического анализа и требования, которые предъявляются к осаждаемой и гравиметрической форме.
Примерные решения задач.
Пример 1. Выпадет ли осадок сульфата бария присмешении одинаковых объемов 0,002М растворов сульфата натрия (Na2SО4) и хлоридабария (BaC12)?
Решение:Запишем уравнение химической реакции в краткой ионной форме:
Ва2 + SO  = BaSО4$
= BaSО4$
После смешения растворов сильных электролитов концентрации ионов Ва2+ и SO  :
:
[Ва2+]= С0 (Ва2+) = 0,002 = 0,001 моль/л,
2 2
[SО  ]= С0 (SO
]= С0 (SO  )= 0,002 = 0,001 моль/л,
)= 0,002 = 0,001 моль/л,
2 2
где С0(Ва2+) и С0(SО  ) - концентрации ионов до смешения растворов.
) - концентрации ионов до смешения растворов.
Произведение этих концентраций:
С(Ва2+)С(SО  ) = 1·10-3·1·10-3 = 1·10-6, а ПРВаSО
) = 1·10-3·1·10-3 = 1·10-6, а ПРВаSО  = 1,1·10-10
= 1,1·10-10
Поскольку 1·10-6 > ПРВаSО  то сульфат бария выпадет в осадок.
то сульфат бария выпадет в осадок.
Пример 2. Вычислить растворимость хлорида серебра в молях и миллиграммах на литр в чистой воде при 20ºС, если известно, что при этой температуре ПРAgCl = 1,78·10-10.
Решение:Уравнение, описывающее равновесие в растворе:
AgCl(тв.) D Ag+ + Cl‾
Произведение растворимости для AgCl:
ПРАgС1 = [Аg+] [Cl‾].
Выразим растворимость AgCl в молях на литр:
SAgC1 =  =
=  = 1,33·10-5 моль/л.
= 1,33·10-5 моль/л.
Вычислим растворимость AgCl в миллиграммах на литр:
mАgС1 = n(AgCl)·M(AgCl);
M(AgCl) = 143,3 г/моль, n(AgCl) = SАgСl;
mАgСI = 1,33·10-5·143,3 = 1,91·10-3 г/л = 1,91 мг/л.
Итак, 1 л насыщенного при 20ºС раствора хлорида серебра содержит 1,33·10-5 моль/л или 1,91 мг/л этой соли.
Пример 3. Произведение растворимости CaF2 при 25ºС равно 4,0·10-11. Найти растворимость этой соли, г/л, в чистой воде при той же температуре.
Решение.Уравнение реакции:
СаF2(тв.) D Са2+ + 2F‾
Произведение растворимости
ПРСаF  = [Ca+] [F‾]2.
= [Ca+] [F‾]2.
Найдем растворимость S СаF  моль/л:
моль/л:
[Са2+] = S, [F‾] = 2S;
тогда ПР СаF  = S (2S)2 = 4S3 и
= S (2S)2 = 4S3 и
S = 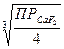 =
=  = 2,15·10-4 моль/л.
= 2,15·10-4 моль/л.
Растворимость CaF2, мг/л:
mСаF  = SМ(CaF2),
= SМ(CaF2),
M(CaF2) = 78,08 г/моль,
mСаF  = 2·15·10-4·78,08 = 1,68·10-2 г/л = 16,8 мг/л.
= 2·15·10-4·78,08 = 1,68·10-2 г/л = 16,8 мг/л.
Таким образом, растворимость фторида кальция в чистой воде составляет 16,8 мг/л.